Questões de Vestibular
Sobre relações da química com as tecnologias, a sociedade e o meio ambiente em química
Foram encontradas 360 questões
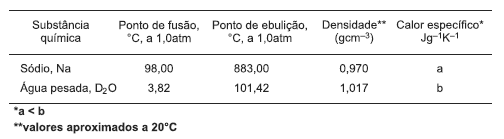
De acordo com as informações do texto, da utilização de sódio no estado líquido, como refrigerante de reatores nucleares avançados de metal líquido e das propriedades físicas desse elemento químico, quando comparadas com as da água pesada, é correto afirmar:
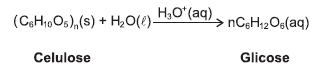
Tendo em vista os principais desafios tecnológicos na produção de etanol celulósico, de segunda geração, a partir de biomassa de cana-de-açúcar, e com base na equação química que representa a hidrólise da celulose, é correto afirmar:
DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

Aquecer uma gordura na presença de uma base consiste em um método tradicional de obtenção de sabão (sal de ácido graxo), chamado de saponificação.
Dentre as opções, a estrutura que representa um sabão é
O nome da Propionibacterium acnes vem da sua capacidade de produzir um ácido carboxílico, o ácido propanoico (também chamado de propiônico), como subproduto de seu metabolismo. Não se conhece o papel desse ácido, se houver, na patologia da acne.
Suponha que um adolescente que sofre de acne resolve passar etanol no rosto e que esse álcool reagirá com o ácido propanoico produzido pelas bactérias. Sobre essa reação de condensação, considere as afirmativas abaixo.
I – Um dos produtos da reação terá uma ligação éster
II – Na reação haverá formação de água.
III – O produto maior terá cinco carbonos.
IV – A reação formará propanoato de etila.
Está correto o que se afirma em:
De acordo com as informações do texto, afirma-se que:

Al 2 ( SO4)3(aq) + 3 Ca (OH)2 (aq) → 2 Al (OH)3(s) + 3 CaSO4 (aq)
A etapa do tratamento da água em que ocorre essa reação é denominada
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0





