Questões de Vestibular
Sobre relações da química com as tecnologias, a sociedade e o meio ambiente em química
Foram encontradas 358 questões
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Si 14 28,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Mn 25 55,0
Fe 26 56,0
Br 35 80,0
Rb 37 85,5
Zr 40 91,0
Ag 47 108,0
Cd 48 112,5
Ba 56 137,0
Pb 82 207,0
U 92 238,0
Pu 94 244,0
Com relação ao ferro, assinale a opção correta.
Ao colocar as bananas em um recipiente fechado o processo de maturação é acelerado, pois

Texto I:
Matar ou morrer
Ao longo dos anos, tem-se tornado cada vez mais necessário aumentar a produtividade agrícola, visando à produção de alimentos. Já nos ambientes urbanos, o controle dos diversos tipos de pragas e insetos é fundamental para a garantia da saúde pública. Para esses fins, passou-se a utilizar, cada vez mais, não só fertilizantes, como também pesticidas, incluindo os inseticidas, herbicidas e fungicidas. Dentre os inseticidas, a Deltametrina é amplamente utilizada no controle de pragas de diversas culturas, no combate de insetos domésticos, dentre outros. O amplo uso da Deltametrina justifica-se por sua potente ação inseticida, toxicidade relativamente baixa em mamíferos e persistência limitada no meio ambiente. Algumas de suas características físicas e químicas estão listadas na tabela abaixo:
TABELA - Características físicas e químicas da Deltametrina
Estado físico pó cristalino
Cor sem cor
Odor sem odor
Densidade (20 ºC) 0,5 g/cm3
Massa Molar 505,24 g/mol
Ponto de fusão 98 – 101 ºC
Ponto de ebulição acima de 300 ºC
Solubilidade em água (20 ºC) < 0,002 mg/L
Solubilidade em solventes orgânicos Solúvel
Solubilidade em Acetona 500 g/L
FONTE: WHO - WORLD HEALTH ORGANIZATION. Environmental Health Criteria 97 – Deltamethrin. Geneva: International Program on Chemical Safety - IPCS, 1990.
A formula estrutural da Deltametrina é apresentada na figura abaixo:

Comumente, a indústria química comercializa o inseticida Deltametrina com as seguintes especificações:
cada 1000 mL contém:
Deltametrina..............25 g
Veículo q.s.p.............1000 mL
No rótulo desse produto há também recomendações para dilução em água para sua aplicação final, de acordo com a tabela abaixo.
Quantidade de água Moscas Insetos rasteiros
1 litro 6 mL 8 mL
10 litros 60 mL 80 mL
20 litros 120 mL 160 mL
Responda a questão com base nas informações dadas sobre o tema “inseticidas” e em seus conhecimentos
de química.
I - O uso da água como solvente para diluição do inseticida Deltametrina, citado no texto I, tem a vantagem econômica de ser barata e acessível. No entanto, o inseticida não formará uma solução em água, dada sua baixa solubilidade nesse meio. II - Utilizando-se a acetona como solvente tem-se a vantagem desta dissolver bem a Deltametrina, de modo a formar uma solução. No entanto, a acetona, além de ser bem mais cara que a água, também é inflamável. Portanto, por questões econômicas e de segurança, o uso desse solvente é não recomendável para diluição do inseticida. III - A Deltametrina mata os insetos principalmente pelo seu mau cheiro, o que provoca sufocamento nos mesmos.
Está(ão) correta(s) a(s) afirmativa(s):
Texto I:
Matar ou morrer
Ao longo dos anos, tem-se tornado cada vez mais necessário aumentar a produtividade agrícola, visando à produção de alimentos. Já nos ambientes urbanos, o controle dos diversos tipos de pragas e insetos é fundamental para a garantia da saúde pública. Para esses fins, passou-se a utilizar, cada vez mais, não só fertilizantes, como também pesticidas, incluindo os inseticidas, herbicidas e fungicidas. Dentre os inseticidas, a Deltametrina é amplamente utilizada no controle de pragas de diversas culturas, no combate de insetos domésticos, dentre outros. O amplo uso da Deltametrina justifica-se por sua potente ação inseticida, toxicidade relativamente baixa em mamíferos e persistência limitada no meio ambiente. Algumas de suas características físicas e químicas estão listadas na tabela abaixo:
TABELA - Características físicas e químicas da Deltametrina
Estado físico pó cristalino
Cor sem cor
Odor sem odor
Densidade (20 ºC) 0,5 g/cm3
Massa Molar 505,24 g/mol
Ponto de fusão 98 – 101 ºC
Ponto de ebulição acima de 300 ºC
Solubilidade em água (20 ºC) < 0,002 mg/L
Solubilidade em solventes orgânicos Solúvel
Solubilidade em Acetona 500 g/L
FONTE: WHO - WORLD HEALTH ORGANIZATION. Environmental Health Criteria 97 – Deltamethrin. Geneva: International Program on Chemical Safety - IPCS, 1990.
A formula estrutural da Deltametrina é apresentada na figura abaixo:

Comumente, a indústria química comercializa o inseticida Deltametrina com as seguintes especificações:
cada 1000 mL contém:
Deltametrina..............25 g
Veículo q.s.p.............1000 mL
No rótulo desse produto há também recomendações para dilução em água para sua aplicação final, de acordo com a tabela abaixo.
Quantidade de água Moscas Insetos rasteiros
1 litro 6 mL 8 mL
10 litros 60 mL 80 mL
20 litros 120 mL 160 mL
Responda a questão com base nas informações dadas sobre o tema “inseticidas” e em seus conhecimentos
de química.
I - O uso de inseticidas pode e deve ser banido das diversas atividades humanas uma vez que esses produtos têm impactos diretos no problema do aquecimento global II - Espera-se que a Deltametrina tenha grande influência também no buraco da camada de ozônio, uma vez que os átomos de bromo de sua estrutura têm as mesmas propriedades dos átomos de cloro dos CFCs (os CloroFluoro-Carbonetos), poderosos agentes impactantes dessa região atmosférica. III - Os inseticidas, principalmente quando usados de forma indevida, acumulam-se no solo, e os animais se alimentam da vegetação contaminada prosseguindo o ciclo de contaminação. Também, com as chuvas, os produtos químicos usados na composição dos pesticidas infiltram no solo, contaminando os lençóis freáticos, e acabam escorrendo para os rios continuando, assim, a contaminação.
Está(ão) correta(s):
Analisando as informações anteriores, pode-se concluir que:
DADOS QUE PODERÃO SER UTILIZADOS
NA QUESTÃO DE QUÍMICA

Constante Universal dos Gases
Perfeitos: 0,082 atm.L/mol.K
DADOS QUE PODERÃO SER UTILIZADOS
NA QUESTÃO DE QUÍMICA

Constante Universal dos Gases
Perfeitos: 0,082 atm.L/mol.K
Os extintores de incêndio à base de espuma contêm soluções aquosas de sulfato de alumínio e bicarbonato de sódio. Sobre a chama ocorre a reação cuja equação não balanceada é:
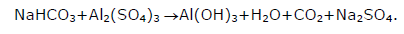
Com relação a reação anterior e seus efeitos
sobre a chama, assinale a afirmação FALSA.
DADOS QUE PODERÃO SER UTILIZADOS
NA QUESTÃO DE QUÍMICA

Constante Universal dos Gases
Perfeitos: 0,082 atm.L/mol.K
Ao entrar na sua sala de aula, um aluno de química foi surpreendido pelo teor de algumas frases sobre variados temas da química.
I - O metano, um gás estufa, é gerado por queima de biomassa, pecuária, depósito de lixo, etc.
II - Os metais alcalino-terrosos são também conhecidos como terras raras.
III - Os produtos naturais não causam danos à saúde.
IV - Misturas e substâncias diferem entre si porque as primeiras não obedecem à lei de Proust.
V - As leis de Faraday tratam apenas de aspectos qualitativos da eletrólise.
São verdadeiras as afirmações
Disponível em: <http://www.sadia.com.br/vida-saudavel> (Adaptado) Acesso em 29-maio-2011.
De acordo com o texto, é correto afirmar que:



