Questões de Vestibular
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 333 questões
Tubo A: 10 mL de solução de hidróxido de cálcio
Tubo B: 10 mL de solução diluída de hidróxido de amônio com gotas de fenolftaleína a 0,1%
Tubo C: 10 mL de água
Pela adição de porções de gelo seco aos tubos, ocorre
Uma das formas mais comuns de preparar medicamentos homeopáticos é por diluições conhecidas como centesimais hahnemannianas (CH). Nelas, o farmacêutico começa com um determinado material ou solução e o dilui a um centésimo da concentração inicial. A solução assim produzida será diluída novamente a um centésimo do que era. Desse modo, são feitas diluições sucessivas até chegar ao número prescrito na receita do médico. Assim, se um medicamento é 30 CH, isso significa que foi submetido a 30 diluições centesimais sucessivas. O medicamento homeopático acidum hydrochloricum, por exemplo, é preparado a partir de uma solução aquosa de ácido clorídrico. Tipicamente, o acidum hydrochloricum é preparado em diluições entre 5 e 30 CH.
Considerando que uma solução 1 mol/L de ácido clorídrico é diluída até certo número de CH, é correto afirmar que

O incêndio na boate Kiss, em Santa Maria (RS), ocorrido no início deste ano [2013], trouxe à tona uma série de questões sobre a segurança dos estabelecimentos e também sobre o atendimento a vítimas de grandes incêndios. Uma delas é por que foi preciso trazer dos Estados Unidos uma substância tão simples - uma vitamina B injetável - para atender os pacientes que, se gundo exames, foram intoxicados com cianeto?
gás cianídrico liberado na queima da espuma, utilizada para melhorar a acústica da casa noturna, intoxicou a maior parte das vítimas, segundo perícia. “É descaso e ignorância”, resume o toxicologista Anthony Wong, diretor do Ceatox (Centro de Assistência Toxicológica do Hospital das Clínicas da Faculdade de Medicina da Universi dade de São Paulo). Segundo ele, é inadmissível que o país não tenha a substância e que seu uso não seja difundido entre mé dicos e socorristas, como acontece em outras partes do mundo.
A hidroxocobalamina, que faz parte do complexo B, é usada em altas concentrações como antídoto para o cianeto. O gás, o mesmo que já foi usado no extermínio de judeus nos campos de concentração nazistas, é subproduto da queima de diversos componentes usados na indústria, como o plástico, o acrílico e a espuma de poliuretano. Segundo os peritos que investigam o incêndio em Santa Maria, essa última foi usada no isolamento acústico da boate.
Capaz de matar em poucos minutos, o cianeto bloqueia a cadeia respiratória das células, impedindo que o oxigênio chegue aos órgãos e tecidos. Quando usada logo após a exposição, a hi droxocobalamina salva vidas. “O efeito é tão rápido que parece até milagroso”, conta Wong. Mas isso não é algo que os médicos aprendem na escola: “São poucas as faculdades que oferecem curso de toxicologia e, nas que tem, a matéria é opcional”.
Informações adicionais:
• O gás cianídrico é o cianeto de hidrogênio (HCN) no estado gasoso.
• A fórmula estrutural da hidroxocobalamina é:

• A massa molar da hidroxocobalamina é aproximadamente igual a 1,3 × 103g/mol.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
Considerando o pH, a 25°C, da solução mencionada no texto, temos meio.
Dado: Produto iônico da água,
Kw=1,0• 10–14 , a 25°C.
Uma empresa alimentícia usou uma solução de hidróxido de sódio (soda cáustica) a 2,5% (m/v) para a limpeza de seus equipamentos.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
A solução de NaOH, descrita no texto, apresenta concentração em mol/L, aproximadamente, de.

Em um processo de limpeza, quantidades iguais de água sanitária foram adicionadas a volumes iguais de líquidos com diferentes valores de pH a 25 ºC, de acordo com a tabela.



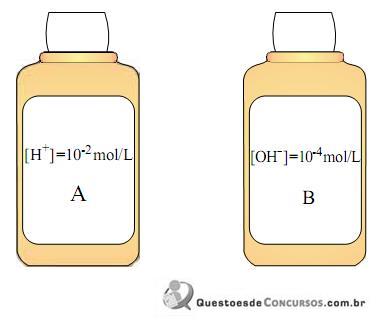
A razão entre os valores de pH da solução B e da solução A, a 25 ° C, é

Pela análise do texto, é correto afirmar que
Três amostras líquidas, identificadas pelas letras A, B e C, foram testadas por meio de indicadores ácido- base. Os resultados são apresentados no quadro a seguir:
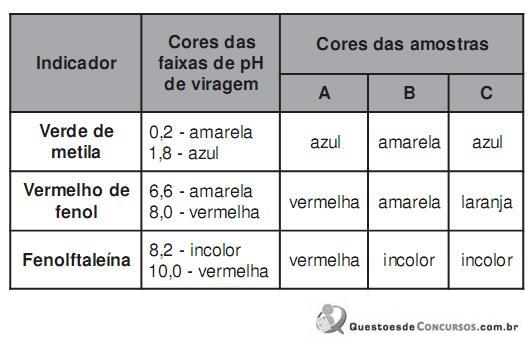
A análise dos resultados permite concluir que as amostras A, B e C são, respectivamente,
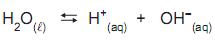
O produto iônico da água é
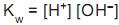 , cujo valor é 1 x
, cujo valor é 1 x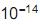 a 25 °C. Ao se adicionar 1,0 mL de NaOH 1,0 mol/L (base forte) a um copo bécher contendo 99 mL de água pura, o pH da solução será aproximadamente igual a
a 25 °C. Ao se adicionar 1,0 mL de NaOH 1,0 mol/L (base forte) a um copo bécher contendo 99 mL de água pura, o pH da solução será aproximadamente igual a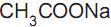 ) e ácido acético (
) e ácido acético (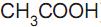 ). O pH desse tampão pode variar de 4,0 a 5,4 de acordo com a proporção dessa mistura.
). O pH desse tampão pode variar de 4,0 a 5,4 de acordo com a proporção dessa mistura. Sobre o tampão acetato, é ERRADO afirmar que:
O pH da solução final é:

Considerando essas informações, julgue os próximos itens.

Considerando essas informações, julgue os próximos itens.

Considerando essas informações, julgue os próximos itens.

