Questões de Vestibular
Sobre transformações químicas e energia em química
Foram encontradas 963 questões


Tendo como referência essas informações, julgue o item seguinte.
Quando o cálcio-41 captura um elétron, é formado o
nuclídeo 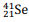 .
.
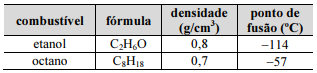
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue os item.
Considerando a combustão total, assinale a opção que representa corretamente os volumes dos combustíveis octano (à esquerda) e etanol (à direita) que devem ser queimados para que haja emissão de uma quantidade equivalente de CO2 pelos dois compostos.
Tendo como referência as informações precedentes, julgue o item que se segue.
O valor da variação de entalpia molar da reação em relação
à hematita, que reage com o monóxido de carbono,
produzindo apenas ferro metálico e dióxido de carbono, é
3 ΔHI + 2 ΔHII +ΔHIII.
Tendo como referência as informações precedentes, julgue o item que se segue.
Na reação III, há redução do ferro em um processo que
envolve a transferência de dois mols de elétrons por mol
de FeO.
A massa de iodo-131 presente na amostra decairá a 25 mg no seguinte intervalo de tempo, em dias:
LIGAÇÃO ENERGIA DE LIGAÇÃO (kJ/mol) C—H 410
Cl—Cl 240
C—Cl 330
H—Cl 430
A energia, em quilojoules, liberada na formação de 1,0 mol de diclorometano é igual a:
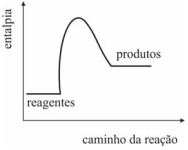
O gráfico a seguir representa corretamente a reação de combustão da madeira usada na queima da argila para a formação da cerâmica.
No contexto da pandemia de covid-19, o antimalárico cloroquina e o vermífugo nitazoxanida têm causado controvérsia quanto à sua eficácia contra o novo coronavírus. As fórmulas estruturais desses dois fármacos são mostradas a seguir.
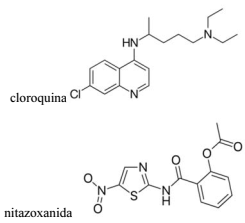
Na combustão completa da cloroquina, em que todo o carbono é convertido a CO2, para cada 100 g de cloroquina queimados, são gerados mais de 200 g de gás carbônico.
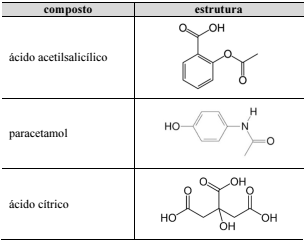
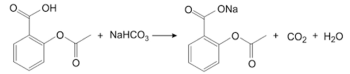
Os compostos orgânicos listados na tabela precedente são amplamente utilizados em medicamentos, entre os quais estão incluídos os efervescentes. Estes resultam da combinação de sólidos misturados e prensados para formar um comprimido contendo o fármaco ácido e um composto básico, como o NaHCO3. Quando o medicamento é colocado na água, a reação entre esses compostos libera CO2, que forma as bolhas na efervescência, como representado para o ácido acetilsalicílico na reação a seguir. Existem, também, vários compostos inorgânicos que são empregados na fabricação de medicamentos, como o FeSO4 e o KMnO4.
Tendo como referência as informações precedentes, julgue o item.
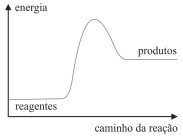
Sabendo que o KMnO4 reage com a glicerina em uma reação que libera bastante calor, é correto concluir que a variação de energia para essa reação pode ser corretamente representada pelo gráfico a seguir.
Fonte: https://ucmp.berkeley.edu/glossary/gloss3/pigments.html (acessado em 02/05/2019).
As palavras que completam as lacunas, na ordem em que se encontram no texto, são:
I. No cátodo ocorre a formação de um gás.
II. No ânodo observa-se a liberação de um gás utilizado nas estações de tratamento de água.
III. O pH da solução resultante, após a eletrólise, é menor que 7.
Está/Estão correta(s) apenas a(s) afirmativa(s)
O fenômeno climático das monções, que ocorre na Ásia, propicia a dispersão de poluentes que formam particulados, como o sulfato de amônio [(NH4)2SO4]. Esse composto é formado na atmosfera pela reação da amônia (NH3) com o dióxido de enxofre (SO2), de acordo com as equações:
SO2 (g)+ 1/2O2(g) → SO3 (g)
H2O (ℓ)+SO3(g) → H2SO4 (ℓ)
2NH3 (g) + H2SO4 (ℓ) → (NH4)2SO4 (s)
Considere os valores de entalpia-padrão de formação:
SO2 (g) 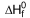 = -298 kJ/mol
= -298 kJ/mol
NH3 (g) 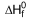 = -46 kJlmol
= -46 kJlmol
H2O (ℓ) 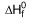 = -286 kJ/mol
= -286 kJ/mol
(NH4)2SO4 (s) 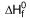 = -1179 kJ/mol
= -1179 kJ/mol
Com base nas informações apresentadas, pode-se afirmar
que a entalpia-padrão de reação de formação de 1 mol de
sulfato de amônio é
A chegada do homem à Lua, há 50 anos, possibilitou a coleta das rochas lunares, cuja análise permititu datar a idade do satélite natural da Terra com maior precisão. A técnica utilizada consistiu em determinar a proporção das quantidades do radioisótopo háfnio-182 e do isótopo estável tungstênio-182 presentes nessas rochas lunares.
O processo de decaimento radioativo do háfnio-182 apresenta uma etapa intermediária, na qual se forma o radioisótopo instável tântalo-182 que, por sua vez, decai para o tungstênio-182, de acordo com a equação:
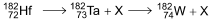
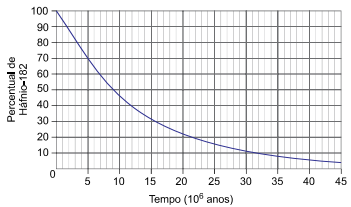
O decaimento radioativo do háfnio-182 resultando no tungstênio-182 em função do tempo ocorre de acordo com a curva apresentada no gráfico.
A emissão radioativa representada pela letra X na equação
de decaimento do háfnio-182 e a meia-vida desse radioisótopo em 106 anos são
O radioisótopo 18F é empregado em exames de tomografia por emissão de pósitrons.
O número de nêutrons presentes nesse radioisótopo é igual a:
DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

As baterias recarregáveis possuem a característica de prolongar muito sua vida útil, o que aumenta a relação custo-benefício. A bateria recarregável mais conhecida é a bateria de chumbo usada nos carros, que, por armazenar energia elétrica, é definida como bateria de armazenamento. Esse tipo de bateria consiste em seis células, cada uma gerando 2,0 V para um total de 12,0 V. A reação celular geral é dada pela seguinte equação química:
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l)
Sobre essa reação, é correto afirmar que
Um marcador radioativo (24Na) foi injetado em um ponto de um cano de água subterrâneo e, na sequência, com um detector sobre o solo, foi medida a radioatividade ao longo do percurso do cano. A figura a seguir esquematiza o local de injeção do marcador e o perfil da radioatividade detectada ao longo do cano.
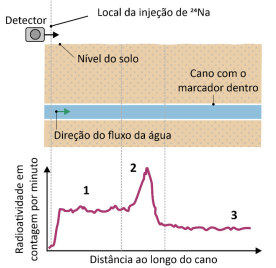
Assinale a alternativa que melhor explica o perfil da radioatividade.
Note e adote:
Tempo de meia-vida do 24Na = 15 horas.
Oxigênio (O2) e ozônio (O3) estão em constante processo de consumo e produção na estratosfera, como representado pelas equações químicas a seguir. As reações I e II ilustram etapas da produção de ozônio a partir de oxigênio, e a reação III mostra a restauração de oxigênio a partir de ozônio.
Reação ΔH (kcal/mol de O2)
I O2 → 2 O. −118
II 2 O2 + 2 O. → 2 O3 ΔHII
III 2 O3 → 3 O2 +21
