Questões de Vestibular
Sobre transformações químicas e energia em química
Foram encontradas 975 questões
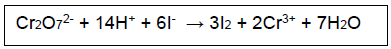
Com base na reação, é CORRETO afirmar:
Considere as semiequações e potenciais padrão de redução (ε 0 ) para o estanho e o ferro.
Fe2+(aq) + 2e- → Fe(s) ε 0 = -0,44 V
Sn2+(aq) + 2e- → Sn(s) ε 0 = -0,14 V
A corrosão da lata revestida com estanho é explicada pelo(a):
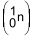 ,
forma dois nuclídeos radioativos: o bário-144, que decai emitindo partículas beta
,
forma dois nuclídeos radioativos: o bário-144, que decai emitindo partículas beta 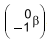 , e o nuclídeo X. Esse bombardeamento produz também três nêutrons, que colidirão com
outros núcleos de urânio, causando uma reação em cadeia.
O nuclídeo produzido pelo decaimento do bário-144 e o nuclídeo X são, respectivamente,
, e o nuclídeo X. Esse bombardeamento produz também três nêutrons, que colidirão com
outros núcleos de urânio, causando uma reação em cadeia.
O nuclídeo produzido pelo decaimento do bário-144 e o nuclídeo X são, respectivamente, 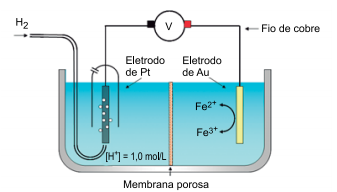
(https://mycourses.aalto.fi. Adaptado.)
Considere os eletrodos de platina e de ouro inertes e os potenciais de redução das espécies químicas presentes nas soluções:

Durante o funcionamento da célula galvânica representada na figura,
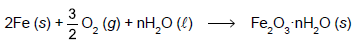
A tabela fornece os potenciais-padrão de redução (Eº) de algumas semirreações, a 25 ºC.

Com base nas informações fornecidas, pode-se afirmar que:
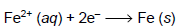
Considerando a Constante de Faraday = 96 500 C/mol, 1 hora = 3 600 s e massa molar do ferro (Fe) = 56 g/mol, a massa aproximada de ferro metálico que pode ser depositada no cátodo, nessas condições, é
CaCℓ2 (s) + H2O (ℓ) → CaCℓ2 (aq) ∆H = −82,7 kJ/mol
Nesse processo,
Uma das maneiras de se obter industrialmente o hidrogênio é pelo processo conhecido como “reforma de hidrocarbonetos a vapor”, que envolve a reação entre hidrocarboneto e água no estado gasoso, gerando como produtos gasosos CO e H2 . Considere os valores das entalpias de formação indicados na tabela. Uma das maneiras de se obter industrialmente o hidrogênio é pelo processo conhecido como “reforma de hidrocarbonetos a vapor”, que envolve a reação entre hidrocarboneto e água no estado gasoso, gerando como produtos gasosos CO e H2 .
Considere os valores das entalpias de formação indicados na tabela.
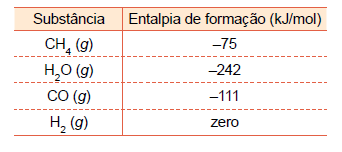
A partir das informações fornecidas, calcula-se que a produção
de cada mol de hidrogênio pela reforma a vapor do metano
C6(s) + Li+ (PC) + e- → LiC6(s) E° = 0,855 V
CoO2(s) + Li+ (PC) + e- → LiCoO2(s) E° = - 2,745 V
Baseado nos dados acima, qual a equação global e o potencial da pilha?
2 C(graf) + 3 H2(g) + 1/2 O2(g) → C2H6O(l) ΔHf = ?
Energeticamente, a entalpia padrão de formação do etanol pode ser determinada através de 3 diferentes equações de combustão. As equações estão representadas abaixo:
C(graf) + O2(g) → CO2(g) ΔHf = -394 kJ mol-1
H2(g) + 1/2 O2(g) → H2O(l) ΔHf = -286 kJ mol-1
C2H6O(l) + 3 O2(g) → 2 CO2(g) + 3 H2O(l) ΔHf = -1368 kJ mol-1
Baseado nos dados acima, qual o ΔHf do etanol, em kJ.mol-1?
Al2O3(s) + 3 C(s) → 2 Al(l) + 3 CO(g)
O processo de extração demanda um custo energético de aproximadamente 600 kJ para a obtenção de 54 g de alumínio, enquanto para a mesma massa através da reciclagem são utilizados 50 kJ de energia. Quanto é economizado de energia, para cada 108 kg do alumínio reciclado em relação ao material extraído da bauxita, em 106 kJ?
Dados: Massas atômica em g·mol-1 : Al = 27.
Dados: Massa molar do metano = 16 g.mol-1 .Calor de combustão do metano , △H° = 210 kcal.mol-1 .
Calor específico da água = 1,0 cal.g-1 .°C-1 .
De acordo com os potenciais de redução descritos abaixo, em qual(is) recipiente(s) será possível armazenar a solução de CuSO4, sem que ocorram reações químicas redox espontâneas?
Zn2+(aq) + 2e- → Zn(s) - 0,76 V Fe2+(aq) + 2e- → Fe(s) - 0,44 V Ni2+(aq) + 2e- → Ni(s) - 0,25 V Cu2+(aq) + 2e- → Cu(s) + 0,34 V Ag+ (aq) + e- → Ag(s) + 0,80 V
Dados: Mn +2 + 2e ⇾ Mnº Eº = -1,18v Zn +2 + 2e º ⇾ Znº Eº = -0,76v
I. H2(g) + O2(g) ⇾ H2O(l) ΔH = -68 Kcal/mol II. C(g) + O2(g) ⇾ CO2(g) ΔH = -94 Kcal/mol III.C2H5OH(l) + O2(g) ⇾ CO2(g) + H2O(l) ΔH = -327 Kcal/mol
A entalpia de formação do etanol será: