Questões de Vestibular
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 724 questões
Em um laboratório químico, foi encontrado um frasco de vidro contendo um líquido incolor e que apresentava o seguinte rótulo:
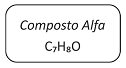
Para identificar a substância contida no frasco, foram feitos os seguintes testes:
I. Dissolveram-se alguns mililitros do líquido do frasco em água, resultando uma solução neutra. A essa solução, adicionaram-se uma gota de ácido e uma pequena quantidade de um forte oxidante. Verificou-se a formação de um composto branco insolúvel em água fria, mas solúvel em água quente. A solução desse composto em água quente apresentou pH = 4.
II. O sólido branco, obtido no teste anterior, foi dissolvido em etanol e a solução foi aquecida na presença de um catalisador. Essa reação produziu benzoato de etila, que é um éster aromático, de fórmula C9H10O2.
Com base nos resultados desses testes, concluiu-se que o
Composto Alfa é:
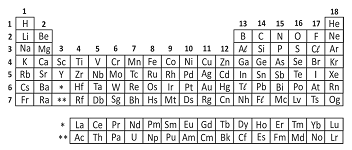
Analise a tabela periódica e as seguintes afirmações a respeito do elemento químico enxofre (S):
I. Tem massa atômica maior do que a do selênio (Se).
II. Pode formar com o hidrogênio um composto molecular de fórmula H2S.
III. A energia necessária para remover um elétron da camada mais externa do enxofre é maior do que para o sódio (Na).
IV. Pode formar com o sódio (Na) um composto iônico de fórmula Na3S.
São corretas apenas as afirmações
Na Onda do Sódio
Eu sou o Sódio,
não tenho ódio.
Quando estou com a água,
não guardo mágoa.
Explodo de emoção,
nessa reação.
Não esbanjo meu potencial,
sou muito legal.
Minha família é a um,
me dou bem com cada um.
Meu período é o terceiro,
de quem eu sou parceiro.
Existe um halogênio especial,
me ligo a todos, mas com o cloro...
Eu adoro!
Que união genial!
Me envolvo em muitas reações,
com diferentes emoções.
Base, cátion, sal...
Eu sou mesmo radical!
(Poesia de autoria de equipe participante da Gincana de Química (2011) da
Universidade Federal do Ceará. Disponível em:<http://www.quimica.ufc.br>
Acerca das informações químicas do elemento sódio que podem ser extraídas do texto “Na onda do sódio”, considere as seguintes afirmativas:
1. Da afirmativa “Minha família é a um”, pode-se concluir que sódio pertence à família I e, portanto, possui configuração eletrônica finalizada em ns1 .
2. Da afirmativa “Meu período é o terceiro”, interpreta-se que a configuração eletrônica é preenchida até o nível n = 3.
3. O cloro é o “halogênio especial”, pois é com o qual o sódio reage para formar o cloreto de sódio.
4. No sal de cloreto de sódio, a configuração eletrônica do cátion Na+ é preenchida até o nível n = 2, finalizando em 2s2 , 2p6 .
Assinale a alternativa correta.
A hemoglobina é uma proteína de elevada massa molar, responsável pelo transporte de oxigênio na corrente sanguínea. Esse transporte pode ser representado pela equação química abaixo, em que HB corresponde à hemoglobina.
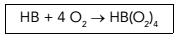
Em um experimento, constatou-se que 1 g de hemoglobina é capaz de transportar 2,24 x 10–4 L de oxigênio molecular com comportamento ideal, nas CNTP.
A massa molar, em g/mol, da hemoglobina utilizada no experimento é igual a:
BENEFÍCIOS NUTRICIONAIS DO QUIABO
O quiabo tem um baixo teor calórico. Ele fornece cerca de 30 calorias por 100 gramas de seu consumo e, principalmente, carboidratos e fibras dietéticas, além de Vitamina A, Vitamina B, Vitamina C, Vitamina E, Vitamina K e minerais como cálcio, ferro, zinco, magnésio e potássio.
Disponível em:<http://www.dicademusculacao.com.br/os-10-beneficios-do-quiabo-para-saude/>. Acesso em: 16 de julho de 2016.
Dados: Z (Mg) = 12; Z (K) = 19; Z (Ca) = 20;
Z (Fe) = 26; Z (Zn) = 30
Relacionado aos cinco elementos químicos citados no
texto acima, depreende-se que
Considerando-se essas informações relacionadas às configurações dos elementos químicos, é correto afirmar:
1s2 2s2 2p6 3s2 3p10 4s6 3d10 4p6 5s2 4d1 , o número de camadas e o número de elétrons mais energéticos para o ítrio, serão respectivamente:
Zz com número atômico 19 e
Yy com número atômico 17.
Analise cada uma das seguintes afirmativas. 1) Zz é um metal. 2) O elemento Yy está localizado no 3º período da tabela periódica. 3) O elemento Yy possui eletronegatividade menor que o elemento Zz 4) Yy é um halogênio
Estão corretas apenas
Com relação a essa descrição, três afirmações foram feitas:
1) O Li, Na e K fazem parte do grupo dos metais alcalino-terrosos, grupo que apresenta facilidade em perder 1 elétron, formando cátions monovalentes.
2) O Ni, Cu, Fe, Ag, Pb, Au e Zn são chamados de elementos metálicos por possuírem os últimos elétrons localizados em obitais d.
3) O F, Cl, Br e I fazem parte do grupo dos calcogênios, grupo que apresenta facilidade em perder 1 elétron, formando ânions monovalentes.
Está(ão) correta(s) a(s) afirmativa(s):
Os fertilizantes agrícolas são largamente utilizados para garantir nutrientes aos vegetais, na forma de íons e moléculas, indispensáveis ao crescimento, à floração e à frutificação. Dentre esses fertilizantes, o nitrato de amônio, NH4NO3 , é um dos mais empregados na correção do teor de nitrogênio do solo. Esta substância pode ser obtida através da reação entre ácido nítrico e hidróxido de amônio de acordo com a equação:
HNO3 + NH4OH --> NH4NO3 + H2O.
Esta reação é classificada como de:

Exames de imagem como ressonância magnética e tomografia computadorizada podem revelar a estrutura cerebral dos bebês que nasceram com microcefalia. Imagens do cérebro desses bebês, em geral, mostram pequenos círculos brancos bem próximos uns dos outros. Segundo neurologistas, os círculos brancos são sinais de calcificação, uma espécie de cicatriz que se forma em áreas lesadas do cérebro por algum tipo de infecção.
Sabendo-se que a ressonância magnética, que revela o interior do corpo humano mapeando a posição de moléculas de água, que existem em diferentes densidades, em variados tipos de tecido, induz um campo magnético no organismo, considerandose que o corpo humano é formado por 75% de água, é correto afirmar:

Analisando-se as informações a respeito dos eventos e consequências que ocorreram antes da origem do primeiro ser vivo,
é possível inferir: