Questões de Vestibular
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 724 questões
( ) A fervura da água a 100o C.
( ) A obtenção do oxigênio líquido a partir do ar atmosférico.
( ) O cozimento de um ovo em uma panela de pressão.
( ) O amadurecimento de uma fruta na árvore.
( ) A permanência do óleo de cozinha na fase de cima de um recipiente com água a que foi adicionado.
A sequência correta de cima para baixo é
Considere que um atleta com M kg de massa, partindo do repouso, comece a correr com aceleração constante de a m/s² ; que, enquanto corre, o atleta sofre a ação de uma força de resistência constante igual a R newtons; que toda a energia do atleta resulta da oxidação de gordura, a qual é representada pela expressão a seguir, em que E é a energia, em joules, liberada por mol de gordura.
C3H5O3(OC4H7)3 + 18,502 ? 15CO2 + 13H2O + E
Supondo-se que a eficiência do atleta seja 0, então a expressão matemática que representa a quantidade de moles N de gás carbônico produzido pelo atleta até o tempo t, em segundos, transcorrido desde o momento em que ele iniciou a corrida, é
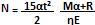
Os compostos orgânicos gerados pela oxidação branda das duplas do ácido araquidônico usando-se uma solução aquosa diluída e neutra de KMnO4 — reação de Bayer — apresentam maior solubilidade em água que o ácido araquidônico.
Presente na hemoglobina, o íon divalente do ferro tem seu raio iônico maior que o raio do átomo do ferro metálico e apresenta distribuição eletrônica 1s2 2s2 2p6 3s2 3p6 4s2 3d8 .
Questão Discursiva
Em um frasco de 1,0 L, foram colocados, a determinada temperatura, 0,880 g de N2O e 1,760 g de O2 gasosos, para reagir. Após se estabelecer o equilíbrio químico, foi formado 1,012 g de gás NO2. Considerando essas condições, calcule a concentração molar de equilíbrio do O2 e multiplique o resultado por 104 . Para marcação no Caderno de Respostas, despreze, caso exista, a parte fracionária do resultado obtido, após ter efetuado todos os cálculos solicitados.
R:385
Sabe-se que o pH de alvejantes formados por soluções aquosas de hipoclorito de sódio é superior a 7. Isso se deve ao fato de o NaClO, ao reagir com a água, produzir o ácido hipocloroso (HClO), o que aumenta a razão [OH- ]/[H3O+ ] no meio.
Caso uma solução contendo NaOH reaja com o alumínio metálico contido em um recipiente e produza o aluminato (AlO33- ), outro produto dessa reação será um gás explosivo, o hidrogênio.
O percentual em massa de nitrogênio presente em todo o explosivo usado para demolir a arquibancada do estádio Mané Garrincha foi de
Considerando-se o rendimento de 100% para a reação de combustão do nitrato de amônio, é correto afirmar que a quantidade de explosivo utilizada na referida demolição da arquibancada do estádio Mané Garrincha produziu mais de 9,0 × 105 kJ de energia.
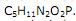 O sarin, quando em contato com a pele ou inalado, gera contrações musculares, convulsões, estado de coma e paralisia do sistema respiratório, provocando a morte lenta da pessoa.
O sarin, quando em contato com a pele ou inalado, gera contrações musculares, convulsões, estado de coma e paralisia do sistema respiratório, provocando a morte lenta da pessoa. Sobre alguns dos elementos que constituem o sarin e que formam também substâncias essenciais à manutenção da vida, assinale a afirmação FALSA.
Sobre os componentes do feijão, é correto afirmar- se que

A sequência correta, de cima para baixo, é:
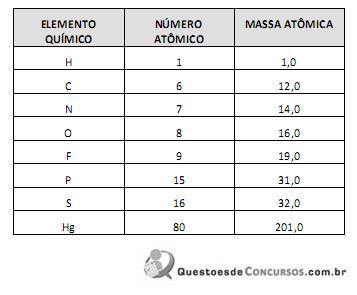
Consta que o elemento químico mercúrio recebeu esse nome por causa de sua fluidez e pelo fato de o deus romano Mercúrio ser considerado o mensageiro dos deuses, enquanto o símbolo Hg vem de hydrargyrum que significa prata líquida.
Sobre o elemento químico mercúrio e suas aplicações, assinale a alternativa FALSA.
I. K2S(aq.) + 2 HCℓO3(aq.) → 2 KCℓO3(aq.) + H2S(aq.)
II. Zn(OH) 2(s) → ZnO(s) + H2O(ℓ)
III. Cℓ2(g) + 2 HI(aq.) → I2(s) + 2 HCℓ(aq.)
A classificação da reação equacionada e o nome do composto em negrito são respectivamente:
Em relação a isso, assinale a alternativa correta.




