Questões de Vestibular de Química - Transformações Químicas
Foram encontradas 248 questões
Para descrever o comportamento dos gases ideais em função do volume V, da pressão P e da temperatura T, podem ser utilizadas as seguintes equações:
Equação de Clapeyron Equação de Boltzmann
P × V = n × R × T P × V = N × k × T
n – número de mols N – número de moléculas
R – constante dos gases k – constante de Boltzmann
De acordo com essas equações, a razão R/k é aproximadamente igual a:


Considere as seguintes afirmações:
I. A aparência macroscópica do fleróvio é desconhecida, mas, provavelmente, será a de um sólido metálico.
II. Na formação do fleróvio-288, por processo análogo ao da síntese do fleróvio-289, são liberados 3 prótons.
III. No grupo da tabela periódica ao qual pertence o fleróvio, há elementos que formam óxidos covalentes.
É correto o que se afirma apenas em



Note e adote: Volume molar nas condições de produção de biogás: 24 L/mol; energia liberada na combustão completa da gasolina: 4,5 x 104 kJ/L.
Num processo de fissão nuclear, um nêutron colidiu com o núcleo de um isótopo do urânio levando à formação de dois núcleos menores e liberação de nêutrons que produziram reações em cadeia com liberação de grande quantidade de energia. Uma das possíveis reações nucleares nesse processo é representada por:
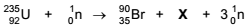
O produto X, formado na fissão nuclear indicada acima, é
um isótopo do elemento químico:
Uma estudante de Química realizou o seguinte experimento: pesou um tubo de ensaio vazio, colocou nele um pouco de NaHCO3 (s) e pesou novamente. Em seguida,adicionou ao tubo de ensaio excesso de solução aquosa de HCl, o que provocou a reação química representada por
NaHCO3(S) + HCl(aq) → NaCl(aq) + CO2(g) +H2O(l)
Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu caderno, juntamente com dados obtidos consultando um manual de Química:

A estudante desejava determinar a massa de
I. HCl que não reagiu;
II. NaCl que se formou;
III. CO2 que se formou.
Considerando as anotações feitas pela estudante, é possível
determinar a massa de
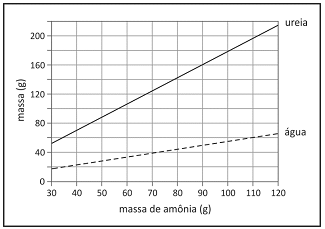
Amônia e gás carbônico podem reagir formando ureia e água. O gráfico ao lado mostra as massas de ureia e de água que são produzidas em função da massa de amônia, considerando as reações completas.
A partir dos dados do gráfico e dispondo-se de 270 g de amônia, a massa aproximada, em gramas, de gás carbônico minimamente necessária para reação completa com essa quantidade de amônia é
O suco gástrico contém um ácido, produzido pelas células da parede do estômago, que desempenha papel fundamental para a eficiência do processo digestório no ser humano.
O ânion do ácido produzido no estômago corresponde ao elemento químico pertencente ao grupo 17 e ao terceiro período da tabela de classificação periódica.
Esse ácido é denominado:
No ano de 2014, o Estado de São Paulo vive uma das maiores crises hídricas de sua história. A fim de elevar o nível de água de seus reservatórios, a Companhia de Saneamento Básico do Estado de São Paulo (Sabesp) contratou a empresa ModClima para promover a indução de chuvas artificiais. A técnica de indução adotada, chamada de bombardeamento de nuvens ou semeadura ou, ainda, nucleação artificial, consiste no lançamento em nuvens de substâncias aglutinadoras que ajudam a formar gotas de água.
(http://exame.abril.com.br. Adaptado.)
Uma das substâncias aglutinadoras que pode ser utilizada para a nucleação artificial de nuvens é o sal iodeto de prata, de fórmula AgI. Utilizando os dados fornecidos na Classificação Periódica dos Elementos, é correto afirmar que o cátion e o ânion do iodeto de prata possuem, respectivamente,
Dados de massas molares em g mol-1 : C=12; N=14 e O=16.
CH3OH(g)+ 3/2 O2(g) → CO2(g) + 2 H2O(g) combustão direta
CH3OH(g)+H2O(g) → CO2(g) + 3H2(g) H2(g)+ ½ O2(g) → H2O(g) geração e queima de hidrogênio
De acordo com essas equações, o processo de geração e queima de hidrogênio apresentaria uma variação de energia
Dados: Equação da reação: ½ N2 + O2 → NO2
Massas molares em g mol-1: N2=28 , O2=32 e NO2= 46
CaF2 (s) + H2SO4 (l) → CaSO4 (s) + 2 HF (g)
Considere que a massa molar do HF seja igual a 20 g· mol-1 e que a massa molar do CaF2 seja igual a 78 g· mol-1. Se 100 kg de ácido fluorídrico são obtidos a partir de 260 kg de fluorita impura, é correto afirmar que o teor percentual, em massa, de CaF2 nesse minério é
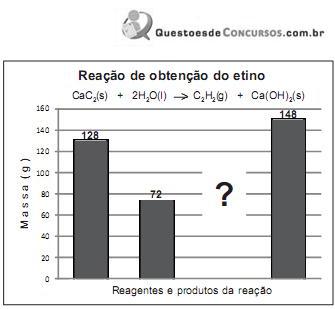
A massa, em gramas, de etino obtido nessa reação, que corresponde à coluna representada pelo ponto de interrogação, é
“No verão de 1774, Joseph Priestley, na Inglaterra, descobriu que quando se aquecia cal de mercúrio (óxido de mercúrio) ao rubro, dela desprendia um “ar” que, surpreendentemente, parecia ainda mais forte ou mais puro do que o ar comum. [...] Fascinado, Priestley investigou mais a fundo, descobrindo que camundongos podiam viver naquele ar ar por um tempo quatro vezes maior do que o ar comum. E assim, convencido de que aquele “novo” ar era benigno, ele próprio o experimentou.”
SACHS, Oliver. Tio Tungstênio. São Paulo: Companhia das Letras, 2002. P. 114.
O “novo ar” de que trata o texto é constituído essencialmente do elemento químico que