Questões de Vestibular
Sobre transformações químicas em química
Foram encontradas 1.209 questões
I. A adição de algumas gotas de fenolftaleína a amostras de cada solução fez com que apenas a amostra de B se tornasse rosada.
II. A solução rosada, obtida no ensaio I, tornou-se incolor pela adição de amostra de A.
III. Amostras de A e C produziram precipitados brancos quando misturadas, em separado, com amostras de D.
Com base nessas observações e sabendo que sulfatos de metais alcalino-terrosos são pouco solúveis em água, pode-se concluir que A, B, C e D são, respectivamente, soluções aquosas de
I. As moléculas dos componentes da gasolina e as do oxigênio estão em equilíbrio químico e, por isso, não reagem.
II. À temperatura ambiente, as moléculas dos componentes da gasolina e as do oxigênio não têm energia suficiente para iniciar a combustão.
III. As moléculas dos componentes da gasolina e as do oxigênio encontram-se tão separadas que não há colisão entre elas.
Dentre as explicações, está correto apenas o que se propõe em
I. É solúvel em água.
II. Sua solução aquosa é condutora de corrente elétrica.
III. Quando puro, o sólido não conduz corrente elétrica.
IV. Quando fundido, o líquido puro resultante não conduz corrente elétrica.
Considerando essas informações, o sólido em questão pode ser
NOTE E ADOTE As porcentagens aproximadas dos isótopos 238U e 235U existentes em uma amostra de urânio natural são, respectivamente, 99,3% e 0,7%.




Leia o texto e a tabela para responder à questão.
Barcarena, no nordeste do Pará, é uma cidade da Amazônia marcada por desastres ambientais. Há semanas, depois de fortes chuvas, houve um vazamento de rejeitos em uma das empresas do polo industrial, o que contaminou rios da região. No município de Barcarena já houve outros registros de crimes ambientais de contaminação.
Em 2004, a Universidade Federal do Pará (UFPA) realizou uma pesquisa que concluiu que a água consumida pela população, em 26 localidades, estava contaminada por íons de metais pesados tais como Pb2+, Cd2+ e Hg2+, descartados pelas indústrias. Amostras de água de Vila Nova, Burajuba e do Distrito Industrial apresentaram concentração de chumbo 12 vezes maior que o máximo permitido por uma resolução de 2011 do Ministério da Saúde.

Os íons cádmio,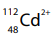 , presentes na água contaminada apresentam
, presentes na água contaminada apresentam
Leia o texto e a tabela para responder à questão.
Barcarena, no nordeste do Pará, é uma cidade da Amazônia marcada por desastres ambientais. Há semanas, depois de fortes chuvas, houve um vazamento de rejeitos em uma das empresas do polo industrial, o que contaminou rios da região. No município de Barcarena já houve outros registros de crimes ambientais de contaminação.
Em 2004, a Universidade Federal do Pará (UFPA) realizou uma pesquisa que concluiu que a água consumida pela população, em 26 localidades, estava contaminada por íons de metais pesados tais como Pb2+, Cd2+ e Hg2+, descartados pelas indústrias. Amostras de água de Vila Nova, Burajuba e do Distrito Industrial apresentaram concentração de chumbo 12 vezes maior que o máximo permitido por uma resolução de 2011 do Ministério da Saúde.

Certo isótopo desse elemento possui 86 prótons, 86 elétrons e número de massa 222, logo o número de nêutrons desse isótopo é

O besouro-bombardeiro consegue afastar seus predadores, lançando sobre eles um jato quente e repelente de quinona, substância produzida em seu abdômen, através da reação química entre hidroquinina e peróxido de hidrogênio. O fenômeno pode ser representado pela equação:
C6 H6 O2(aq) + H2O2(aq) → C6 H4O2(aq) + 2H2 O ∆H = –204 kJ/mol
Hidroquinona Quinona
Em 1911, o renomado cientista Ernest Rutherford e seus colaboradores Marsden e Geiger realizaram uma série de experimentos com materiais que emitiam partículas alfa (α). Os resultados obtidos levaram esse pesquisador a sugerir um novo modelo para o átomo. A figura a seguir representa, esquematicamente, um desses experimentos.
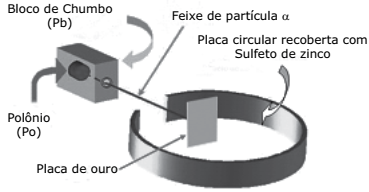
Sobre os motivos que levaram Rutherford a realizar esses experimentos e as conclusões que ele obteve, foram feitas as afirmações:
I. Rutherford concordava com o modelo atômico sugerido por Thomson e, por isso, esperava que todas as partículas alfa(α) atravessassem a placa de ouro com facilidade.
II. O modelo atômico proposto por Rutherford sugere que o átomo é eletricamente neutro, apesar de ser constituído por partículas positivas e negativas.
III. Rutherford desenvolveu esses experimentos porque estudava o comportamento dos prótons e elétrons que constituem a placa de ouro.
Assinale a alternativa em que foram apontadas as afirmativas CORRETAS.
Ao ingerirmos fígado de boi, couve ou gemas de ovos, temos uma dieta rica em ferro.
Sobre o ferro, é CORRETO afirmar que
I. O raio do Li+ é menor do que o raio do Li, pois o primeiro apresenta um elétron a menos. II. Os íons Na+, F– e Mg²+ têm a mesma configuração eletrônica, porém, seus raios são diferentes porque eles têm diferentes números atômicos. III. O raio dos ânions é maior do que o raio dos átomos originais devido ao aumento do número de elétrons na camada de valência dos ânions e aos efeitos de repulsão que os elétrons exercem uns sobre os outros. IV. O raio iônico diminui de cima para baixo em um mesmo grupo na tabela periódica devido ao aumento sucessivo do número de camadas eletrônicas.
Estão corretas as afirmações em
O elemento químico arsênio (As) é um metaloide encontrado naturalmente no meio ambiente, sendo as erupções vulcânicas uma de suas principais fontes. Dentre os diversos minerais que contêm arsênio, a arsenopirita (FeAsS) é o mais comum. Esse elemento também pode ser encontrado em alimentos como peixes e crustáceos, e também na cerveja e no vinho branco. Porém, a maior contaminação no homem ocorre por ingestão de água contaminada. Compostos de arsênio foram amplamente utilizados na agricultura como pesticidas. No ramo da medicina veterinária é utilizado como antiparasitário e como aditivo em ração animal. Seu uso também está presente nas indústrias de eletrônicos, como clarificador de vidros e na conservação da madeira.
Analise as afirmativas em relação às informações, no quadro acima.
I. O elemento arsênio pode apresentar estados de oxidação +3 e -3.
II. O raio atômico do elemento arsênio é maior do que o elemento alumínio.
III. O elemento arsênio pode realizar três ou cinco ligações covalentes.
Assinale a alternativa correta.
Analise o Quadro que apresenta o número de prótons, elétrons e nêutrons de quatro espécies químicas.
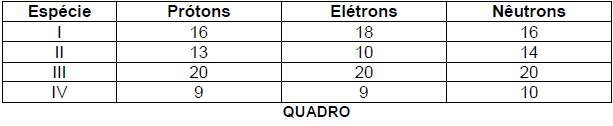
Considerando os dados apresentados no Quadro e de acordo com a Tabela Periódica, assinale
a alternativa incorreta.
O nitrato de amônio NH4NO3(s) é utilizado na agricultura como fertilizante para promover o crescimento e a frutificação de plantas, entretanto é um explosivo potente que, ao se decompor, libera, rapidamente, um volume muito grande de gases de acordo com a equação termoquímica.
A partir dessas informações, dessa equação termoquímica e admitindo-se que os gases desprendidos na explosão são ideais, é correto afirmar: