Questões de Vestibular
Sobre transformações químicas em química
Foram encontradas 1.180 questões
Assinale a alternativa que melhor representa a variação da pressão (p) exercida pelo gás, em função da variação do volume (V) do recipiente.
 têm-se mostrado
promissoras devido ao potencial terapêutico comprovado
em cobaias. Sobre um átomo eletricamente neutro do elemento químico ouro, verifica-se que no núcleo há
têm-se mostrado
promissoras devido ao potencial terapêutico comprovado
em cobaias. Sobre um átomo eletricamente neutro do elemento químico ouro, verifica-se que no núcleo há Assinale a alternativa correta.
Nas equações abaixo, representadas na forma simplificada, há espécies ionizadas (não mostradas nessa forma) que participam das reações enquanto outras não:
I. KCℓ(aq) + AgNo3(aq) -> AgCℓ(s) + KNO3(aq)
I. FeCℓ3(aq) + SnCℓ2(aq) -> FeCℓ2(aq) + SnCℓ4(aq)
III. Ba(OH)2(aq) + H2SO4(aq) -> BaSo4(s) + H20(ℓ)
Nessas equações, os símbolos (aq), (s) e (ℓ) representam, respectivamente, “espécies químicas dissolvidas em água”, “espécies químicas no estado sólido” e “espécies químicas no estado líquido”.
É correto afirmar que, na reação indicada, são íons espectadores
Considerando as informações do texto, têm-se as seguintes afirmativas: I - O suor é uma mistura heterogênea do tipo suspensão. II - A densidade do suor é a razão entre seu volume e sua massa e representa uma propriedade química. III - O suor sobre a pele desaparece quando o atleta pára de jogar, porque retira energia térmica do corpo para transformar seu estado físico de líquido para gasoso. IV - Os íons sódio e potássio, contidos no suor, são metais alcalinos e pertencem ao primeiro grupo da tabela periódica. V - Os íons sódio, potássio e magnésio, liberados durante a transpiração, possuem cargas iguais a +1, +1 e +2, respectivamente.
Assinale a alternativa que reúne somente afirmativas corretas.
DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

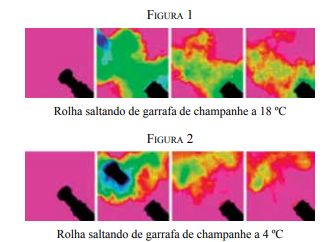
(Pesquisa Fapesp, janeiro de 2013. Adaptado.)
As figuras permitem observar diferenças no espocar de um champanhe: a 18 ºC, logo no início, observa-se que o volume de CO2 disperso na nuvem gasosa – não detectável na faixa da luz visível, mas sim do infravermelho – é muito maior do que quando a temperatura é de 4 ºC. Numa festa de fim de ano, os estudantes utilizaram os dados desse experimento para demonstrar a lei que diz:

A primeira lâmpada comercial, desenvolvida por Thomas Edison, consistia em uma haste de carbono, que era aquecida pela passagem de uma corrente elétrica a ponto de emitir luz visível. Era, portanto, uma lâmpada incandescente, que transforma energia elétrica em energia luminosa e energia térmica. Posteriormente, passou-se a utilizar, no lugar da haste, filamentos de tungstênio, cuja durabilidade é maior. Hoje, esse tipo de lâmpada tem sido substituído pelas lâmpadas fluorescentes e de LED.
As lâmpadas fluorescentes são construídas com tubos de vidro transparente revestidos internamente e contêm dois eletrodos (um em cada ponta) e uma mistura de gases em seu interior — vapor de mercúrio e argônio, por exemplo. Quando a lâmpada fluorescente é ligada, os eletrodos geram corrente elétrica, que, ao passar através da mistura gasosa, excita seus componentes, os quais, então, emitem radiação ultravioleta. O material que reveste o tubo tem a propriedade de converter a radiação ultravioleta em luz visível, que é emitida para o ambiente.
A lâmpada de LED é mais econômica que a incandescente, pois dissipa menos energia em forma de calor. Em geral, essas lâmpadas têm eficiência de 15 lumens por watt. Um lúmen (unidade padrão do Sistema Internacional) é o fluxo luminoso emitido por uma fonte puntiforme com intensidade uniforme de 1 candela e contido em um cone de ângulo sólido de um esferorradiano. A tabela a seguir apresenta características específicas das lâmpadas incandescentes, fluorescentes e de LED.

A partir do texto acima e considerando que 6,63 × 10-34 J-s seja o valor da constante de Planck, que 3 × 108 m/s seja a velocidade da luz e que a temperatura em graus Kelvin seja exatamente igual à temperatura em graus Celsius acrescida de 273, julgue o item.
Considere que o volume disponível para o gás dentro do tubo
de uma lâmpada fluorescente seja independente da temperatura
e que o gás apresente comportamento ideal. Nessas condições,
se, após o acendimento da lâmpada, a temperatura do gás
aumentar de 25 ºC para 2.707 ºC, a pressão do gás será
aumentada em dez vezes.
A primeira lâmpada comercial, desenvolvida por Thomas Edison, consistia em uma haste de carbono, que era aquecida pela passagem de uma corrente elétrica a ponto de emitir luz visível. Era, portanto, uma lâmpada incandescente, que transforma energia elétrica em energia luminosa e energia térmica. Posteriormente, passou-se a utilizar, no lugar da haste, filamentos de tungstênio, cuja durabilidade é maior. Hoje, esse tipo de lâmpada tem sido substituído pelas lâmpadas fluorescentes e de LED.
As lâmpadas fluorescentes são construídas com tubos de vidro transparente revestidos internamente e contêm dois eletrodos (um em cada ponta) e uma mistura de gases em seu interior — vapor de mercúrio e argônio, por exemplo. Quando a lâmpada fluorescente é ligada, os eletrodos geram corrente elétrica, que, ao passar através da mistura gasosa, excita seus componentes, os quais, então, emitem radiação ultravioleta. O material que reveste o tubo tem a propriedade de converter a radiação ultravioleta em luz visível, que é emitida para o ambiente.
A lâmpada de LED é mais econômica que a incandescente, pois dissipa menos energia em forma de calor. Em geral, essas lâmpadas têm eficiência de 15 lumens por watt. Um lúmen (unidade padrão do Sistema Internacional) é o fluxo luminoso emitido por uma fonte puntiforme com intensidade uniforme de 1 candela e contido em um cone de ângulo sólido de um esferorradiano. A tabela a seguir apresenta características específicas das lâmpadas incandescentes, fluorescentes e de LED.

A partir do texto acima e considerando que 6,63 × 10-34 J-s seja o valor da constante de Planck, que 3 × 108 m/s seja a velocidade da luz e que a temperatura em graus Kelvin seja exatamente igual à temperatura em graus Celsius acrescida de 273, julgue o item.
O tungstênio apresenta, em seu estado fundamental de energia, elétrons que ocupam orbitais ƒ.
A primeira lâmpada comercial, desenvolvida por Thomas Edison, consistia em uma haste de carbono, que era aquecida pela passagem de uma corrente elétrica a ponto de emitir luz visível. Era, portanto, uma lâmpada incandescente, que transforma energia elétrica em energia luminosa e energia térmica. Posteriormente, passou-se a utilizar, no lugar da haste, filamentos de tungstênio, cuja durabilidade é maior. Hoje, esse tipo de lâmpada tem sido substituído pelas lâmpadas fluorescentes e de LED.
As lâmpadas fluorescentes são construídas com tubos de vidro transparente revestidos internamente e contêm dois eletrodos (um em cada ponta) e uma mistura de gases em seu interior — vapor de mercúrio e argônio, por exemplo. Quando a lâmpada fluorescente é ligada, os eletrodos geram corrente elétrica, que, ao passar através da mistura gasosa, excita seus componentes, os quais, então, emitem radiação ultravioleta. O material que reveste o tubo tem a propriedade de converter a radiação ultravioleta em luz visível, que é emitida para o ambiente.
A lâmpada de LED é mais econômica que a incandescente, pois dissipa menos energia em forma de calor. Em geral, essas lâmpadas têm eficiência de 15 lumens por watt. Um lúmen (unidade padrão do Sistema Internacional) é o fluxo luminoso emitido por uma fonte puntiforme com intensidade uniforme de 1 candela e contido em um cone de ângulo sólido de um esferorradiano. A tabela a seguir apresenta características específicas das lâmpadas incandescentes, fluorescentes e de LED.

A partir do texto acima e considerando que 6,63 × 10-34 J-s seja o valor da constante de Planck, que 3 × 108 m/s seja a velocidade da luz e que a temperatura em graus Kelvin seja exatamente igual à temperatura em graus Celsius acrescida de 273, julgue o item.
O tungstênio tem maior raio atômico e menor energia de
ionização que o carbono.
Ao longo dos anos, diversas descobertas levaram ao crescente aperfeiçoamento dos modelos atômicos. Em relação a esse assunto, faça o que se pede no item, que é do tipo C.
.
Assinale a opção correspondente à figura que melhor ilustra o modelo atômico de Thomson, que sucedeu o modelo de Dalton.

Ao longo dos anos, diversas descobertas levaram ao crescente aperfeiçoamento dos modelos atômicos. Em relação a esse assunto, julgue o item.
Apesar de inúmeras falhas, o modelo atômico de Dalton foi
capaz de explicar o princípio da conservação de massa, de
Lavoisier.
.
A base de uma escultura é formada por uma placa de latão, uma liga metálica de zinco (Zn) e cobre (Cu). Para minimizar os problemas relacionados à corrosão provocada pela chuva ácida, a placa foi recoberta com uma fina camada de prata (Ag). O recobrimento foi realizado a partir da eletrólise de uma solução aquosa de AgCl, fixando-se a placa de latão no anodo da célula eletrolítica. A voltagem foi ajustada de forma a se obter corrente constante de 10,0 A.

Átomos de Cu-63 e de Zn-65 têm a mesma quantidade de nêutrons.
De acordo com a teoria das colisões, para ocorrer uma reação química em fase gasosa deve haver colisões entre as moléculas reagentes, com energia suficiente e com orientação adequada.
Considere as seguintes afirmações a respeito da teoria das colisões.
I - O aumento da temperatura aumenta a frequência de colisões e a fração de moléculas com energia suficiente, mas não altera a orientação das moléculas.
II - O aumento da concentração aumenta a frequência das colisões.
III- Uma energia de ativação elevada representa uma grande fração de moléculas com energia suficiente para a reação ocorrer.
Quais estão corretas?