Questões ENEM de Química
Foram encontradas 471 questões
Disponível em: www.anvisa.gov.br. Acesso em: 1 ago. 2012 (adaptado).
Considerando-se o valor de 6 X 1023 mol-1 para a constante de Avogadro e a massa molar do cálcio igual a 40 g/mol, qual a quantidade mínima diária de átomos de cálcio a ser ingerida para que uma pessoa supra suas necessidades?
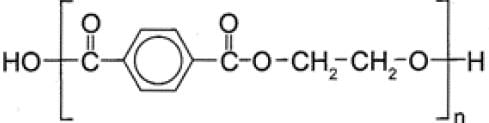
Disponível em: wwwabrpet.org.br. Acesso em: 27 fev. 2012 (adaptado).
Com base nas informações do texto, uma alternativa para a obtenção de etilenoglicol a partir do PET é a
CORRÊA. A. G.; ZUIN, V. G. (Orgs). Química Verde: fundamentos e aplicações. São Carlos: EdUFSCar. 2009.
À luz da Química Verde, métodos devem ser desenvolvidos para eliminar ou reduzir a poluição do ar causada especialmente pelas
Revista Promoção da Saúde da Secretaria de Políticas de Saúde.
Ano 1 ,n °4 , dez. 2000 (adaptado)
Quais procedimentos técnicos tornam o aterro sanitário mais vantajoso que o lixão, em relação às problemáticas abordadas no texto?
espécies invasoras que não teriam naturalmente adaptação para este ambiente, no entanto elas estão dominando as margens da rodovia, equivocadamente chamada de “estrada ecológica” . Possivelmente a entrada de espécies de plantas exóticas neste ambiente foi provocada pelo uso, neste empreendimento, de um tipo de asfalto (cimento-solo), que possui uma mistura rica em cálcio, que causou modificações químicas aos
solos adjacentes à rodovia MG-010.
Scientific American. Brasil. Ano 7, n° 79, 2008 (adaptado).
Essa afirmação baseia-se no uso de cimento-solo, mistura rica em cálcio que
A reação descrita no texto mostra o processo de extração dos metais por meio da reação com moléculas orgânicas, X e Y . Considerando-se as estruturas de X e Y e o processo de separação descrito, pode-se afirmar que
Tipo A, na qual o enxofre não se incorpora na molécula; Tipo B, na qual o oxigênio, que faz dupla ligação com fósforo, é substituído pelo enxofre; e Tipo C, no qual dois oxigênios são substituídos por enxofre.
BAIRD, C. Química Ambiental. Bookmam, 2005.
Um exemplo de pesticida organofosforado Tipo B, que apresenta grupo etoxi em sua fórmula estrutural, está representado em:
Revista Aquecimento Global. Ano 2, n° 8. Publicação do Instituto Brasileiro de Cultura Ltda.
Um dos principais constituintes da gasolina é o octano (C 8H18). Por meio da combustão do octano é possível a liberação de energia, permitindo que o carro entre em movimento. A equação que representa a reação química desse processo demonstra que
O monofluoracetato de sódio pode ser obtido pela
Suponha que, em um processo de recuperação de cobre puro, tenha-se eletrolisado uma solução de sulfato de cobre (II) (CuS04) durante 3 h, empregando-se uma corrente elétrica de intensidade igual a 10 A. A massa de cobre puro recuperada é de aproximadamente
Dados: Constante de Faraday F= molar 96 500 C/mol; Massa molar em g/mol: Cu= 63,5.
PbS04 Na2CO3→PbCo3 + Na2SO4
Dados: Massas Molares em g/mol Pb = 207; S = 32; Na = 23; 0 = 1 6 ;C = 12
ARAÚJO, R. V. V.; TINDADE, R. B. E.; SOARES, P. S. M. Reciclagem de chumbo de bateria auto motiva: estudo de caso.
Disponível em: http://www.iqsc.usp.br. Acesso em: 17 abr. 2010 (adaptado)
Segundo as condições do processo apresentado para a obtenção de carbonato de chumbo (II) por meio da lixiviação por carbonato de sódio e considerando uma massa de pasta residual de uma bateria de 6 kg, qual quantidade aproximada, em quilogramas, de PbC03 é obtida?
o limite entre a vida aeróbica e anaeróbica. Nesse contexto, um parâmetro chamado Demanda Bioquímica de Oxigênio (DBO) foi definido para medir a quantidade de matéria orgânica presente em um sistema hídrico. A DBO corresponde à massa de 0 2 em miligramas necessária para realizar a oxidação total do carbono orgânico em um litro de água.
BAIRD, C. Quimica Ambiental. Ed. Bookmam, 2005 (adaptado).
Dados: Massas molares em g/mol: C = 12;H = 1 ;0 = 1 6 .
Suponha que 10 mg de açúcar (fórmula mínima CH2O e massa molar igual a 30 g/mol) são dissolvidos em um litro de água; em quanto a DBO será aumentada?
Considere que, em pequenos volumes, o custo de produção de ambos os alcoóis seja o mesmo. Dessa forma, do ponto de vista econômico, é mais vantajoso utilizar
BROWN, T. Química a Ciência Central. São Paulo: Pearson Prentice Hall, 2005.
Atualmente, uma das formas de se utilizar a energia solar tem sido armazená-la por meio de processos químicos endotérmicos que mais tarde podem ser revertidos para liberar calor. Considerando a reação: CH4(g) + H2O(v) + calor ⇌ CO(g) + 3 H2( g ) e analisando-a como potencial mecanismo para o aproveitamento posterior da energia solar, conclui-se que se trata de uma estratégia
bichos pertençam a um grupo pouco conhecido, o dos loricíferos, que mal chegam a 1,0 mm. Apesar do tamanho, possuem cabeça, boca, sistema digestivo e uma carapaça. A adaptação dos bichos à vida no sufoco é tão profunda que suas células dispensaram as chamadas mitocôndrias.
LOPES, R. J. Italianos descobrem animal que vive em água sem oxigênio.
Disponível em: http://www1.folha.uol.com.br. Acesso em:10 abr. 2010 (adaptado).
Que substâncias poderiam ter a mesma função do 02 na respiração celular realizada pelos loricíferos?
As matérias-primas que atuam na efervescência são, em geral, o ácido tartárico ou o ácido cítrico que reagem com um sal de caráter básico, como o bicarbonato de sódio (NaHC03), quando em contato com a água. A partir do contato da mistura efervescente com a água, ocorre uma série de reações químicas simultâneas: liberação de íons, formação de ácido e liberação do gás carbônico — gerando a efervescência.
As equações a seguir representam as etapas da reação da mistura efervescente na água, em que foram omitidos os estados de agregação dos reagentes, e H3A representa o ácido cítrico.
I - NaHCO3 → Na+ + HCO3
II - H2CO3 ⇌ H2O + CO2
III - HCO3 + H+ ⇌ H2CO3
IV - H3A ⇌ 3H+ + A
A ionização, a dissociação iônica, a formação do ácido e a liberação do gás ocorrem, respectivamente, nas seguintes etapas:
Com base no texto e na figura, a produção de energia elétrica por meio da célula a combustível hidrogênio/ oxigênio diferencia-se dos processos convencionais porque
Em áreas urbanas, devido à atuação conjunta do efeito estufa e das “ilhas de calor” , espera-se que o consumo de energia elétrica
• Colocou uma caneca metálica contendo água no fogareiro do fogão de sua casa.
• Quando a água começou a ferver, encostou cuidadosamente a extremidade mais estreita de uma seringa de injeção, desprovida de agulha, na superfície do líquido e, erguendo o êmbolo da seringa, aspirou certa quantidade de água para seu interior, tapando-a em seguida.
• Verificando após alguns instantes que a água da seringa havia parado de ferver, ele ergueu o êmbolo da seringa, constatando, intrigado, que a água voltou a ferver após um pequeno deslocamento do êmbolo.
Considerando o procedimento anterior, a água volta a ferver porque esse deslocamento




