Questões ENEM de Química
Foram encontradas 471 questões

Das espécies apresentadas, a adequada para essa recuperação é
SANTOS, W. L. P.; MÓL, G. S. (Coords.). Química e sociedade. São Paulo: Nova Geração, 2005 (adaptado).
A substância capaz de formar as estruturas mencionadas é
Os impactos da má qualidade do óleo diesel brasileiro. Disponível em: www.cnt.org.br.Acesso em: 20 dez. 2012 (adaptado).
A substituição do diesel usado nos anos 1980 por aquele difundido em 2012 permitiu uma redução percentual de emissão de SO3 de
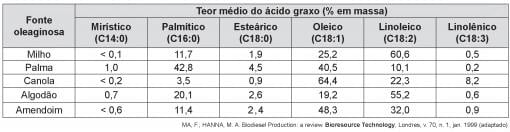
Qual das fontes oleaginosas apresentadas produziria um biodiesel de maior resistência à oxidação?
COELHO, F. A. S. Fármacos e quiralidade. Cadernos Temáticos de Química Nova na Escola, São Paulo, n. 3, maio 2001 (adaptado).
Essa malformação congênita ocorre porque esses enantiômeros
SPIRO, T. G.; STIGLIANI, W. M. Química ambiental. São Paulo: Pearson, 2009 (adaptado).
Visando eliminar da água o clorofórmio e outras moléculas orgânicas, o tratamento adequado é a
Essa fonte de energia subutilizada, citada no texto, é o
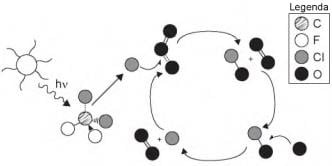
Quimicamente, a destruição do ozônio na atmosfera por gases CFCs é decorrência da
O método de separação comumente usado para retirar o sulfato de alumínio com as impurezas aderidas é a
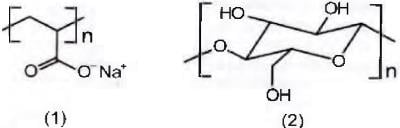
CURI. D Química Nova na Escola, São Paulo, n. 23, maio 2006 (adaptado).
A maior eficiência dessas fraldas descartáveis, em relação às de pano, deve-se às
LEE. J. D Química Inorgânica não tão concisa. São Paulo: Edgard Blucher. 1999 (adaptado).
Considerando que um forno foi alimentado com 2,5 toneladas de ferro-gusa, a massa de gás carbônico formada, em quilogramas, na produção de aço doce, é mais próxima de
SACKS. O. Tio Tungstênío; memórias de uma infância química. São Paulo: Cia, das Letras, 2002.
O fragmento do romance de Oliver Sacks relata a separação dos elementos que compõem a água. O princípio do método apresentado é utilizado industrialmente na
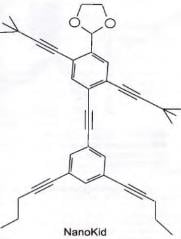
CHANTEAU, S. H.; TOUR, J. M. The Journal of Organic Chemistry. v. 68, n. 23. 2003 (adaptado).
Em que parte do corpo do NanoKid existe carbono quaternário?
Cl2 (g) + 2 H2O ( l ) ⥨ HCIO (aq) + H3O+ (aq) + Cl (aq)
HCIO (aq) + H2O (I) ⥨ H3O+ (aq) + CIO- (aq) pKa = - log Ka = 7,53
A ação desinfetante é controlada pelo ácido hipocloroso, que possui um potencial de desinfecção cerca de 80 vezes superior ao ânion hipoclorito. O pH do meio é importante, porque influencia na extensão com que o ácido hipocloroso se ioniza.
Para que a desinfecção seja mais efetiva, o pH da água a ser tratada deve estar mais próximo de
Para que se consiga atrair um maior número de abelhas para uma determinada região, a molécula que deve estar presente em alta concentração no produto a ser utilizado é:
Em um medicamento, a varfarina é administrada por via intravenosa na forma de solução aquosa, com concentração de 3,0 mg/mL. Um indivíduo adulto, com volume sanguíneo total de 5,0 L, será submetido a um tratamento com solução injetável desse medicamento.
Qual é o máximo volume da solução do medicamento que pode ser administrado a esse indivíduo, pela via intravenosa, de maneira que não ocorram hemorragias causadas pelo anticoagulante?
4 FeS2 (s) + 15O2 (g) + 2 H2O (I) ➙ 2 Fe2(SO4)3 (aq) + 2 H2 SO4 (aq)
FIGUEIREDO, B. R. Minérios e ambiente. Campinas: Unicamp, 2000.
Para corrigir os problemas ambientais causados por essa drenagem, a substância mais recomendada a ser adicionada ao meio é o
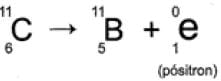
A partir da injeção de glicose marcada com esse nuclídeo, o tempo de aquisição de uma imagem de tomografia é de cinco meias-vidas.
Considerando que o medicamento contém 1,00 g do carbono-1 1 , a massa, em miligramas, do nuclídeo restante, após a aquisição da imagem, é mais próxima de
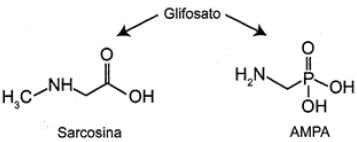
AMARANTE JR „ O. P. et al. Quimíca Nova. São Pauto, v. 25, n, 3, 2002 (adaptado).
A partir do texto e dos produtos de degradação apresentados, a estrutura química que representa o glifosato é:
ROSA, A, H.: COELHO, J. C. R. Cadernos Temáticos de Química Nova na Escola. São Paulo, n. 5, nov. 2003 (adaptado).
De que maneira as práticas agrícolas podem ajudar a minimizar o agravamento do efeito estufa?