Questões do Enem Sobre química
Foram encontradas 487 questões
Considera-se combustível aquele material que, quando em combustão, consegue gerar energia. No caso dos biocombustíveis, suas principais vantagens de uso são a de serem oriundos de fontes renováveis e a de serem menos poluentes que os derivados de combustíveis fósseis. Por isso, no Brasil, tem-se estimulado o plantio e a industrialização de sementes oleaginosas para produção de biocombustíveis.
No quadro, estão os valores referentes à energia produzida pela combustão de alguns biocombustíveis:
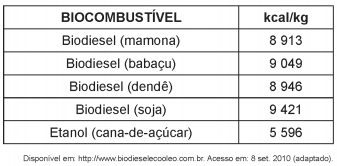
Entre os diversos tipos de biocombustíveis apresentados
no quadro, aquele que apresenta melhor rendimento
energético em massa é proveniente
Os materiais radioativos emitem diferentes tipos de radiação. A radiação gama, por exemplo, por sua alta energia e penetração, consegue remover elétrons dos átomos dos tecidos internos e romper ligações químicas por ionização, podendo causar mutação no DNA. Já as partículas beta têm o mesmo efeito ionizante, mas atuam sobre as células da pele.
RODRIGUES JR., A. A. O que é radiação? E contaminação radioativa? Vamos esclarecer. Física na Escola. V. 8, n° 2, 2007. São Paulo: Sociedade Brasileira de Física (adaptado).
Segundo o texto, um indivíduo irradiado por uma fonte radioativa é exposto ao risco de
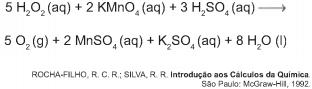
De acordo com a estequiometria da reação descrita, a quantidade de permanganato de potássio necessária para reagir completamente com 20,0 mL de uma solução 0,1 mol/L de peróxido de hidrogênio é igual a

Considerando que uma pessoa consuma refrigerantes diariamente, poderá ocorrer um processo de desmineralização dentária, devido ao aumento da concentração de
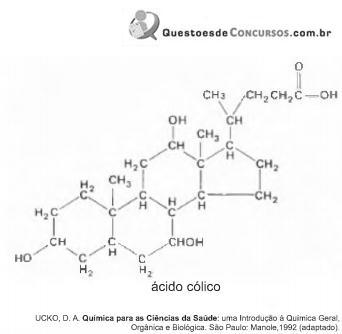
A combinação entre o ácido cólico e a glicina ou taurina origina a função amida, formada pela reação entre o grupo amina desses aminoácidos e o grupo

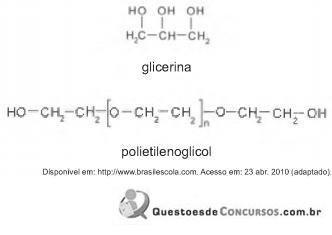
A retenção de água na superfície da pele promovida pelos hidratantes é consequência da interação dos grupos hidroxila dos agentes umectantes com a umidade contida no ambiente por meio de
Um lote contendo 5 amostras de solda estanho- chumbo foi analisado por um técnico, por meio da determinação de sua composição percentual em massa, cujos resultados estão mostrados no quadro a seguir.
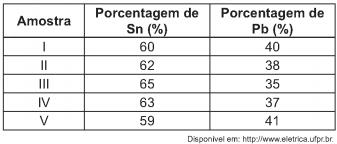
Com base no texto e na análise realizada pelo técnico, as amostras que atendem às normas internacionais são

Neste contexto, qual dos combustíveis, quando queimado completamente, libera mais dióxido de carbono no ambiente pela mesma quantidade de energia produzida?
Veja. Especial Tecnologia. São Paulo: Abril, set. 2008 (adaptado).
A partir dos resultados obtidos pelos pesquisadores em relação ao uso de nanocristais de dióxido de titânio na produção de tecidos e considerando uma possível utilização dessa substância no combate às infecções hospitalares, pode-se associar que os nanocristais de dióxido de titânio
Tabela 1: Solubilidade em água de alguns compostos presentes na água do mar a 25 oC
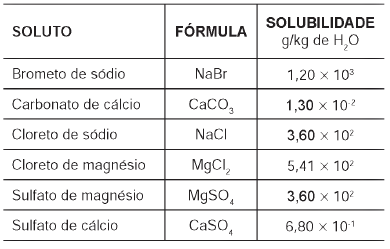
Pitombo, L.R.M.; Marcondes, M.E.R.; GEPEC. Grupo de pesquisa em Educação em Química. Química e Sobrevivência: Hidrosfera Fonte de Materiais. São Paulo: EDUSP, 2005 (adaptado).
Suponha que uma indústria objetiva separar determinados sais de uma amostra de água do mar a 25 °C, por meio da precipitação fracionada. Se essa amostra contiver somente os sais destacados na tabela, a seguinte ordem de precipitação será verificada:
Disponível em: http://www.odontologia.com.br. Acesso em: 27 jul. 2010 (adaptado).
A reação de dissolução da hidroxiapatita é:
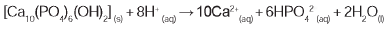
Dados: Massas molares em g/mol — [Ca10(PO4)6(OH2)] = 1004; HPO42 = 96; Ca = 40.
Supondo-se que o esmalte dentário seja constituído exclusivamente por hidroxiapatita, o ataque ácido que dissolve completamente 1 mg desse material ocasiona a formação de, aproximadamente,
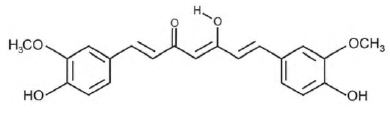
ANTUNES, M. G. L. Neurotoxicidade induzida pelo quimioterápico cisplatina: possíveis efeitos citoprotetores dos antioxidantes da dieta curcumina e coenzima Q10. Pesquisa FAPESP. São Paulo, n. 168, fev. 2010 (adaptado).
Na estrutura da curcumina, identificam-se grupos característicos das funções
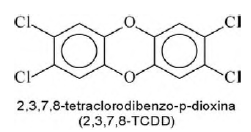
A molécula do 2,3,7,8 - TCDD é popularmente conhecida pelo nome ‘dioxina’, sendo a mais tóxica dos 75 isômeros de compostos clorados de dibenzo-p-dioxina existentes.
FADINI, P S; FADINI, A. A. B. Lixo: desafios e compromissos. Cadernos Temáticos de Química Nova na Escola, São Paulo, n. 1, maio 2001 (adaptado).
Com base no texto e na estrutura apresentada, as propriedades químicas das dioxinas que permitem sua bioacumulação nos organismos estão relacionadas ao seu caráter
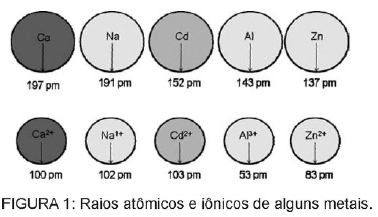
ATKINS, P; JONES, L. Princípios de química: Questionando a vida moderna e o meio ambiente. Porto Alegre: Bookman, 2001 (adaptado).
Com base no texto, a toxicidade do cádmio em sua forma iônica é consequência de esse elemento
O rótulo de uma garrafa de água mineral natural contém as seguintes informações:
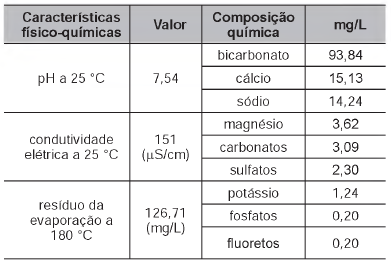
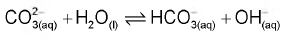
Esses tipos de solos são alcalinos demais para fins agrícolas e devem ser remediados pela utilização de aditivos químicos.
BAIRD, C. Química ambiental. São Paulo: Artmed, 1995 (adaptado).
Suponha que, para remediar uma amostra desse tipo de solo, um técnico tenha utilizado como aditivo a cal virgem (CaO). Nesse caso, a remediação
Fator de emissão de CO2 = Massa de CO2 emitida/ Quantidade de material
O termo “quantidade de material” pode ser, por exemplo, a massa de material produzido em uma indústria ou a quantidade de gasolina consumida por um carro em um determinado período.
No caso da produção do cimento, o primeiro passo é a obtenção do óxido de cálcio, a partir do aquecimento do calcário a altas temperaturas, de acordo com a reação:
CaCO3(s) → CaO(s) + CO2(g)
Uma vez processada essa reação, outros compostos inorgânicos são adicionados ao óxido de cálcio, tendo o cimento formado 62% de CaO em sua composição.
Dados: Massas molares em g/mol — CO2 = 44; CaCO3 = 100; CaO = 56.
TREPTOW, R. S. Journal of Chemical Education. v. 87 n° 2, fev. 2010 (adaptado).
Considerando as informações apresentadas no texto, qual é, aproximadamente, o fator de emissão de CO2 quando 1 tonelada de cimento for produzida, levando-se em consideração apenas a etapa de obtenção do óxido de cálcio?
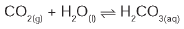
A alteração do equilíbrio anterior, relacionada ao vazamento do refrigerante nas condições descritas, tem como consequência a
1. A maioria dos produtos alimentícios se conserva por muito mais tempo quando submetidos à refrigeração. Esse procedimento diminui a rapidez das reações que contribuem para a degradação de certos alimentos. 2. Um procedimento muito comum utilizado em práticas de culinária é o corte dos alimentos para acelerar o seu cozimento, caso não se tenha uma panela de pressão. 3. Na preparação de iogurtes, adicionam-se ao leite bactérias produtoras de enzimas que aceleram as reações envolvendo açúcares e proteínas lácteas.
Com base no texto, quais são os fatores que influenciam a rapidez das transformações químicas relacionadas aos exemplos 1,2 e 3, respectivamente?