Questões Militares de Engenharia Química e Química Industrial - Termodinâmica e Equilíbrio de Fases
Foram encontradas 98 questões
Um mol de gás, em um vaso fechado, passa por um ciclo termodinâmico de 4 etapas. Na tabela a seguir estão apresentadas as variações da energia interna do gás, o calor adicionado ao sistema e o trabalho realizado pelo sistema em algumas etapas em que foi possível realizar as medições (dados em branco não foram medidos).
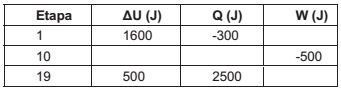
Fonte: Arquivo da Banca Elaboradora.
Na quadragésima etapa, foram adicionados 1300J ao sistema na forma de calor e o trabalho realizado pelo
sistema foi de
Um vaso fechado, a 120°C, contém 0,55mol de fenol e 0,45mol de tolueno. Nessa temperatura, a pressão de vapor do fenol é 13,0kPa e a do metanol é 131,3kPa.
Considerando que o sistema se encontra no ponto de orvalho, que a fase líquida se comporta como uma solução ideal e a fase vapor se comporta como uma mistura de gases ideais, a pressão no interior do vaso é
O saturador adiabático é um equipamento utilizado para umidificar o ar em um processo industrial. Esse equipamento consiste de uma câmara contendo água no estado líquido sobre a qual passa uma corrente de ar. A água evapora adiabaticamente e, assim, o ar que entra seco no equipamento, sai umidificado. Considerando um saturador adiabático que possua uma câmara que comporta 5.000cm3 de água e com uma altura h de 500cm. Ar seco entra no equipamento e, após umidifcado, sai com água a uma concentração igual a 50% da saturação, a uma velocidade constante, sem que haja perturbações na superfície da água. O nível da água é mantida constante devido ao bombeamento de 20cm3 .h-1 de água para dentro da câmara. O sistema opera a 25°C (298K) e 101kPa. O coeficiente de difusão da água no ar é igual a 900cm2 .h-1, a densidade da água líquida é 1,0g.cm-3, a massa molar da água é 18g.mol-1 e a pressão de vapor da água 3,17kPa.
A constante dos gases pode ser admitida como 8314kPa.cm3 .mol-1.K-1.

Fonte: Arquivo da Banca Elaboradora.
O fluxo de água que evapora é igual a
Muitos foram os pesquisadores que contribuíram para as leis conhecidas como Leis dos Gases. Algumas das contribuições mais importantes dos gases ideais estão resumidas nos postulados na lei de Boyle, lei de Charles, lei de Gay-Lussac e lei de Clapeyron. Com relação às leis dos gases, analise as afirmativas a seguir.
I. De acordo com a lei de Boyle, a pressão e o volume de um gás são inversamente proporcionais entre si para um gás ideal.
II. De acordo com a lei de Gay-Lussac, a velocidade de difusão e de efusão de um gás é inversamente proporcional à raiz quadrada de sua densidade.
III. De acordo com a lei de Charles, o volume de um gás é diretamente proporcional à sua temperatura absoluta.
IV. De acordo com a lei de Clapeyron, à volume constante, a pressão de uma certa massa constante de um gás é proporcional à temperatura absoluta a qual está submetida.
Está correto apenas o que se afirma em