Questões Militares Sobre química
Foram encontradas 2.062 questões
Um laboratorista pesou separadamente uma amostra I, de hidróxido de sódio (NaOH), e uma amostra II, de óxido de cálcio (CaO), e, como não dispunha de etiquetas, anotou somente a soma das massas das amostras (I + II) igual a 11,2 g.
Cada uma das amostras I e II foi tratada separadamente com ácido sulfúrico (H 2SO4) produzindo, respectivamente, sulfato de sódio (Na2SO4) mais água (H2O) e sulfato de cálcio (CaSO4) mais água (H2O). Considere o rendimento das reações em questão igual a 100%.
Sendo a soma das massas dos sais produzidos (Na 2SO4 + CaSO4) igual a 25,37 g, então a massa da amostra I de hidróxido de sódio (NaOH) e a massa de amostra II de óxido de cálcio (CaO) são, respectivamente:
Dados:

A concentração em mol · L-1 dos íons sulfato ( SO
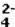 ) presentes na solução final é :
) presentes na solução final é :
A Tabela II mostra os elementos químicos (H, F, Cl, Br e I) e suas respectivas massas atômicas.
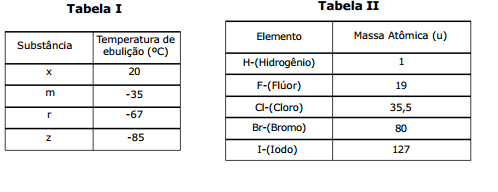
Com base nas Tabelas acima, são feitas as seguintes afirmações:
I- As substâncias correspondentes a x, m, r e z são, respectivamente, HF, HI, HBr e HCl.
II- As moléculas de HCl, HBr e HI são unidas por forças do tipo pontes ou ligações de hidrogênio.
III- Das substâncias em questão, o HI apresenta a maior temperatura de ebulição, tendo em vista possuir a maior massa molar.
Das afirmações feitas, está(ão) correta(s) apenas:
4 C3H5(NO3)3(l) → 6 N2(g) + 12 CO(g) + 10 H2O(g) + 7 O2(g)
Considerando os gases acima como ideais, a temperatura de 300 Kelvin (K) e a pressão de 1 atm, o volume gasoso total que será produzido na detonação completa de 454 g de C3H5(NO3)3(l) é:
Dados:
Elemento H(hidrogênio) C( carbono) O ( Oxigênio) N( nitrogênio)
Massa 1 12 16 14
atômica(u)
Constante universal dos gases: R=8,2 · 10-2 atm · L · K-1 · mol-1
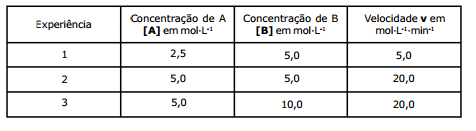
Baseando-se na tabela, são feitas as seguintes afirmações:
I- A reação é elementar.
II- A expressão da velocidade da reação é v=K·[A] 3·[B]2.
III- A expressão da velocidade da reação é v=K·[A] 2.[B]0.
IV- Dobrando-se a concentração de B, o valor da velocidade da reação não se altera.
V- A ordem da reação em relação a B é 1 (1ª ordem).
Das afirmações feitas, utilizando os dados acima, estão corretas apenas
FeSO4(aq) + Ag(s) → não ocorre a reação
2 AgNO3(aq) + Fe(s) → Fe(NO3)2(aq) + 2 Ag(s)
3 Fe(SO4)(aq) + 2 Al(s) → Al2(SO4)3(aq) + 3 Fe(s)
Al2(SO4)3(aq) + Fe (s) → não ocorre a reação
De acordo com as reações acima equacionadas, a ordem decrescente de reatividade dos metais envolvidos em questão é:
Dada a seguinte equação iônica de oxidorredução:
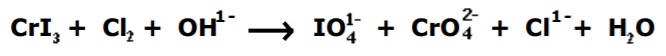
Considerando o balanceamento de equações químicas por oxidorredução, a soma total dos coeficientes mínimos e inteiros obtidos das espécies envolvidas e o(s) elemento(s) que sofrem oxidação, são, respectivamente,
(25 °C e 1 atm), expressas em kJ · mol -1.

A alternativa que corresponde ao valor da entalpia da reação abaixo, nas condições-padrão, é:
4 C(grafita)(s) + 5 H2(g) → C4H10(g)
Com base na equação da reação química que ocorre no borbulhador, é correto afirmar que o peróxido de hidrogênio atuou no processo como agente oxidante.
Considerando que, na titulação do ácido sulfúrico formado no borbulhador, foram gastos 3,2 mol de NaOH e que o totalizador de volume indicou 4 m3 de amostra de ar, conclui-se que, nessa análise, a concentração de dióxido de enxofre no ar amostrado era de 8 × 10-4 mol / L.
O método de separação de misturas representado pelo dispositivo 2, representado na figura, também é eficaz para a separaração dos componentes da solução resultante do processo de titulação empregado na dosagem do ácido sulfúrico.
O dióxido de enxofre, além ser um poluente atmosférico associado à formação de precipitações ácidas, tem destacado papel como gás estufa, influindo no aquecimento global.
Da análise da estrutura do dióxido de carbono (CO2) , conclui-se que, apesar de a ligação entre C e O ser polar, a molécula é apolar pelo fato de sua geometria ser linear.
O raio do íon sódio (Na+) é inferior ao do íon potássio (K+).
O fato de o carbono na molécula de CO2 apresentar estado de oxidação o mais reduzido possível corrobora a informação mencionada no texto de que essa substância não atua como combustível.
O bicarbonato de sódio é um hidrogenossal que apresenta, em sua estrutura, ligações iônicas e covalentes.
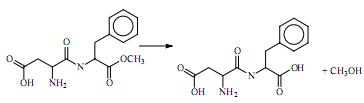
Considerando-se que o aspartame se degrada em aspartilfenilalanina e metanol sob exposição prolongada ao calor, de acordo com a equação química a seguir, é correto afirmar que, nessas condições, a molécula de aspartame sofre oxidação.
A maior solubilidade em água do benzoato de sódio em relação ao ácido benzoico deve-se, especialmente, ao fato de o grupo carboxilato ser mais hidrofílico que o grupo carboxila.
De acordo com o texto, a concentração máxima de ácido benzoico permitida em bebidas refrigerantes é superior a 40 mmol/L.
Infere-se da estrutura do aspartame, apresentada acima, que estão presentes, em sua composição, as funções ácido carboxílico, amina, amida e éter.


