Questões Militares
Sobre representação das transformações químicas em química
Foram encontradas 289 questões
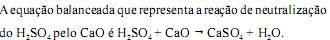
A corrosão de objetos metálicos é acelerada em meio ácido. Supõe-se ter sido esse fator preponderante para o trágico desabamento de parte das arquibancadas do estádio da Fonte Nova, em Salvador – BA, em 2007, que causou a morte de 8 pessoas. Os torcedores tinham o hábito de urinar nas arquibancadas do estádio.
Como a estrutura de concreto é porosa, a urina, que contém ácidos e sais, penetrava e atingia a estrutura de ferro do estádio, o que causou a sua corrosão.
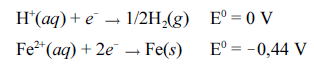
Tendo como base essas informações e considerando os potenciais padrão (E0) fornecidos para as semirreações acima, julgue o item subsequente.
A reação balanceada que representa a corrosão de uma peça de ferro pelo íon
H+ é H+(aq) + Fe(s)  1/2H2(g) + Fe2+(aq).
1/2H2(g) + Fe2+(aq).

Com base nessas informações e considerando
 a variação de
a variação deentalpia padrão das reações a 25 ºC, julgue os itens a seguir.
Em uma eletrólise ígnea do cloreto de sódio, uma corrente elétrica, de intensidade igual a 5 ampères, atravessa uma cuba eletrolítica, com o auxilio de dois eletrodos inertes, durante 1930 segundos.
O volume do gás cloro, em litros, medido nas CNTP, e a massa de sódio, em gramas, obtidos nessa eletrólise, são, respectivamente:
A composição química do cimento Portland, utilizado na construção civil, varia ligeiramente conforme o que está indicado na tabela abaixo:
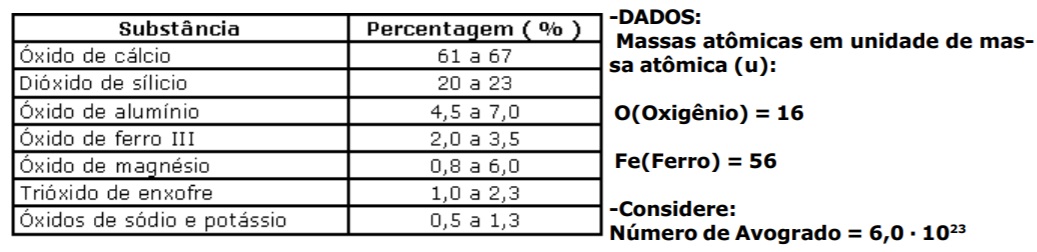
Assinale a alternativa correta:
I-mono-hidrogenossulfito de potássio + ácido clorídrico → ácido sulfuroso + cloreto de potássio
II-fosfato de cálcio + dióxido de silício + carvão → metassilicato de cálcio + monóxido de carbono + fósforo branco
A tabela abaixo apresenta alguns dos produtos químicos existentes em uma residência.
Assinale a alternativa correta:
Um laboratorista pesou separadamente uma amostra I, de hidróxido de sódio (NaOH), e uma amostra II, de óxido de cálcio (CaO), e, como não dispunha de etiquetas, anotou somente a soma das massas das amostras (I + II) igual a 11,2 g.
Cada uma das amostras I e II foi tratada separadamente com ácido sulfúrico (H 2SO4) produzindo, respectivamente, sulfato de sódio (Na2SO4) mais água (H2O) e sulfato de cálcio (CaSO4) mais água (H2O). Considere o rendimento das reações em questão igual a 100%.
Sendo a soma das massas dos sais produzidos (Na 2SO4 + CaSO4) igual a 25,37 g, então a massa da amostra I de hidróxido de sódio (NaOH) e a massa de amostra II de óxido de cálcio (CaO) são, respectivamente:
Dados:

A concentração em mol · L-1 dos íons sulfato ( SO
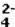 ) presentes na solução final é :
) presentes na solução final é :
4 C3H5(NO3)3(l) → 6 N2(g) + 12 CO(g) + 10 H2O(g) + 7 O2(g)
Considerando os gases acima como ideais, a temperatura de 300 Kelvin (K) e a pressão de 1 atm, o volume gasoso total que será produzido na detonação completa de 454 g de C3H5(NO3)3(l) é:
Dados:
Elemento H(hidrogênio) C( carbono) O ( Oxigênio) N( nitrogênio)
Massa 1 12 16 14
atômica(u)
Constante universal dos gases: R=8,2 · 10-2 atm · L · K-1 · mol-1
Dada a seguinte equação iônica de oxidorredução:
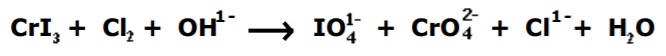
Considerando o balanceamento de equações químicas por oxidorredução, a soma total dos coeficientes mínimos e inteiros obtidos das espécies envolvidas e o(s) elemento(s) que sofrem oxidação, são, respectivamente,
Considerando que, na titulação do ácido sulfúrico formado no borbulhador, foram gastos 3,2 mol de NaOH e que o totalizador de volume indicou 4 m3 de amostra de ar, conclui-se que, nessa análise, a concentração de dióxido de enxofre no ar amostrado era de 8 × 10-4 mol / L.
De acordo com o texto, a concentração máxima de ácido benzoico permitida em bebidas refrigerantes é superior a 40 mmol/L.
Considerando-se que o rendimento da reação completa de combustão do butano seja de 100%, é correto afirmar que, para a queima completa de 116 g desse hidrocarboneto, seria necessária massa mínima de oxigênio superior a 410 g.
Os átomos de um elemento Z cujo número atômico é 20 se unem com os átomos de um elemento Y cujo número atômico é 7 através de uma ligação iônica. Qual a fórmula do composto formado por esses dois elementos?
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
A taxa de emissão de dióxido de carbono em função do consumo médio de certo combustível, em um carro de testes, é apresentada a seguir.
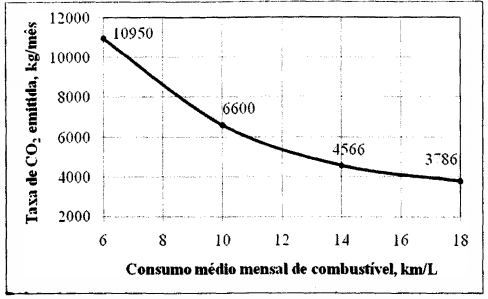
Para um consumo médio de 10 km/L, a massa total mensal de combustível consumida é 2175
kg. Dentre as opções abaixo, pode-se afirmar que o combustível testado foi o:
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1



