Questões Militares
Sobre soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. em química
Foram encontradas 114 questões
Das afirmativas apresentadas estão corretas apenas
Coloque F (falso) ou V (verdadeiro), nas afirmativas abaixo, assinalando a seguir a opção correta.
( ) Na formação de um precipitado, é necessário considerar as etapas de nucleação e o crescimento dos cristais.
( ) Segundo a equação de Von Weimarn, quanto maior a concentração dos reagentes, maior o grau de dispersão e menor o tamanho das partículas.
( ) Precipitados formados por aglomeração coloidal são amorfos e porosos, com enormes áreas superficiais.
( ) É comum, nos procedimentos gravimétricos, deixar o precipitado repousar na presença da água mãe, durante um determinado tempo, antes de ser filtrado.

Com base nestes dados, e sabendo que HA tem constante de ionização igual a 4,0 x 10−10, é coerente afirmar que o indicador HA
(Dado: log 4 = 0,6)
Observe a reação a seguir.
H2C2O4(aq) + 2OH- (aq) → C2O4- (aq) + 2H2O(I)
Suponha que um técnico em química dissolva em água uma
amostra de 1,0g de ácido oxálico impuro e adicione algumas
gotas de indicador ácido-base. Em seguida, ele titula a
solução com NaOH 0,5M. A amostra consome 40mL da solução de
NaOH até atingir o ponto de equivalência. Qual é a massa de
ácido oxálico na amostra inicial?
Assinale a opção que completa corretamente as lacunas da sentença abaixo.
Considere que determinado ácido sofre uma diluição, de modo que sua concentração de íons H+ é alterada de 4x10-7mol/l para 5x10-8 mol/l. Sendo assim, é correto afirmar que o pH da solução original foi alterado de____________ para ___________ .
Dados:
log(2) = 0,301
log(3) = 0,477
log(5) = 0,698
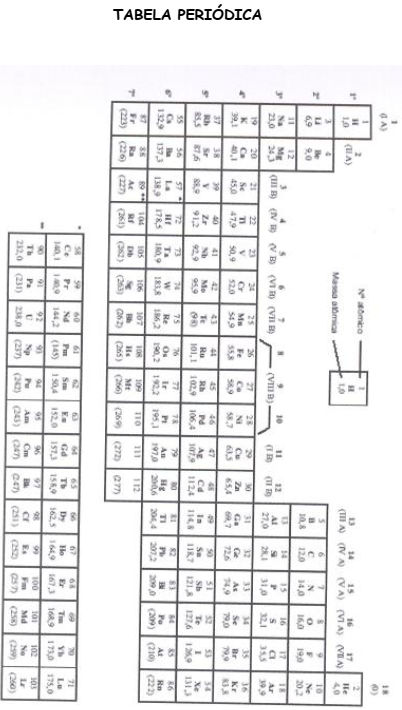
Com base nas informações acima e na tabela periódica, incluída no final deste caderno de provas, julgue os itens a seguir.
Com base nas informações acima e na tabela periódica, incluída no final deste caderno de provas, julgue os itens a seguir.
NH4NO3 ( s ) → NH3 ( g ) + N2O ( g ) + NO2 ( g ) + H2O ( g ) + O2 ( g )
Com base nessas informações, julgue os itens que se seguem, considerando que as massas molares do N, do H e do O sejam iguais a 14, 1 e 16 g/mol, respectivamente.
Considere que 3,0 L de uma solução de NH4NO3 tenham sido preparados pela dissolução de 8,0 g do composto em quantidade suficiente de água. Nessa situação, é correto afirmar que a concentração da solução preparada é superior a 0,030 mol/L.
Dado: massa molar do Sulfato de Bário = 233 g/mol