Questões de Concurso
Sobre cinética química em química
Foram encontradas 829 questões
No passado, muitos cientistas acreditavam na concepção do filósofo grego Aristóteles, 384-322 a.C, de que tudo no Universo seria formado por quatro “elementos”: ar, água, fogo e terra. Essa ideia permaneceu aceita até o século XVII, quando o cientista irlandês Robert Boyle, 1627-1691, apresentou argumentos sobre o conceito de elemento químico como qualquer substância pura que não se decompõe, como o hidrogênio e o oxigênio obtidos a partir da decomposição da água. A Química somente adquiriu caráter cientifico a partir do século XVIII, com A. L. Lavoisier, quando o trabalho feito no laboratório foi vinculado ao esforço de buscar explicação para a natureza da matéria e de suas transformações.
Considerando-se o aperfeiçoamento, ao longo do tempo, dos conhecimentos sobre a natureza da matéria e o surgimento da Química como ciência, é correto afirmar:
Há cerca de 500 mil anos, ocorreu uma das maiores descobertas da humanidade, o fogo. A primeira fogueira acesa mudou o curso da história da espécie humana. Com o fogo o ser humano primitivo conseguiu iluminar a caverna, se aquecer, cozinhar os alimentos e afugentar os animais, um grande progresso. A tirinha de Bob Thaves faz alusão ao consumo demasiado de combustível, na geração de energia pela combustão da lenha.
Considerando-se essas informações relacionadas à produção de fogo e de energia e a tirinha de Bob Thaves, é correto afirmar:
Para calibração de um método fotométrico com a finalidade de determinar a quantidade de sódio em uma amostra, foi necessário preparar uma solução padrão de Na+ (0,0100 mol/L). Dentre as alternativas abaixo, qual delas indica o volume (em litros) dessa solução padrão previamente preparada necessário para produzir um volume de 50,00 mL de uma solução de Na+ (0,00500 mol/L)?
Um perito oficial dissolveu certa quantidade de um sal em solvente e, por alguma perturbação, parte do sal se depositou, produzindo uma solução. Pode-se considerar nominalmente essa solução como:
A produção de aço envolve o aquecimento do minério de ferro, junto com carvão (carbono) e ar atmosférico em uma série de reações de oxirredução. O produto é chamado de ferro-gusa e contém cerca de 3,3% de carbono. Uma forma de eliminar o excesso de carbono é a oxidação a partir do aquecimento do ferro-gusa com gás oxigênio puro. Os dois principais produtos formados são aço doce (liga de ferro com teor de 0,3% de carbono restante) e gás carbônico. As massas molares aproximadas dos elementos carbono e oxigênio são, respectivamente, 12 g/mol e 16 g/mol.
LEE, J. D. Química Inorgânica não tão concisa. São Paulo: Edgard Blucher, 1999 (adaptado).
Considerando que um forno foi alimentado com 2,5 toneladas de ferro-gusa, a massa de gás carbônico formada, em quilogramas, na produção de aço doce, é mais próxima de
A varfarina é um fármaco que diminui a agregação plaquetária, e por isso é utilizada como anticoagulante, desde que esteja presente no plasma, com uma concentração superior a 1,0 mg/L. Entretanto, concentrações plasmáticas superiores a 4,0 mg/L podem desencadear hemorragias. As moléculas desse fármaco ficam retidas no espaço intravascular e dissolvidas exclusivamente no plasma, que representa aproximadamente 60% do sangue em volume. Em um medicamento, a varfarina é administrada por via intravenosa na forma de solução aquosa, com concentração de 3,0 mg/mL. Um indivíduo adulto, com volume sanguíneo total de 5,0 L, será submetido a um tratamento com solução injetável desse medicamento.
Qual é o máximo volume da solução do medicamento que pode ser administrado a esse indivíduo, pela via intravenosa, de maneira que não ocorram hemorragias causadas pelo anticoagulante?
A formação frequente de grandes volumes de pirita (FeS2) em uma variedade de depósitos minerais favorece a formação de soluções ácidas ferruginosas, conhecidas como “drenagem ácida de minas”. Esse fenômeno tem sido bastante pesquisado pelos cientistas e representa uma grande preocupação entre os impactos da mineração no ambiente. Em contato com oxigênio, a 25 °C, a pirita sofre reação, de acordo com a equação química:
4 FeS2 (s) + 15 O2 (g) + 2 H2O (I) 2Fe2(SO4)3 (aq) + 2 H2SO4 (aq)
FIGUEIREDO, B. R. Minérios e ambiente. Campinas: Unicamp, 2000.
Para corrigir os problemas ambientais causados por essa drenagem, a substância mais recomendada a ser adicionada ao meio é o
Glicose marcada com nuclídeos de carbono-11 é utilizada na medicina para se obter imagens tridimensionais do cérebro, por meio de tomografia de emissão de pósitrons. A desintegração do carbono-11 gera um pósitron, com tempo de meia-vida de 20,4 min, de acordo com a equação da reação nuclear:
+
(pósitron)
A partir da injeção de glicose marcada com esse nuclídeo, o tempo de aquisição de uma imagem de tomografia é de cinco meias-vidas.
Considerando que o medicamento contém 1,00 g do carbono-11, a massa, em miligramas, do nuclídeo restante, após a aquisição da imagem, é mais próxima de
O brasileiro consome em média 500 miligramas de cálcio por dia, quando a quantidade recomendada é o dobro. Uma alimentação balanceada é a melhor decisão para evitar problemas no futuro, como a osteoporose, uma doença que atinge os ossos. Ela se caracteriza pela diminuição substancial de massa óssea, tornando os ossos frágeis e mais suscetíveis a fraturas.
Disponível em: www.anvisa.gov.br. Acesso em: 1 ago. 2012 (adaptado).
Considerando-se o valor de 6 × 1023 mol–1 para a constante de Avogadro e a massa molar do cálcio igual a 40 g/mol, qual a quantidade mínima diária de átomos de cálcio a ser ingerida para que uma pessoa supra suas necessidades?
O cloreto de cobalto (II) é um composto químico utilizado como indicador de umidade devido às suas diferentes formas anidra e hidratada apresentarem coloração bem distinta. A forma anidra CoCl2 é azul, e a forma hidratada (úmida) CoCl2·6H2O é rosa profundo. Esta característica o faz ser um dos mais comuns compostos de cobalto em laboratórios. A forma anidra pode ser preparada a partir do metal cobalto e gás cloro:
Co(s) = Cl2(g) → CoCl2(s)
Uma mistura em equilíbrio contém 20 g de CO, 35 g de Cl2 e 198 g de COCl2 num recipiente de 2,5 L de capacidade. Identifique a alternativa que apresenta, respectivamente, as concentrações molares (mol/L) do Co, Cl2 e do CoCl2, de forma correta:
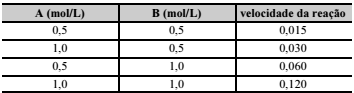
De acordo com a lei da ação das massas, a velocidade de uma reação é diretamente proporcional ao produto das concentrações molares dos reagentes. Assim, para a reação aA + bB ⇄ cC + dD, a equação da velocidade é V = K·[A]a ·[B]b . Considerando essas informações e que, na tabela acima, são apresentados resultados experimentais para essa mesma reação, assinale a opção correta.
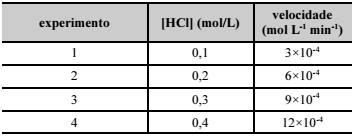
Considerando a tabela acima, que apresenta os valores de
concentração de HCl e das velocidades de decomposição do gás
cloreto de hidrogênio obtidos experimentalmente, conforme reação
elementar 2HCl(g) → H2(g) + Cl2(g), e que não houve variação de
temperatura, assinale a opção que apresenta a constante de
velocidade característica dessa reação.
O biodísel pode ser obtido a partir da reação de transesterificação do óleo de soja catalisada por base. Com o objetivo de aumentar o rendimento do produto dessa reação em bancada, foi aplicada a metodologia de planejamento fatorial, sendo os fatores, níveis estudados e efeitos obtidos apresentados na tabela abaixo.

Considerando as informações acima apresentadas, julgue o item a
seguir, relativo à otimização da reação e ao planejamento de
experimentos realizados.
O biodísel pode ser obtido a partir da reação de transesterificação do óleo de soja catalisada por base. Com o objetivo de aumentar o rendimento do produto dessa reação em bancada, foi aplicada a metodologia de planejamento fatorial, sendo os fatores, níveis estudados e efeitos obtidos apresentados na tabela abaixo.

Considerando as informações acima apresentadas, julgue o item a seguir, relativos à otimização da reação e ao planejamento de experimentos realizados.
Para aumentar o rendimento da reação em apreço deve-se usar
KOH e realizá-la à temperatura de 50 °C durante o tempo
de 60 min.
Nesse sentido, observa-se que
A decomposição do ozônio é representada pela seguinte equação não balanceada: O3 → O2, e a lei da velocidade dessa reação é representada pela seguinte equação: e a lei da velocidade dessa reação é representada pela seguinte equação: V = k [ O3]2 [ O2]-1.
Considerando essa situação hipotética e sabendo que, durante o processo de compostagem, as proteínas presentes na matéria orgânica do lixo são hidrolisadas por enzimas proteolíticas produzidas por microrganismos, gerando polipeptídios, aminoácidos e outros derivados nitrogenados, e o nitrogênio orgânico é convertido à forma amoniacal, julgue os próximos itens.
Durante o processo de compostagem, ocorrem fenômenos químicos envolvendo processo de catálise, no qual moléculas maiores são convertidas em moléculas menores.
A equação química acima descreve a queima do gás metano, uma reação de combustão muito utilizada na indústria. A partir dessas informações, julgue os itens a seguir.