Questões de Concurso
Sobre sistemas heterogêneos: produto de solubilidade (kps). em química
Foram encontradas 90 questões
No meio aquoso, esses dois sais reagem instantaneamente, de acordo com a equação balanceada abaixo, e nela se forma um sal muito pouco solúvel.

A quantidade máxima, em gramas, de AgCL sólido (massa molar = 143,5 g/mol e Kps = 10-10 ) que se forma é de, aproximadamente,
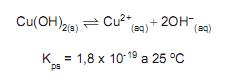
Sendo o valor do pH ideal da água da piscina igual a 6, a quantidade máxima de CuSO4 . 5H2 O em massa, que deve ser adicionada a uma piscina de volume igual a 10.000 L, com água no pH ideal, em kg, é
Adicionando-se cloreto de sódio na proporção de 2 mol/L de solução, qual o teor residual de prata, em mol/L, que permanecerá solúvel?
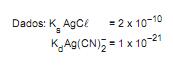
- o produto precipitado deve ser suficientemente insolúvel para que não ocorram perdas na filtração e lavagem;
- a natureza física do precipitado deve ser tal que permita ser separado da solução por filtração e possa ser lavado até ficar livre de impurezas solúveis;
- o produto precipitado deve ser conversível em uma substância pura de composição química;
- o agente precipitante não deve ser reativo com os constituintes da atmosfera.
Considerando que o produto de solubilidade do AgCl, em água pura, seja 1,6 x 10-10 (Kps a 25 °C) e que a solubilidade do AgCl seja 1,3 x 10-5 mol/L, qual seria a solubilidade de Ag+ em uma solução de NaCl 0,10 M?
Etapa I - Adição de quantidade conhecida de Ag+ para garantir a reação completa com todo íon haleto (X- ) e excesso de Ag+ na solução Ag+(aq) + X- (aq) → AgX(s)
Etapa II - Titulação do excesso de Ag+
Ag+ (aq) + SCN-(aq) → AgSCN(s)
Etapa III - Formação de complexo vermelho com o primeiro excesso de SCN-
SCN- + Fe3+→ [(Fe(SCN)] 2+(aq)
Com base nas informações relativas a cada etapa do processo, analise as afirmações a seguir.
I - O SCN- atua como indicador do ponto ? nal da titulação.
II - Pelo fato de o valor do
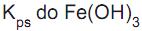 do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido.
do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido. III - O
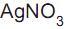 é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz.
é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz. IV - Nas titulações argentométricas, os sais de prata tipo AgX são bem solúveis em água.
É correto APENAS o que se afirma em
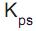 = 1,8 x 10-14 .
= 1,8 x 10-14 .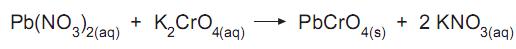
Se a uma solução aquosa contendo 0,01 mol de nitrato de chumbo II adiciona-se um volume pequeno de solução aquosa contendo 0,00002 mol de cromato de potássio, a quantidade máxima de precipitado de cromato de chumbo II que se forma é, em miligramas, aproximadamente igual a
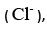 precipitado na forma de cloreto de prata (AgCl).
precipitado na forma de cloreto de prata (AgCl). Analise a situação a seguir.
Em um experimento de Química Geral, um estudante misturou 1 mL de uma solução aquosa de nitrato de chumbo (Pb(NO3 )2 ) 0,2 mol/L com 10 mL de uma solução aquosa de iodeto de potássio (KI) 0,05 mol/L.
Considerando que o experimento foi realizado a certa temperatura, em que o Kps do iodeto de chumbo (PbI2 ) é igual a 1 x 10–8, quanto em porcentagem da massa total do iodeto de chumbo ficou solúvel na mistura?
Internet: <http://portal.anvisa.gov.br> (com adaptações).
Ao analisar a problemática do uso desse medicamento contaminado, observa-se a importância social do conhecimento químico. Considerando essa informação e que o produto de solubilidade (Kps) do BaSO4 é igual a 1 x 10-10, assinale a alternativa correta.
