Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.239 questões
Use: Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-1; N = 14 g mol-1; Cl = 35,5 g mol-1
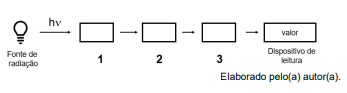
Com base no esquema acima, os componentes 1, 2, e 3 são, respectivamente:
Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-
Quando um composto iônico solúvel é adicionado à água, ocorre um processo chamado de hidratação, onde as moléculas de água envolvem os íons da superfície do sólido, separando-os dos outros íons e dissolvendo-os, gradativamente. Este processo ocorre pelas interações íon-dipolo entre as moléculas da água e os íons devido ao caráter polar da molécula de H2O, onde a carga parcial negativa do átomo de O é atraída pelos cátions e as cargas parciais positivas dos átomos de H são repelidas por eles.
ATKINS, Peter; LAVERMAN, Leroy; JONES, Loretta. Princípios de química: questionando a vida moderna e o meio ambiente. 7. Porto Alegre: Bookman, 2018.[Adaptado].
Baseado no texto acima, para qual dos cátions listados abaixo espera-se a maior energia de interação íon-dipolo?.
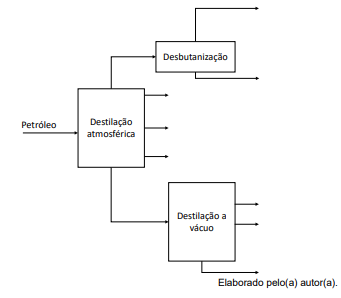
No processo descrito no fluxograma anterior, as destilações ocorrem produzindo
É correto afirmar que são encontradas em jazidas na crosta terrestre:
pH = pKa + log([OAc–] / [HOAC])
Com relação a esse exemplo, assinale a alternativa correta.
ER║HA, CA│Pt, H2 (1 atm)
Dados:
ΔE = Ec – Ea
Ka = [H3O+] . [A–] / [HA]
E = E0 – (0,0592 / n). log ([Red.] / [Oxid.]), em que “Red.” é a espécie reduzida, e “Oxid.”, a oxidada.
Com relação ao exposto, assinale a alternativa que expressa corretamente a relação entre Ka e ΔE.