Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.297 questões
Quanto às soluções, julgue o item seguinte.
Um composto molecular dissolve‑se em água
formando, invariavelmente, moléculas carregadas
eletricamente (íons) dispersas pela solução, formando
um eletrólito.
Quanto às soluções, julgue o item seguinte.
Quando em solução aquosa, os íons positivos
provenientes de um sólido iônico (cátions) são atraídos
pelo lado negativo da molécula da água, enquanto os
íons negativos (ânions) são atraídos pelo lado positivo.
Quanto às soluções, julgue o item seguinte.
Quando o cloreto de sódio (NaCl) se dissolve em água,
cada íon separa‑se da estrutura cristalina e dispersa‑se
pela solução, ou seja, o sólido iônico dissocia‑se em
seus íons constituintes à medida que se dissolve.
A respeito dos ácidos, bases, sais e óxidos, julgue o item seguinte.
Os óxidos iônicos binários são compostos formados
por oxigênio e por mais dois outros elementos
químicos, sendo sua fórmula apresentada por esses
elementos precedidos pelo símbolo do oxigênio.
A respeito dos ácidos, bases, sais e óxidos, julgue o item seguinte.
Presente na água da chuva, o dióxido de carbono (CO2) reage com a água formando ácido carbônico (H2CO3), conforme a equação química apresentada a seguir.
CO2 (g) + H2O (l) → H2CO3 (aq)
A respeito dos ácidos, bases, sais e óxidos, julgue o item seguinte.
A base de Brønsted‑Lowry é uma espécie química
capaz de receber um ou mais prótons. Essa teoria leva
em conta vários compostos com caráter básico que
não liberam o íon hidroxila, quando dissolvidos em
solução aquosa.
Acerca das transformações da matéria, julgue o item seguinte.
Em uma reação de neutralização, quando uma substância ácida e uma substância básica são misturadas, obtêm‑se, como produtos, sal e água, conforme apresentado pela equação química a seguir.
HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l)
Al2(SO4)3 + Ca(OH)2 → Al(OH)3 + CaSO4
Certo químico coletou um espectro de absorção
eletrônica de uma substância natural porfirínica. O
espectro obtido (com simplificações) em etanol encontrase apresentado na imagem a seguir. A cubeta utilizada foi
de quartzo, com apenas duas faces polidas e 1 cm de
caminho óptico.

Sobre a coleta do espectro apresentado na imagem,
assinale a alternativa correta.
Certo químico coletou um espectro de absorção
eletrônica de uma substância natural porfirínica. O
espectro obtido (com simplificações) em etanol encontrase apresentado na imagem a seguir. A cubeta utilizada foi
de quartzo, com apenas duas faces polidas e 1 cm de
caminho óptico.

Se a absortividade molar da substância (em etanol e λ=
665 nm) é 70 x 103 L.mol-1
.cm-1 , a concentração da
espécie na cubeta será de:
Certo profissional preparou uma solução de hidróxido de cálcio na concentração de 0,3 mol/L. O pH dessa solução será de aproximadamente:
Considere os valores logaritmos, se necessário, de 
O Sulfato de Ferro heptahidratado é empregado como
parte integrante de um fertilizante hidrossolúvel
disponível no mercado para uso em adubação foliar,
fertirrigação ou aplicação direta no solo. Uma amostra
desse fertilizante foi submetida à análise físico-química,
na qual o profissional utilizou o Sulfato de ferro (II)
heptahidratado sólido, de grau analítico, fornecido pela
marca Merck, como padrão de referência. A massa molar
aproximada dessa substância é:
Na rotina de laboratório, o químico precisou coletar 10 µL
de uma solução estoque de azul de metileno 5,0 mol/L e
solubilizar em 10 ml de água destilada. A imagem ilustra
uma etapa do procedimento realizado.

Com base nas informações apresentadas, assinale a
alternativa que apresenta a concentração da solução de
azul de metileno diluída.
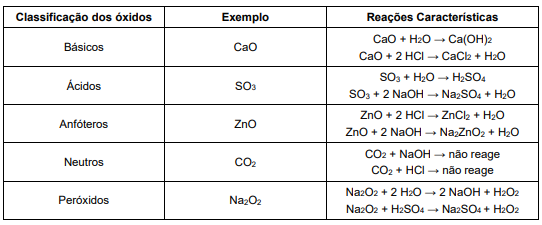
Ao observar a tabela, o professor precisou explicar ao estudante que um exemplo estava errado e não correspondia à classificação sugerida. A categoria cujo exemplo está incorreto é a dos óxidos:
Massas molares em g/mol: C = 12; O = 16; Ca = 40
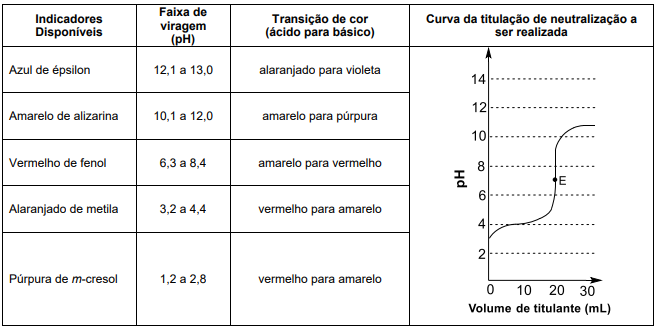
O indicador que o técnico deve utilizar é:

Nessa localidade há um rio em que ocorre despejo de efluentes industriais de uma empresa do ramo metalúrgico. Em um procedimento de fiscalização, uma amostra desse efluente foi coletada para análise e identificou-se a presença tanto de íons Cr2+ como de íons Hg2+ em concentrações de 1,0 x 10-3 g/L e 1,5 x 10-3 g/L, respectivamente. Considerando a densidade da amostra igual a 1g/cm3 , é correto afirmar que: