Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.171 questões
A osmose é a passagem de solvente através de uma membrana semipermeável de um meio para outro meio mais concentrado. Para evitar a osmose e garantir o equilíbrio entre os meios, é necessária a aplicação de uma pressão π (pressão osmótica) no meio mais concentrado. Considere o esquema a seguir, em que volumes iguais de água destilada e de determinada solução aquosa estejam separados por uma membrana porosa permeável ao solvente. Considere, ainda, que foram medidos os valores de pressão osmótica de três soluções aquosas distintas: 1) CH3COOH(aq) 0,010 mol/L; 2) NaOH(aq) 0,010 mol/L e 3) CaCl2(aq) 0,008 mol/L.
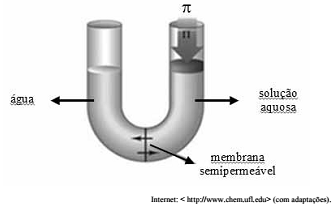
Com base nessas informações e supondo que as soluções
comportem-se idealmente, a ordem crescente das pressões
osmóticas medidas corresponde a
I. NaHCO3 II. HClO4 III. NH4OH IV. H3PO4 V. CaCl2
Considere as três reações químicas indicadas que envolvem ácido sulfúrico e assinale a alternativa incorreta.
I. H2SO4 + CaCO3 → CaSO4 + H2O+ CO2
II. H2SO4 + 2 NaOH → Na2SO4 + 2 H2O
III. H2SO4 + Mg(OH)2 → MgSO4 + 2 H2O
O modelo mais tradicional considera como ácido uma substância que libera o íon H+ e como base uma substância que libere o íon OH-. No entanto, esse modelo não contempla a neutralização de ácidos por moléculas que não contenham o íon OH-, como no caso da reação da amónia com o ácido clorídrico:
HCI(g) + NH3(I) ⇄ NH4+ + Cl-
O modelo de Lowry-Bronsted altera este modelo, de forma a abranger reações como a acima. Assinale a alternativa que corresponde a essa nova definição.
Sobre a bauxita, que é utilizada como principal fonte de extração do alumínio metálico, analise as afirmativas a seguir e assinale a alternativa correta.
I. É uma mistura de óxidos de óxidos de alumínio, principalmente Al2O3, sendo abundante na natureza.
II. A extração do alumínio metálico, a partir desse óxido, envolve um processo de redução eletroquímica.
III. A dificuldade de extração do alumínio desse material fez com que o alumínio metálico, embora seja o metal mais abundante na crosta terrestre, só passasse a ser utilizado amplamente a partir do século XIX.
Estão corretas as afirmativas:
As substâncias inorgânicas possuem diversas aplicações: o Aℓ2(SO4)3 é utilizado em uma das etapas do tratamento de água, o H2SO4 é matéria-prima para produção de fertilizantes, o Aℓ (OH)3 é empregado em medicamentos, e o Aℓ2O3 é utilizado na fabricação de materiais cerâmicos.
A respeito dessas substâncias, verifica-se que o
Uma solução aquosa de bicarbonato de sódio (NaHCO3) foi preparada em um balão volumétrico de 250,00 mL utilizando-se 10,0 g do soluto, com o volume final ajustado pela adição de água pura. Dessa solução foi retirada uma alíquota de 25,00 mL, que foi transferida para um balão de 100,00 mL, no qual o volume final foi ajustado pela adição de água pura.
Os valores mais próximos das concentrações, em quantidade de matéria (mol L-1), da solução inicial e da solução após a diluição são, respectivamente,
Dado
M (NaHCO3) = 84,0 g mol-1
Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5

Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5

Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5

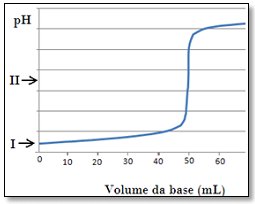
A figura apresentada ao lado representa a titulação para 100 mL de uma solução de HCl com uma solução padrão de NaOH 0,2 mol L-1 .
Os valores de pH indicados pelas setas no gráfico são, respectivamente:
Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5

As afirmativas a seguir referem-se a reações de neutralização.
I. Sais derivados de ácidos fortes com bases fortes se dissolvem na água para produzir íons H3O+ ou íons OH- .
II. A reação estequiométrica entre um ácido forte e uma base fraca produz uma solução ácida.
III. A reação estequiométrica entre um ácido fraco e uma base forte produz uma solução ácida.
IV. Sais derivados de ácidos ou bases fracas se dissolvem na água para produzir íons H3O+ ou íons OH- .
Dentre as afirmativas, estão corretas apenas
Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5
