Questões de Concurso
Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 453 questões
O calor e a entalpia de combustão do ácido benzoico foram determinados por meio de um calorímetro que opera a volume constante e cuja capacidade calorífica é de 10.000 J. A queima de 1,00 g do ácido ocasionou um aumento de 2,64 °C na temperatura do sistema. A equação que representa a combustão do ácido benzoico é apresentada a seguir.
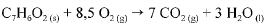
Considerando que todos os gases envolvidos na reação de combustão do ácido benzoico tenham com portamento ideal e desprezando a contribuição de líquidos e sólidos para a pressão dentro do sistema, julgue o próximo item.
O módulo da entalpia de combustão do ácido benzoico é maior
que o módulo do calor de combustão nas condições do
experimento calorimétrico realizado.
O calor e a entalpia de combustão do ácido benzoico foram determinados por meio de um calorímetro que opera a volume constante e cuja capacidade calorífica é de 10.000 J. A queima de 1,00 g do ácido ocasionou um aumento de 2,64 °C na temperatura do sistema. A equação que representa a combustão do ácido benzoico é apresentada a seguir.
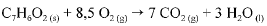
Considerando que todos os gases envolvidos na reação de combustão do ácido benzoico tenham com portamento ideal e desprezando a contribuição de líquidos e sólidos para a pressão dentro do sistema, julgue o próximo item.
Os dados fornecidos permitem concluir que o módulo do calor
de combustão a volume constante do ácido benzoico é maior
que 400 kJ/mol.
O processo ilustrado no esquema acima deverá ser
 cHº(298 K) = -3953 kJ mol -1 e se processa de acordo com a equação abaixo.
cHº(298 K) = -3953 kJ mol -1 e se processa de acordo com a equação abaixo.C6H12(g) + 9O2(g) ÷ 6CO2(g) + 6H2O( l )
A entalpia padrão de formação (
 f Hº) a 298 K para o CO2(g) é -394 kJ mol -1 e para a H2O(l) é -286 kJ mol -1 . Com base nessas informações, assinale a opção que apresenta o valor de
f Hº) a 298 K para o CO2(g) é -394 kJ mol -1 e para a H2O(l) é -286 kJ mol -1 . Com base nessas informações, assinale a opção que apresenta o valor de  f Hº(C6H12, g, 298 K).
f Hº(C6H12, g, 298 K). 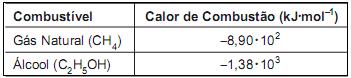
O volume, em litros, de gás natural, medido nas CNTP, que precisa ser queimado para produzir a mesma quantidade de calor que resulta da combustão de 1,0 mol de etanol é igual a
NH4 NO3 (s) -> N2O(g) + 2H2O(g)
As entalpias padrão de formação dos compostos NH4NO3 (s), N2O(g) e H2O(g) são iguais a -365,3 kJmol –1 , +81,6 kJmol –1 e -241,8 kJmol –1 , respectivamente. Sendo ΔH0 , ΔS0 e Δ?G0 , respectivamente, as variações de entalpia, entropia e energia livre padrão para a reação, a decomposição do nitrato de amônio em óxido de dinitrogênio e água apresenta
CO2(g) + H2(g) -> CO(g) + H2O(g) -> ΔH0 = +41,2 KJ.mol –1
Sabendo-se que os calores de formação padrão para H2O(g) e Fe2O3 (s) são iguais a -241,8 kJ×mol –1 e -824,8 kJ x mol –1 , respectivamente, a variação de entalpia no estado padrão para a reação
Fe2O3 (s) + 3CO(g) -> 2Fe(s) + 3CO2 (g)
será igual a
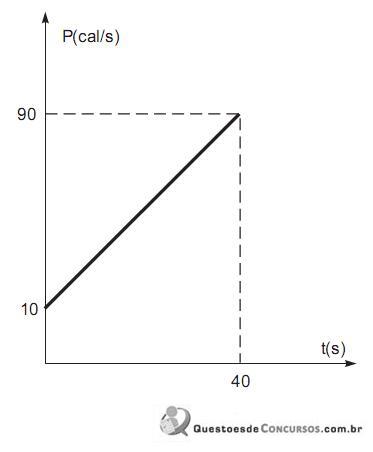
Sabe-se que, durante o intervalo de tempo representado no gráfico, todo o calor produzido pela fonte térmica é utilizado no aquecimento do bloco. Com base nessas informações, o calor específico da substância que constitui o referido corpo, em cal/g. o C, vale
A temperatura ótima para uma reação química em um dado processo é 145 °C. Antes de dar início à reação, o reator contendo o meio reacional que, no instante t = 0 se encontra a 25 °C, deve ser aquecido para, então, ser adicionado o catalisador. O sistema de aquecimento foi programado
para aquecer o reator a uma taxa média de 2 °C/minuto.
No entanto, com 15 minutos de aquecimento, o sistema apresentou um problema e passou a operar com uma taxa média de aquecimento igual a 1,5 °C/minuto.
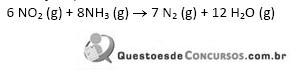
Dados os seguintes valores de entalpias padrão de formação:
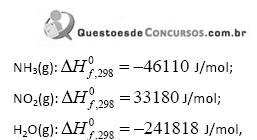
assinale a alternativa que apresenta o valor da entalpia padrão da reação a 298 K.

As lacunas são preenchidas corretamente por, respectivamente,
Em um determinado processo industrial, um tubo cilíndrico, de 0,050 m de diâmetro e de 5 m de comprimento, transporta água a uma taxa mássica de 0,3 kg/s. A temperatura da superfície externa desse tubo é mantida constante ao longo de todo o seu comprimento, sendo igual a 100 oC. A água entra no tubo a 20 oC e sai aquecida a 60 oC. Considere o número igual a, aproximadamente, 3, ln 2 igual a, aproximadamente, 0,7 e o calor específico da água igual a 4.161 J/kgK. Para essas condições, concluise que o coeficiente médio de película para o escoamento interno encontra-se, em W/m2K, na faixa de
Um trocador de calor casco-tubo (CT 1-4) de 100 tubos é usado para resfriar óleo, tendo água como fluido de resfriamento. A água escoa pelo interior dos tubos, a uma velocidade de 1 m/s, em contracorrente com o óleo. Os diâmetros dos tubos externo e interno são 0,05 m e 0,04 m, respectivamente. A água entra no trocador a 25 oC e sai a 55 oC. Considere que a massa específica da água seja 1.000 kg/m3 e despreze a resistência condutiva da parede do tubo. Considere, também, o número = 3 e ( T)ln = 30 oC, com um fator de correção de 0,9. Suponha que os coeficientes interno e externo de transferência de calor sejam iguais a 3.300 W/m2K e 4.700 W/m2K, respectivamente, e o calor específico da água, igual a 4.161 J/kgK. Para essas condições, o comprimento, em m, do tubo por passagem está na faixa de
O texto a seguir refere-se às questões de nos 34 e 35.
Quando o sistema de refrigeração de uma usina termelétrica recircula o fluido refrigerante e troca calor com a atmosfera em uma torre úmida, ocorrem perdas por evaporação e aumento das concentrações de Ca, Mg, Na, CO3, HCO3 e SO4 no líquido recirculante. Para evitar incrustações, é realizada uma purga constante deste fluido.
Essa purga pode estar contaminada por compostos que são utilizados em medidas de combate à corrosão e a incrustações. Contaminantes que resultam de medidas de combate à corrosão são os

A esse respeito, considere as afirmativas.
I – Um dos objetivos da elaboração de um fluxograma de processo é apresentar a sequência coordenada das conversões químicas e das operações unitárias, expondo, assim, os aspectos básicos do processo.
II – O gás natural não sofre conversão química no sistema de combustão da Turbina a Gás.
III – O vapor que sai da Turbina a Vapor é submetido a uma operação unitária de transferência de calor.
IV – O processo de produção de energia em uma termelétrica é realizado em bateladas.
Estão corretas APENAS as afirmativas
A figura abaixo mostra um esquema de uma termoelétrica que opera segundo um ciclo de Rankine.
O diagrama pressão versus entalpia abaixo representa o ciclo de Rankine, da termoelétrica esquematizada na figura acima. Identifique qual equipamento representa cada trecho do gráfico abaixo.
Resposta:
Um conjunto de placas metálicas é montado conforme mostrado na figura abaixo. Sabe-se que a placa A é de cobre, e as placas B, C e D são de aço inox. Existe uma taxa de geração de energia térmica uniforme e constante na placa C. A resistência de contato entre as placas é desprezível.
Qual dos perfis de temperatura abaixo melhor representa a situação descrita em regime permanente?