Questões de Concurso
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 1.107 questões
Muitas reações químicas inorgânicas podem ser classificadas em reações de síntese ou de análise ou de simples troca ou de dupla troca. Nesse contexto, relacione a COLUNA II com a COLUNA I, classificando as reações químicas.
COLUNA I
1. Reação de síntese
2. Reação de análise
3. Reação de simples troca
4. Reação de dupla troca
COLUNA II
( ) 3 H2(g) + N2(g) → 2 NH3(g)
( ) NaCl + AgNO3 → AgCl + NaNO3
( ) 2 NaN3(s) → 3 N2(g) + 2 Na(s)
( ) 2 Fe(s) + 6 HCl(aq) → 2 FeCl3(aq) + 3 H2(g)
Assinale a sequência correta.
6NH4 ClO4 (s) + 10Al (s) → 5Al2 O3 (s) + 3N2 (g) + 6HCl (g) + 9H2O (g)
Considerando que se colocou para reagir 1 kg do perclorato de amônio com 1 kg do alumínio, quanto, aproximadamente, de massa, em gramas, do óxido foi produzido na reação?
COLUNA I 1. Hidrogênio 2. Oxigênio 3. Nitrogênio 4. Flúor
COLUNA II ( ) É encontrado em duas formas moleculares gasosas, sendo que uma delas é extremamente tóxica e a outra é um não combustível pouco solúvel em água. ( ) É encontrado na forma de gás e extremamente importante na composição química das proteínas, que são moléculas presentes em todos os organismos vivos. ( ) Na forma molecular, é um gás, à temperatura ambiente, amarelo pálido e apresenta elevada reatividade. ( ) É encontrado na natureza como gás diatômico incolor e inflamável muito útil na produção de gás amoníaco.
Assinale a sequência CORRETA.
Análises químicas mostraram que um lote de carvão específico contém 2% de enxofre em massa. Quando esse carvão é queimado, o enxofre é convertido em gás dióxido de enxofre.
Considerando que nesse processo todo o dióxido de enxofre produzido da queima do carvão reagiu completamente com óxido de cálcio produzindo 2 mil toneladas de sulfito de cálcio, é correto afirmar que a massa aproximada, em toneladas, de carvão queimado é:
Um dos processos químicos industriais mais importantes que existem é a produção de amônia a partir de hidrogênio e nitrogênio. Este processo ocorre a altas temperaturas e pressões (>450ºC e 200 atm) e pode ser representado pela seguinte reação: N2(g) + 3 H2(g) → 2 NH3(g). Calcule a quantidade (em gramas) de N2 necessário para conseguir 5,0 mol de NH3 e a quantidade (em mol) de NH3 obtido a partir de 2,0 mol H2 . Dados: 1 mol de N = 14 g, 1 mol de H = 1 g.
Assinale a alternativa que possui ambas respostas corretas.
Um dos grandes problemas ambientais que ocorrem nas grandes cidades é a formação das chuvas ácidas, que ocorrem na seguinte ordem de reações:
I. Quando o oxigênio e o nitrogênio do ar reagem nos motores dos automóveis, o óxido nítrico é formado.
II. Depois de formado e lançado pelos escapamentos, este reage com o oxigênio formando o dióxido de nitrogênio.
III. Este último reage com a água, formando um dos componentes da chuva ácida.
2 Cu(NO3)2 (s) → 2 CuO(s) + 4 NO2 (g) + O2 (g)
Admitindo comportamento de gás ideal para os produtos gasosos formados, 100% de redimento e que o processo ocorre nas CNTP, o volume total, em litros, de gases formados na decomposição de 3750 g Cu(NO3)2 , corresponde a
Dados Massa molar do Cu(NO3)2 : 187,5 g mol-1 Volume molar nas CNTP: 22,4 L
"A pedra constituída
De ferro, níquel e encanto.
Até o dia de hoje
Provoca tristeza e encanto
Queremos nossa pedra de volta
De volta pro nosso canto."
Cordel: A Saga da Pedra do Bendegó.
A pedra do Bendegó foi encontrada próximo ao riacho de Bendegó, na Bahia, na cidade de Monte Claro, em 1784. Bendegó é um
As letras W, X, Y e Z representam átomos de quatro elementos e suas distribuições eletrônicas.
As letras não correspondem aos símbolos dos elementos.
Relacione os elementos às suas respectivas características.
W – 2 : 4
X – 2 : 8 : 1
Y – 2
Z – 2 : 8 : 14 : 2
( ) Gás inerte menos denso que o ar.
( ) Reage com a água, produzindo uma base e gás hidrogênio, liberando grande quantidade de calor.
( ) Metal do quarto período da tabela periódica.
( ) Ametal típico das moléculas orgânicas.
Assinale a opção que mostra a relação correta, segundo a ordem apresentada.
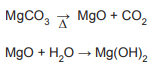
A massa de Mg(OH)2 obtida a partir de uma massa inicial de MgCO3 igual a 2,1 g é
Dados M(Mg) = 24,3 g mol-1 M(C) = 12,0 g mol-1 M(O) = 16,0 g mol-1 M(H) = 1,0 g mol-1
Considere a equação química abaixo:
Cd + 2 Ni(OH)3 => Cd(OH)2 + 2 Ni(OH)2
Após a análise dessa equação, constata-se que o
Qual é o volume ocupado por 270 g de alumínio, em cm3, e qual é o número aproximado de átomos contido nesse volume, respectivamente?
Dado Uma unidade atômica de massa corresponde a 1,66 x 10-27kg. A densidade do alumínio vale 2,7 g/cm3
Considere a reação ácido-base de Lewis entre gás clorídrico e amônia:
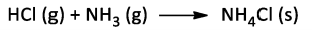
Considerando 100% de rendimento, calcule o volume mínimo da mistura equimolar dos reagentes, a 27ºC e 1 atm, de
modo que seja possível a obtenção de 10,7g do produto. Massas molares (g/mol): H = 1; N = 14; Cl = 35,5.
A decomposição do oxalato de cálcio hidratado foi estudada utilizando-se análise termo gravimétrica em recipiente aberto. Sabe-se que, com o aquecimento, sucessivas decomposições ocorrem, de acordo com as equações abaixo:
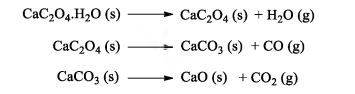
A curva de decomposição térmica esperada para esta análise é:


