Questões de Concurso
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 1.107 questões
2KNO3(s) + S(s) + 3C(s) -> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
A redução do nitrato, que consome três moles de elétrons por mol de NO3 – em meio ácido, gera o óxido nítrico, que é um agente complexante mais forte que o íon nitrato
2KNO3(s) + S(s) + 3C(s) -> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
Se o gás carbônico reagir com a água para formar o ácido carbônico, o CO2 receberá um par de elétrons da água, que é uma base de Lewis.
2KNO3(s) + S(s) + 3C(s)-> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
O nitrato reage com a água conforme a reação NO3 – + H2O -> 6 HNO3 + OH– , aumentando significativamente o pH da solução formada, haja vista que o caráter básico do OH– é mais forte que o caráter ácido do NO3 – .
A transformação de carbonato de cálcio em óxido de cálcio pode ser representada pela equação a seguir:
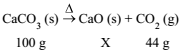
A massa, em gramas, correspondente a X é igual a
Este relato é um histórico importante sobre o elemento ferro, que pode ser obtido através da hematita (óxido férrico). Para a formação da hematita ocorre uma reação entre ferro metálico e gás oxigênio. Considerando este processo químico, quantas gramas de hematita, podem ser obtidas quando 20 mols de ferro reagem com quantidade suficiente de oxigênio? Assinale a alternativa CORRETA.
Em um laboratório de química analítica, um estudante encontrou um frasco com uma solução contendo, o seguinte rótulo: “cátion do grupo IV”. Para rotular corretamente, o aluno realizou alguns testes com alguns reagentes comuns para identificação de cátions do grupo IV e fez as seguintes observações:
1º) Ao fazer o teste utilizando solução de amônia, nenhum precipitado foi observado;
2º) Empregando uma solução de carbonato de amônio, um precipitado de cor branca foi formado, sendo este solúvel em ácidos minerais diluídos;
3º) Após utilizar ácido sulfúrico diluído, ocorreu a precipitação de um sólido branco, pesado e finamente dividido, que foi praticamente insolúvel em água.
Com base nos testes e observações do
estudante, o cátion presente no frasco mal
rotulado é?
Na figura abaixo, podemos observar o ponto de ebulição dos elementos da família 16 da tabela periódica, ligados ao hidrogênio. Um comportamento excepcional da água é notado, comparando-se seu ponto de ebulição com o das substâncias moleculares do restante do grupo.
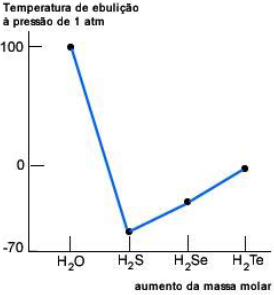
De acordo com a análise do gráfico acima, é CORRETO afirmar:
NaHCO3 + HCl → NaCl + H2O + CO2
Podemos afirmar que o grau de pureza da amostra de bicarbonato de sódio é
A reação química em um bastão de luz ou pulseiras, em geral, envolve várias etapas diferentes. Um bastão de luz comercial é feito de uma solução de peróxido de hidrogênio e de uma solução contendo éster de fenil oxalato e um corante fluorescente. Acompanhe a sequência de acontecimentos quando as duas soluções são combinadas:
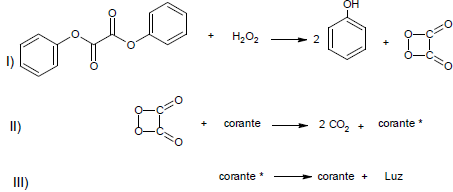
Considere as afirmativas abaixo:
I - O peróxido de hidrogênio oxida o éster de fenil oxalato, resultando em uma substância química chamada fenol e um éster de peroxiácido instável.
II - O composto de peróxi-cíclico se decompõe em dióxido de carbono; essa decomposição libera energia para o corante.
III - Os prótons dos átomos do corante migram para um nível mais alto, e depois retornam liberando energia na forma de luz.
ão CORRETOS:
“Cerca de 60% do nosso corpo é composto por água. Esse líquido precioso é fundamental para manter o sangue em circulação, controlar a temperatura e permitir inúmeras reações químicas que ocorrem a todo instante no organismo. Em dias normais, perdemos aproximadamente 2,5 litros de água pela respiração, pela urina, pelo suor e, em menor escala, pelas fezes. Claro que no verão ou após uma atividade física intensa, a perda pode ser maior.” Indique a alternativa que apresenta o número de átomos de oxigênio que são perdidos pela respiração, de acordo com o texto acima.
Dados: massas atômicas: H = 1 u; O = 16 u; N =; dágua = 1,0 g/mL 6,0 x 1023