Questões de Concurso Público Transpetro 2018 para Engenheiro Júnior - Processamento (Químico)
Foram encontradas 70 questões
Em uma etapa posterior, o reagente em excesso que não participou da reação é recuperado, sendo completamente separado do produto formado. A vazão de reagente recuperado, em kg h-1, é igual a
Dado Massas molares: C2H4 : 28 g mol-1, H2 : 2g mol-1
da = –sdT – Pdv
Utilizando-se as relações de Maxwell e a equação de estado do gás ideal (PV = RT), a relação (∂s/∂v)T para um gás ideal é
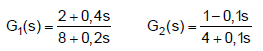
Para controle dessas malhas, um engenheiro deve levar em consideração vários fatores, como estabilidade, margem de fase, ganho, entre outros.
Nesse caso, em relação às funções de transferência G1(s) e G2(s), tem-se o seguinte:
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
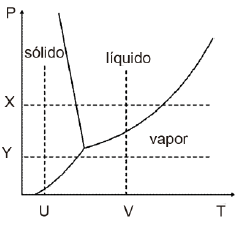
Nesse contexto, em referência ao diagrama, a passagem de