Questões de Concurso
Foram encontradas 8.687 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
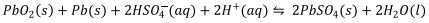
Dados: E° red (cátodo) = + 1,685 V e E° red (ânodo) = - 0,356 V
Analise as afirmações numeradas de I a IV em relação a esse tipo de bateria.
I. Os eletrodos de PbO2(s) e Pb(s) são inertes, sendo o potencial de pilha dependente apenas da concentração de ácido sulfúrico.
II. No processo de recarga da bateria ocorre redução do pH do meio aquoso.
III. O Pb(s) atua como agente redutor no processo de recarga da bateria.
IV. O processo de descarga leva a um potencial padrão de pilha de +2,041 V e a uma redução da densidade do eletrólito.
Assinale a alternativa CORRETA.
I. Na técnica de absorção atômica, os átomos da amostra absorvem parte da radiação proveniente de uma lâmpada e a luz não absorvida alcança o detector. A absorbância de um elemento químico, que é proporcional à sua concentração, pode ser determinada experimentalmente para cada pico referente ao elemento.
II. Na técnica de emissão atômica, nenhuma fonte de radiação precisa ser utilizada. A temperatura da chama e as colisões promovem os átomos da amostra a estados excitados que emitem fótons espontaneamente ao retornarem ao estado fundamental. A intensidade de emissão de um elemento químico é proporcional à sua concentração.
III. No experimento de fluorescência atômica, os átomos da amostra são irradiados com um laser e promovidos a estados excitados a partir do qual eles podem fluorescer para retornarem ao estado fundamental. Como esse processo envolve transições não-radiativas, a intensidade de emissão de um elemento não deve ser usada para determinar sua concentração.
Assinale a alternativa que contém as afirmativas CORRETAS.
Assinale a alternativa que contém, respectivamente, as concentrações dos íons cálcio e cloreto na solução diluída.
Com base nesses dados, assinale a alternativa que mostra o valor da constante Kc para essa reação.
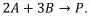
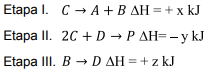
Assinale a alternativa que apresenta a expressão algébrica CORRETA para a variação de entalpia (∆H) da reação global.

Com base nesses dados, analise as afirmativas abaixo e assinale a INCORRETA.
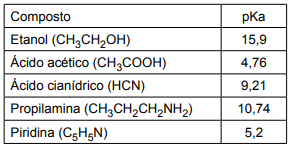
Um técnico propôs preparar cinco soluções aquosas de igual concentração, cada uma contendo um dos seguintes compostos:
- Etóxido de sódio (CH3CH2ONa)
- Acetato de sódio (CH3COONa)
- Cloreto de piridínio (C5H6NCl)
- Ácido cianídrico
- Propilamina
Com base nos dados apresentados, assinale a alternativa que contém os compostos propostos em ordem CRESCENTE do pH das soluções preparadas com eles.
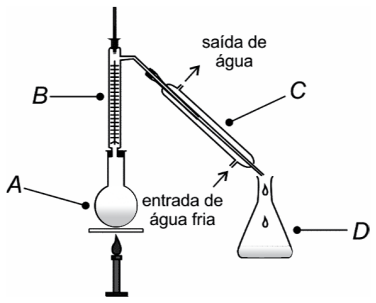
Adaptado de Theresa Knott, Wikimedia Commons, CC-BY-AS-3.0 (https://creativecommons.org/licenses/by-sa/3.0/deed.en)
É CORRETO afirmar que interações intermoleculares são predominantemente
Uma reação catalisada para produção de etanol segue o mecanismo a seguir:
Etapa I. 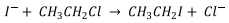
Etapa II. 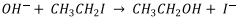
Essa reação de catálise homogênea pode ser representada esquematicamente pelo gráfico abaixo.
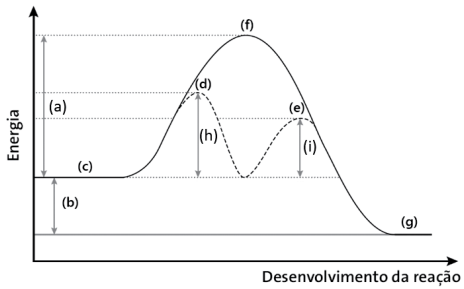
Analise as afirmativas abaixo e assinale a INCORRETA.
Assinale a alternativa que contém a resposta CORRETA.
Considerando tais condições, assinale a opção correta.
Considere que uma amostra de ar contaminada com HPA tenha sido analisada em um laboratório que possui a Norma ISO 17.025, a qual permite a rastreabilidade dos resultados, devido, principalmente, à gestão de todos os passos analíticos.
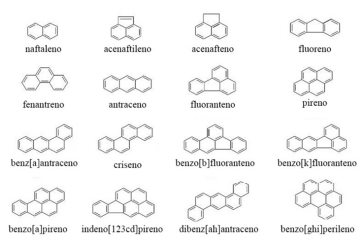
R. O. Meire et al. Aspectos ecotoxicológicos de hidrocarbonetos policíclicos aromáticos. In: Oecol. Bras., v. 11, n.º 2, p. 188-201, 2007 (com adaptações).
Tendo em vista as informações, a situação hipotética e a figura precedentes, assinale a opção correta.
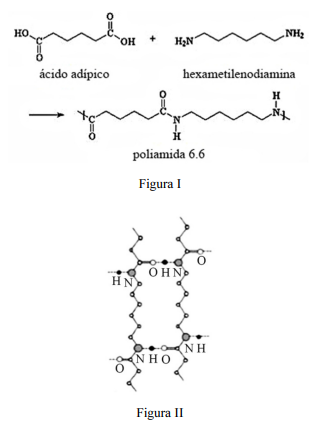
I. M. Factori. Processamento e propriedades de compósitos de poliamida 6.6 reforçada com partículas de vidro reciclado. Dissertação (Mestrado) – USP, São Paulo, 2009. Internet: (com adaptações).
Acerca desse tema, assinale a opção correta.

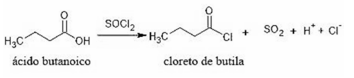
Assinale a opção correta acerca desse texto e dessa síntese.

Considere que, em uma aula prática sobre solventes orgânicos, um estudante tenha recebido de seu professor 50 mL de solução aquosa a 2% de cafeína, com a tarefa de extrair a cafeína da solução aquosa. Para isso, foram colocados à disposição desse estudante os solventes cujas fórmulas estruturais são ilustradas na figura a seguir, que também mostra a fórmula estrutural da cafeína.
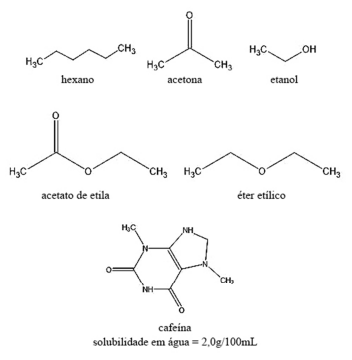
Com base na situação hipotética apresentada, para a extração da cafeína da amostra, o estudante deve escolher o(s) solvente(s)