Questões de Concurso
Comentadas para prefeitura de cuiabá - mt
Foram encontradas 2.056 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. Fruto da interação neuro-biológica-genética com o ambiente, os processos interativos exigem uma modificabilidade constante do sujeito como um todo. II. O ambiente que acolhe e desafia é a base de influência do input, assim como a sua constância e repetição exercem efeitos nas organizações e estruturas corticais, ampliando a potencialidade de crescimento da arborização dentrítica. III. O conceito de plasticidade cerebral nos mostra que não é exclusivamente em intervenções físicas ou medicamentosas que o corpo vai se adaptar às novas exigências do meio. Se essas interposições ao corpo o auxiliarem, será pela interação com o meio onde o sujeito está inserido. IV. A estimulação permanente não é fruto apenas de processos formais de escolarização ou estimulação, sequer de apenas exercícios repetitivos do corpo ou do aprender. É um processo contínuo, no qual elementos e comportamentos cotidianos, permanentemente apresentados e exigidos, estimulam a complexidade relacional e interativa.
Estão corretas as afirmativas:
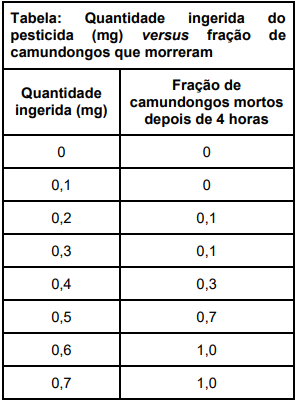
A LD50 aproximada é:
No quadro A, são encontradas algumas classificações de resíduos, no quadro B são encontradas algumas substâncias químicas consideradas perigosas.
Quadro A 1. Resíduo inflamável 2. Resíduo corrosivo 3. Resíduo Tóxico 4. Resíduo de origens específicas
Quadro B I. H2SO4 II. Hg III. Lodo de tratamento de água residual de produção de coque IV. C2H5OH
Faça uma associação entre os quadros A e B e assinale a alternativa correta.
I. Meios de culturas sintéticos são aqueles que a composição química é qualitativa e quantitativamente conhecida. II. Os meios seletivos servem para suprimir algum microrganismo indesejado ou favorecer algum de interesse. III. Os meios diferenciais são aqueles que conferem características especiais às colônias. Em situações normais, elas seriam idênticas.
Assinale alternativa correta.
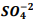 seguindo a reação: BαSO4(s) ⇔
seguindo a reação: BαSO4(s) ⇔ 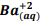 +
+ 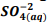 , onde Kps = [ Bα+2] [
, onde Kps = [ Bα+2] [ 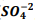 ] = 1, 1 x10−10. Verifica-se que:
] = 1, 1 x10−10. Verifica-se que: I. A partir da concentração de
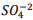 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4. Assinale a alternativa correta:
CH3CO2H(aq) + OH-(aq) ⇔ CH3CO2-(aq) + H2O(l)
Para atingir o ponto de equivalência foram gastos 5,3 x10-6 M de OH- e o pH ficou em 8,72.
Analise as afirmativas a seguir e dê valores Verdadeiro (V) ou Falso (F).
( ) No ponto de equivalência o pH é neutro. ( ) No ponto de equivalência, o pH é ligeiramente básico, porém a partir desse ponto, a adição de mais NaOH torna a solução substancialmente básica.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
A equação que melhor representa a constante de equilíbrio para esse tampão é:
I. Duas substâncias devem ser utilizadas, um ácido capaz de reagir com os íons OH- adicionados e uma base capaz de reagir com os íons H3O+ adicionados. II. Soluções-tampão podem ser preparadas a partir de um par ácido forte e seu sal conjugado. III. A dupla conjugada do sistema tampão do ácido acético é: CH3COOH ⇔ CH3COO-.
Estão corretas as afirmativas:
Um par de aminoácido é separado em uma coluna onde a fase estacionária está saturada com água e o solvente transportados é o metanol. Os aminoácidos são:
HOOC-CHNH2-CH2-OH e HOOC-CHNH2-CH3.
Assinale a alternativa que melhor representa o que acontece.
X KO2(s) + Y CO2(g) ⇔ W K2CO3(s) + Z O2(g).
Calcule a massa de KO2 necessária para reagir com 50 l de CO2 a 25°C e 1,0 atm. A massa molar do KO2 é 71,1 g/mol. Considere o volume molar 24,5l/mol.
Assinale a alternativa que contém os valores de X, Y, W e Z e a massa de KO2 consumida na reação.
Reação: 6CO2(g) + 6H2O(l) ⇔ C6H12O6(g) + 6O2(g).
Considere massa molecular da glicose = 180 g/mol e volume molar = 24,5 l/mol.
Assinale a alternativa que contém a resposta correta.
Assinale a alternativa que contenha a concentração no equilíbrio de H2(g), I2(g) e HI respectivamente:
I. Com o aumento da pressão, a reação deslocou-se na formação dos reagentes. II. Com o volume do recipiente sendo diminuído, a reação deslocou-se no sentido do produto. III. Quando adicionado calor, a reação favoreceu mais a formação do produto. IV. Com a adição de H2, a reação tende a formar mais produto. V. Com a adição de CO, a reação é deslocada para formar mais reagentes.
Estão corretas as afirmativas:
5 µg g-1, 10 µg g-1, 20 µg g-1, 25 µg g-1 e 50 µg g-1.
Para isso, esse técnico partiu de uma solução estoque de 1 mg g-1.
Assinale a alternativa que demonstra a quantidade mínima de solução estoque que é necessário para se conseguir preparar todas as amostras sem ter que fazer uma diluição intermediária, sendo que o volume final de cada uma das amostras foi 10 ml.
I. Misturando-se as soluções Fe2(SO4)3 e hidróxido de sódio, forma-se um precipitado. II. Misturando as soluções AgNO3 e carbonato de potássio, forma-se um precipitado. III. Misturando as soluções MgCO3 e sulfato de sódio, forma-se um precipitado.
A partir da análise das asserções anteriores, assinale a alternativa correta.