Questões de Vestibular Sobre química
Foram encontradas 6.520 questões
Obrigatório desde 1997, o componente reduz as emissões
provenientes da queima de combustível
Na época de frio, a qualidade do ar tende a piorar e, para não tornar a situação ainda mais crítica, é preciso atenção ao catalisador do veículo. A peça pode transformar mais de 90% dos gases tóxicos em derivados menos poluentes. [...]
O principal indício de problemas no catalisador é a perda de potência. “Combustível adulterado provoca a ineficiência da reação química que faz a catálise, o que afeta o rendimento", explica o diretor Associação de Engenharia Automotiva (AEA), Alfredo Castelli.
A cor da fumaça que sai pelo escapamento não está relacionada a defeitos na peça. Nesse caso, indica que há algo de errado com o motor.
Thais Villaça
O Estado de São Paulo, 28.05.14
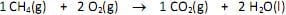
Nessas condições, na queima de 32 mg de metano, será lançada, pelo escapamento do veículo, uma massa de gás carbônico igual a
Dados: H = 1, C = 12, O = 16
Obrigatório desde 1997, o componente reduz as emissões
provenientes da queima de combustível
Na época de frio, a qualidade do ar tende a piorar e, para não tornar a situação ainda mais crítica, é preciso atenção ao catalisador do veículo. A peça pode transformar mais de 90% dos gases tóxicos em derivados menos poluentes. [...]
O principal indício de problemas no catalisador é a perda de potência. “Combustível adulterado provoca a ineficiência da reação química que faz a catálise, o que afeta o rendimento", explica o diretor Associação de Engenharia Automotiva (AEA), Alfredo Castelli.
A cor da fumaça que sai pelo escapamento não está relacionada a defeitos na peça. Nesse caso, indica que há algo de errado com o motor.
Thais Villaça
O Estado de São Paulo, 28.05.14
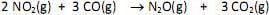
Em um experimento investigativo sobre a velocidade dessa reação, foram realizados três experimentos nas condições mostradas na tabela.
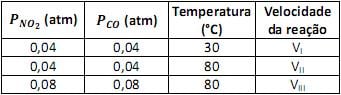
Pode-se prever, considerando apenas os fatores mostrados acima, que a relação entre as velocidades das reações nessas três experiências será
Obrigatório desde 1997, o componente reduz as emissões
provenientes da queima de combustível
Na época de frio, a qualidade do ar tende a piorar e, para não tornar a situação ainda mais crítica, é preciso atenção ao catalisador do veículo. A peça pode transformar mais de 90% dos gases tóxicos em derivados menos poluentes. [...]
O principal indício de problemas no catalisador é a perda de potência. “Combustível adulterado provoca a ineficiência da reação química que faz a catálise, o que afeta o rendimento", explica o diretor Associação de Engenharia Automotiva (AEA), Alfredo Castelli.
A cor da fumaça que sai pelo escapamento não está relacionada a defeitos na peça. Nesse caso, indica que há algo de errado com o motor.
Thais Villaça
O Estado de São Paulo, 28.05.14
RS não deve chegar à costa Catarinense
Mancha se alastrou a uma área equivalente
a 100 campos de futebol
O Litoral catarinense não deve ser afetado com o derramamento de óleo que aconteceu na última
quinta-feira, em Tramandaí (RS), de acordo com o Instituto Nacional do Meio Ambiente (Ibama). Foram cerca de 1,2 mil litros de óleo que caíram no mar, próximo a Tramandaí, no Litoral Norte do Rio Grande do Sul. [...]
A mancha de óleo se alastrou pelo mar e chegou a ocupar uma área equivalente a 100 campos
de futebol. [...] O volume estimado de óleo derramado é de 1,2 m³.
Diário Catarinense, 27.01.2012. Texto adaptado.
Disponível em: http://diariocatarinense.clicrbs.com.br/sc/geral/n...
ento-de-oleo-no-litoral-norte-do-rs-nao-deve-chegar-a-costa-catarinense- 3645427.html
Acesso em 04.07.2014

RS não deve chegar à costa Catarinense
Mancha se alastrou a uma área equivalente
a 100 campos de futebol
O Litoral catarinense não deve ser afetado com o derramamento de óleo que aconteceu na última
quinta-feira, em Tramandaí (RS), de acordo com o Instituto Nacional do Meio Ambiente (Ibama). Foram cerca de 1,2 mil litros de óleo que caíram no mar, próximo a Tramandaí, no Litoral Norte do Rio Grande do Sul. [...]
A mancha de óleo se alastrou pelo mar e chegou a ocupar uma área equivalente a 100 campos
de futebol. [...] O volume estimado de óleo derramado é de 1,2 m³.
Diário Catarinense, 27.01.2012. Texto adaptado.
Disponível em: http://diariocatarinense.clicrbs.com.br/sc/geral/n...
ento-de-oleo-no-litoral-norte-do-rs-nao-deve-chegar-a-costa-catarinense- 3645427.html
Acesso em 04.07.2014

A fórmula molecular que representa o composto 4-metil-3-heptanona é:
Considerando essas características, assinale a alternativa que representa o número de prótons, elétrons e nêutrons do íon Cr+3 respectivamente.
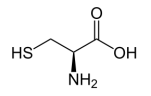
Nesta fórmula representando o aminoácido cisteína, está presente o grupo funcional:
Responda à questão com base na tabela abaixo sobre o rótulo da garrafa de uma determinada marca de refrigerante.

* Valores Diários com base numa dieta de 2 000 kcal ou 8 400 kJ
O carboidrato de que trata o rótulo é a sacarose, cuja fórmula química é mostrada abaixo.
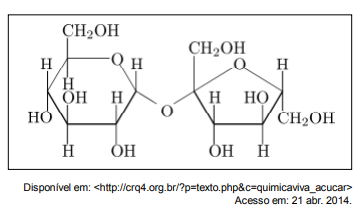
Com relação à fórmula estrutural deste açúcar, podemos afirmar que
Responda à questão com base na tabela abaixo sobre o rótulo da garrafa de uma determinada marca de refrigerante.

* Valores Diários com base numa dieta de 2 000 kcal ou 8 400 kJ
Responda à questão com base na tabela abaixo sobre o rótulo da garrafa de uma determinada marca de refrigerante.

* Valores Diários com base numa dieta de 2 000 kcal ou 8 400 kJ
H3C-NH2(g) + H2O(l) → H3C-NH3+ (aq) + OH- (aq)
De acordo com a reação química equacionada e para completar as lacunas acima se deve utilizar a seguinte sequência:
Considere o sistema em equilíbrio a 25°C e 1 atm que representa a queima ou combustão do metanol líquido:
2CH3OH (l) + 3 O2 (g) ⇄ 2CO2(g) + 4H2O(l) H = -1452 kJ
Assinale a alternativa VERDADEIRA:

II) O ácido nítrico em água tem como base conjugada o íon nitrato, NO .
III) Para cada litro de solução de ácido nítrico obtido tem-se 980 g deste ácido dissolvidos.
IV) A concentração da solução aquosa de ácido nítrico obtido é de 15,6 mol/l.
V) Por meio de uma destilação é possível elevar o teor de ácido nítrico na solução obtida.
A sequência correta que corresponde, respectivamente, à questão é

II) A amônia é um composto gasoso de caráter básico.
III) O ácido nítrico é um oxiácido monoprótico.
IV) Na amônia, o nitrogênio tem número de oxidação +3.
V) A reação que ocorre na etapa 6 é homogênea.
A sequência correta que corresponde, respectivamente, à questão é

II) A etapa 2 de separação dos gases ocorre por liquefação seguida de destilação fracionada.
III) O processo Haber-Bosch consiste em uma reação de síntese total.
IV)Asoma dos coeficientes mínimos e inteiros da equação na etapa 4 é 19.
V) A etapa 4 é uma reação catalítica de oxirredução.
A sequência correta que corresponde, respectivamente, à questão é
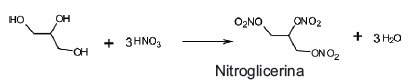
A nitração em escala industrial também é realizada na presença de uma mistura dos ácidos nítrico e sulfúrico, conhecida como mistura sulfonítrica. Sobre a reação de nitração da glicerina e as substâncias que agem como reagentes e seus produtos é correto afirmar que