Questões de Vestibular Sobre química
Foram encontradas 6.520 questões
I. 2H2S(g) + H2SO3(aq) ↠ 3S(s) + 3H2O(l) II. H2S(g) + 2H+(aq) + SO4 2-(aq) ↠ SO2(g) + S(s) + 2H2O(l) III. H2S(g) + Pb(s) ↠ PbS(s) + H2(g) IV. 2H2S(g) + 4Ag(s) + O2(g) ↠ 2Ag‚S(s) + 2H2O(l)
Nas reações representadas pelas equações acima, o sulfeto de hidrogênio é agente redutor em:
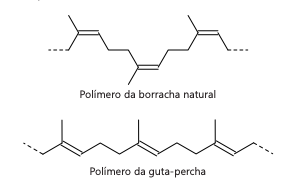
A perda da elasticidade do polímero de isopreno nos materiais apresentados se deve a uma alteração que o transforma em seu isômero:
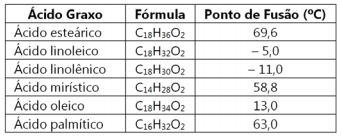
Considerando as informações fornecidas, dentre os ácidos graxos apresentados, aqueles que devem ser encontrados em maior quantidade em óleos vegetais são:
O acendimento instantâneo do palito de fósforo antigo era possível por que a reação entre fósforo branco e oxigênio possui:
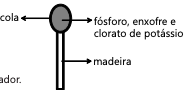
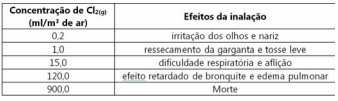
Considere que uma dona de casa tenha produzido 0,01 mol de gás cloro pela mistura de alvejante com outro produto em um cômodo fechado com as dimensões de 2,0m x 3,0m x 2,0m. Após certo período de exposição, a dona de casa terá como mais grave efeito dessa exposição:
Dado: volume molar do gás, na temperatura do cômodo = 24 L/mol.
Considere a reação abaixo, que mostra como se dá a produção do cobre a partir da calcosita, minério rico em sulfeto de cobre (Cu2S):
Cu2S + O2 ↠ 2 Cu + SO2
O processo químico pelo qual o metal é obtido, e um problema ambiental que pode estar associado à sua obtenção são, respectivamente:
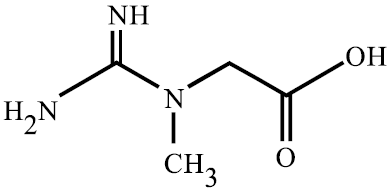
I. Possui em sua estrutura ácido e base segundo a teoria de Bronsted-Lowry.
II. Apresenta os grupos funcionais amina primária, secundária e ácido carboxílico.
III. Possui dois carbonos que apresentam geometria trigonal plana.
Está correto o que se afirma em
Fe(s) + HCℓ(aq) → FeCℓ2(aq) + H2(g)
Assim, pode-se afirmar que as massas de ferro na amostra e de hidrogênio liberada por essa reação são, respectivamente,
Dados: massas molares (g.mol-1): H = 1, Cℓ = 35,5 e Fe = 56
Solução Temperatura de ebulição (ºC)
A 104,2
B 106,7
I. A pressão de vapor de ambas as soluções é menor do que a pressão de vapor da água pura. II. A solução A apresenta menor concentração de sal em relação à concentração salina da solução B. III. As forças de interação intermoleculares na solução B apresentam maior intensidade do que as forças de interação existentes, tanto na solução A como na água.
É correto dizer que
Dado: log 2 = 0,3