Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Na natureza, os metais são encontrados principalmente na forma de óxidos, carbonatos, sulfatos, sulfetos e fosfatos. Para extrair os metais desses minérios, é necessário aplicar processos metalúrgicos, hidrometalúrgicos ou eletrometalúrgicos. Na tabela a seguir, estão listados alguns metais, com seus respectivos minérios e seus principais compostos.
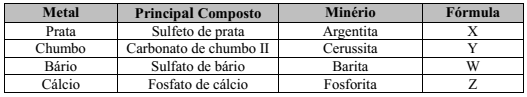
Assinale a alternativa que contenha, respectivamente, as fórmulas X, Y, W e Z.
O biodiesel substitui total ou parcialmente o óleo diesel de petróleo em motores automotivos. O seu consumo contribui para a redução da poluição atmosférica, já que o biodiesel não contém enxofre em sua composição, além de gerar alternativas de empregos em áreas geográficas menos propícias para outras atividades econômicas. Tal combustível é obtido a partir da reação química entre óleos vegetais, como demonstrada na fórmula abaixo, ou gorduras, com um álcool, na presença de um catalisador, produzindo um novo éster (biodiesel) e a glicerina (C3H8O3). Admitindo uma reação entre 319 gramas de óleo de soja (massa molar 638g/mol) e metanol em quantidade suficiente, a massa formada de glicerina (massa molar 92 g/mol), numa reação com 50% de rendimento, é de
C39H74O6 + 3 CH3OH ↔ C3H8O3 + 3 C13H26O2
O rótulo de uma determinada água mineral apresenta uma lista relativamente extensa de sais dissolvidos e também de características físico-químicas como: pH, temperatura da água na fonte, condutividade elétrica e resíduo de evaporação. Uma água mineral com pH 6,29 a 25ºC apresenta a concentração de alguns sais em mg/L: cloreto de sódio (NaCl) 1,17; bicarbonato de sódio (NaHCO3) 1,68; nitrato de sódio (NaNO3) 1,7 e sulfato de cálcio(CaSO4)1,36. Com relação aos aspectos observados, assinale a alternativa CORRETA em relação à referida água mineral. Dados: massa molar (g/mol) Na = 23, Cl = 35,5, H = 1, C = 12, O = 16, Ca = 40 e S = 32.
I. CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ΔHo= −212,8kcalmol−1 II. CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
( ) A partir dos métodos do calor de formação e da energia de ligação, obtêm-se os mesmos valores de variação de entalpia da reação expressa na equação química I. ( ) A queima de alcanos só é exotérmica se os produtos forem gasosos. ( ) A reação expressa na equação química II é mais exotérmica que aquela expressa na equação química I. ( ) O calor da reação expressa na equação química II equivale à soma do calor de vaporização da água com o calor envolvido na reação expressa na equação química I.
A alternativa que contém a sequência correta, de cima para baixo, é a
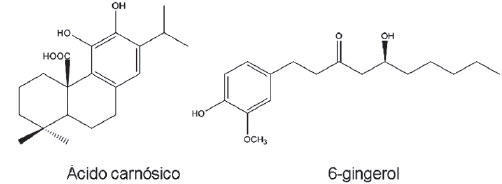
Os recursos naturais continuam sendo importantes fontes de substâncias e precursores com grande potencial terapêutico, não apenas pelo grande número de espécies vegetais com propriedades medicinais inexploradas, mas principalmente pela variedade de metabólitos primários e secundários por elas sintetizados. Os principais compostos antioxidantes extraídos do alecrim e do gengibre são o ácido carnósico e o 6-gingerol, respectivamente, conforme estrutura química.
Sobre a química dessas substâncias, é correto afirmar:

Quem tem medo da radioatividade?
Como herança da destruição causada pela explosão das bombas atômicas ao fim da Segunda Guerra, a energia nuclear ganhou uma reputação difícil de mudar. Um novo livro desmistifica a radioatividade e aponta as vantagens e desvantagens de seu uso. Foram mais de cem mil mortos imediatamente após a explosão das bombas nucleares em Hiroshima e Nagasaki, em agosto de 1945. Ironicamente, as mesmas propriedades do átomo capazes de causar tamanha destruição também podiam salvar vidas se empregadas no tratamento de câncer. A radioterapia, o exame de raios-X e o marca-passo artificial são exemplos de aplicações pacíficas da radioatividade. Para muitos, no entanto, a função da energia nuclear se resume a dizimar vidas. O temor suscitado pelos cogumelos atômicos se espalhou pelo mundo e ecoa até hoje devido à falta de informações precisas sobre o tema.
O risco de acidentes e a destinação do lixo nuclear
são tratados de forma esclarecedora, ao se
destacarem as aplicações da tecnologia nuclear
na medicina molecular, na agricultura, na
indústria e na datação de artefatos na
arqueologia, e tudo que envolve a geração de
energia nas usinas nucleares, como alternativa à
queima de combustíveis fósseis das usinas
termelétricas de gás e carvão e ao impacto
socioambiental das hidrelétricas. Os fantasmas
associados às usinas nucleares – o risco de
acidentes e a destinação do lixo nuclear – são
tratados de forma esclarecedora pelos
pesquisadores sobre a radioatividade. (VENTURA,
2017);

Quem tem medo da radioatividade?
Como herança da destruição causada pela explosão das bombas atômicas ao fim da Segunda Guerra, a energia nuclear ganhou uma reputação difícil de mudar. Um novo livro desmistifica a radioatividade e aponta as vantagens e desvantagens de seu uso. Foram mais de cem mil mortos imediatamente após a explosão das bombas nucleares em Hiroshima e Nagasaki, em agosto de 1945. Ironicamente, as mesmas propriedades do átomo capazes de causar tamanha destruição também podiam salvar vidas se empregadas no tratamento de câncer. A radioterapia, o exame de raios-X e o marca-passo artificial são exemplos de aplicações pacíficas da radioatividade. Para muitos, no entanto, a função da energia nuclear se resume a dizimar vidas. O temor suscitado pelos cogumelos atômicos se espalhou pelo mundo e ecoa até hoje devido à falta de informações precisas sobre o tema.
O risco de acidentes e a destinação do lixo nuclear
são tratados de forma esclarecedora, ao se
destacarem as aplicações da tecnologia nuclear
na medicina molecular, na agricultura, na
indústria e na datação de artefatos na
arqueologia, e tudo que envolve a geração de
energia nas usinas nucleares, como alternativa à
queima de combustíveis fósseis das usinas
termelétricas de gás e carvão e ao impacto
socioambiental das hidrelétricas. Os fantasmas
associados às usinas nucleares – o risco de
acidentes e a destinação do lixo nuclear – são
tratados de forma esclarecedora pelos
pesquisadores sobre a radioatividade. (VENTURA,
2017);
Sobre esse processo, é correto afirmar:

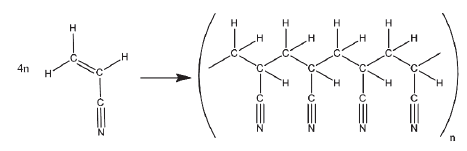
Com base no texto e na equação que ilustra a conversão de acrilonitrila no polímero de poliacrilonitrila, é correto afirmar:
Para explicar a produção de dióxido de carbono, as seguintes afirmações foram feitas.
I. Tanto o fermento químico quanto o biológico reagem com os carboidratos presentes na massa culinária, sendo o dióxido de carbono um dos produtos dessa reação.
II. O hidrogenocarbonato de sódio, presente no fermento químico, pode se decompor com o aquecimento, ocorrendo a formação de carbonato de sódio (Na2CO3), água e dióxido de carbono.
III. As leveduras, que formam o fermento biológico, metabolizam os carboidratos presentes na massa culinária, produzindo, entre outras substâncias, o dióxido de carbono.
IV. Para que ambos os fermentos produzam dióxido de carbono, é necessário que a massa culinária seja aquecida a temperaturas altas (cerca de 200 ºC), alcançadas nos fornos domésticos e industriais.
Dessas afirmações, as que explicam corretamente a produção de dióxido de carbono pela adição de fermento à massa culinária são, apenas,
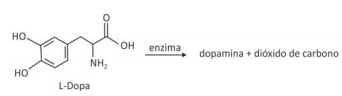
Sendo assim, a fórmula estrutural da dopamina é :
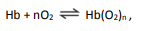
em que Hb representa tanto a hemoglobina do adulto quanto a hemoglobina fetal.
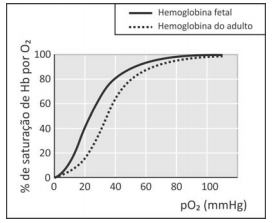
A figura mostra a porcentagem de saturação de Hb por O2 em função da pressão parcial de oxigênio no sangue humano, em determinado pH e em determinada temperatura.
A porcentagem de saturação pode ser entendida como :
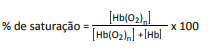
Com base nessas informações, um estudante fez as seguintes afirmações:
I. Para uma pressão parcial de O2 de 30 mmHg, a hemoglobina fetal transporta mais oxigênio do que a hemoglobina do adulto.
II. Considerando o equilíbrio de transporte de oxigênio, no caso de um adulto viajar do litoral para um local de grande altitude, a concentração de Hb em seu sangue deverá aumentar, após certo tempo, para que a concentração de Hb(O2)n seja mantida.
III. Nos adultos, a concentração de hemoglobina associada a oxigênio é menor no pulmão do que nos tecidos.
É correto apenas o que o estudante afirmou em
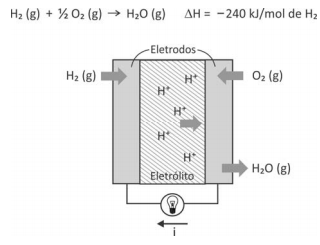
A corrente elétrica (i), em ampère (coulomb por segundo), gerada por uma célula a combustível que opera por 10 minutos e libera 4,80 kJ de energia durante esse período de tempo , é
Sob certas condições, tanto o gás flúor quanto o gás cloro
podem reagir com hidrogênio gasoso, formando,
respectivamente, os haletos de hidrogênio HF e HCl,
gasosos. Pode-se estimar a variação de entalpia 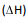 de cada
uma dessas reações, utilizando-se dados de energia de
ligação. A tabela apresenta os valores de energia de ligação
dos reagentes e produtos dessas reações a 25 ºC e 1 atm.
de cada
uma dessas reações, utilizando-se dados de energia de
ligação. A tabela apresenta os valores de energia de ligação
dos reagentes e produtos dessas reações a 25 ºC e 1 atm.

Com base nesses dados, um estudante calculou a variação
de entalpia 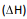 de cada uma das reações e concluiu,
corretamente, que, nas condições empregadas,
de cada uma das reações e concluiu,
corretamente, que, nas condições empregadas,
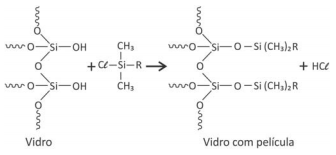
Das alternativas apresentadas, a que representa o melhor material a ser aplicado ao vidro, de forma a evitar o acúmulo de água,
I. Se tivesse ocorrido apenas combustão incompleta, restaria propano no reator. II. Para que todo o propano reagisse, considerando a combustão completa, seriam necessários, no mínimo, 750 L de ar. III. É provável que, nessa combustão, tenha se formado fuligem.
Está correto apenas o que se afirma