Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Se o jogador não se organizar em relação à sua dieta e suplementação, poderá perder força, rendimento e velocidade dentro do campo.
Uma alimentação balanceada deve apresentar alguns itens, como:
I. Carboidratos II. Proteínas III. Gorduras IV. Vitaminas e Minerais
(http://www.anutricionista.com/como-deve-ser-o-cardapio-de-um-jogador-de-futebol.html Acesso em: 14.02.2014. Adaptado)
Considerando os quatro itens mencionados no texto, assinale a alternativa que exemplifica cada um deles, respectivamente.
Feromônios são substâncias químicas secretadas pelos indivíduos que permitem a comunicação com outros seres vivos. Nos seres humanos, há evidências de que algumas substâncias, como o androstenol e a copulina, atuam como feromônios. <http://tinyurl.com/hqfrxbb> Acesso em: 17.09.2016. Adaptado.
As fórmulas estruturais do androstenol e da copulina encontram-se representadas
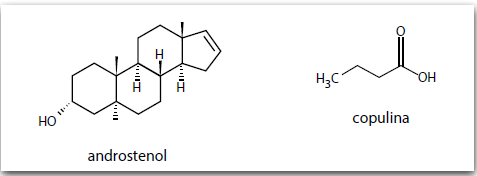
As funções orgânicas oxigenadas encontradas no androstenol e na copulina são, respectivamente,
Um dos piores acidentes nucleares de todos os tempos completa 30 anos em 2016. Na madrugada do dia 25 de abril, o reator número 4 da Estação Nuclear de Chernobyl explodiu, liberando uma grande quantidade de Sr–90 no meio ambiente que persiste até hoje em locais próximos ao acidente. Isso se deve ao período de meia-vida do Sr–90, que é de aproximadamente 28 anos. O Sr–90 é um beta emissor, ou seja, emite uma partícula beta, transformando-se em Y–90. A contaminação pelo Y–90 representa um sério risco à saúde humana, pois esse elemento substitui com facilidade o cálcio dos ossos, dificultando a sua eliminação pelo corpo humano. <http://tinyurl.com/jzljzwc> Acesso em: 30.08.2016. Adaptado.
Em 2016, em relação à quantidade de Sr–90 liberada no acidente, a quantidade de Sr–90 que se transformou em Y–90 foi, aproximadamente, de


4 Li (s) + O2 (g) → 2 Li2O (s)
A massa de lítio necessária para reagir completamente com 3,2 kg de oxigênio é, em quilogramas,
Massas molares: Li: 7 g/mol O: 16 g/mol

Lise Meitner, nascida na Áustria em 1878 e doutora em Física pela Universidade de Viena, começou a trabalhar, em 1906, com um campo novo e recente da época: a radioquímica. Meitner fez trabalhos significativos sobre os elementos radioativos (descobriu o protactínio, Pa, elemento 91), porém sua maior contribuição à ciência do século XX foi a explicação do processo de fissão nuclear. A fissão nuclear é de extrema importância para o desenvolvimento de usinas nucleares e bombas atômicas, pois libera grandes quantidades de energia. Neste processo, um núcleo de U–235 (número atômico 92) é bombardeado por um nêutron, formando dois núcleos menores, sendo um deles o Ba–141 (número atômico 56) e três nêutrons. Embora Meitner não tenha recebido o prêmio Nobel, um de seus colaboradores disse: “Lise Meitner deve ser honrada como a principal mulher cientista deste século”.
Fonte dos dados: KOTZ, J. e TREICHEL, P. Química e Reações Químicas. Rio de Janeiro. Editora LTC,1998. Adaptado. FRANCO, Dalton. Química, Cotidiano e Transformações. São Paulo. Editora FTD,2015. Adaptado.
O número atômico do outro núcleo formado na fissão nuclear mencionada no texto é
Leia o texto para responder a questão.
De onde vem o cheiro de carro novo?
De acordo com o gerente de uma montadora de veículos, o cheiro é composto por uma combinação de vários tipos de substâncias químicas usadas na fabricação do veículo, incluindo solventes, plásticos, colas, tecidos e borracha. Porém, muitas delas são altamente tóxicas, porque contêm Compostos Orgânicos Voláteis (COVs) em sua composição, como benzeno, tolueno e formol, que podem ser letais dependendo da quantidade. Eles acabam escapando e impregnando o ar, porque não requerem altas temperaturas para evaporarem.
<http://tinyurl.com/y8ucob6c> Acesso em: 13.11.2017. Adaptado.
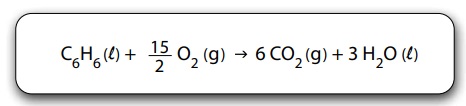
A entalpia de combustão do benzeno pode ser determinada conhecendo-se os valores das entalpias de formação do gás carbônico, assim como da água e do benzeno líquidos.
A tabela apresenta os valores de entalpia de formação de algumas substâncias nas condições padrão.
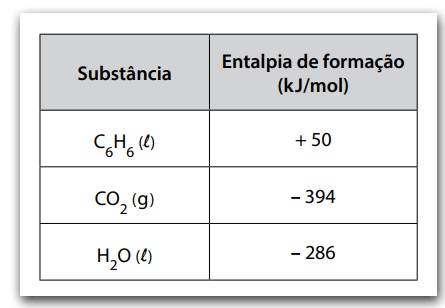
A entalpia de combustão completa do benzeno, em kJ/mol, é
Leia o texto para responder a questão.
De onde vem o cheiro de carro novo?
De acordo com o gerente de uma montadora de veículos, o cheiro é composto por uma combinação de vários tipos de substâncias químicas usadas na fabricação do veículo, incluindo solventes, plásticos, colas, tecidos e borracha. Porém, muitas delas são altamente tóxicas, porque contêm Compostos Orgânicos Voláteis (COVs) em sua composição, como benzeno, tolueno e formol, que podem ser letais dependendo da quantidade. Eles acabam escapando e impregnando o ar, porque não requerem altas temperaturas para evaporarem.
<http://tinyurl.com/y8ucob6c> Acesso em: 13.11.2017. Adaptado.
Leia o texto para responder a questão.
Estima-se que cerca de um bilhão de pessoas sofram com a falta de água potável no mundo. Para tentar combater esse tipo de problema, uma empresa desenvolveu um purificador de água distribuído na forma de um sachê que é capaz de transformar dez litros de água contaminada em dez litros de água potável. Os principais componentes do sachê são sulfato de ferro (III) e hipoclorito de cálcio.
ara purificar a água, o conteúdo do sachê deve ser despejado em um recipiente com dez litros de água não potável. Depois é preciso mexer a mistura por cinco minutos, para ocorrer a união dos íons cálcio (Ca2+) e dos íons sulfato (SO4 2- ), produzindo sulfato de cálcio, que vai ao fundo do recipiente juntamente com a sujeira. Em seguida, a água deve ser passada por um filtro, que pode ser até mesmo uma camiseta de algodão limpa. Para finalizar, deve-se esperar por 20 minutos para que ocorra a ação bactericida dos íons hipoclorito, CℓO1–.
Assim, em pouco tempo, uma água barrenta ou contaminada se transforma em água limpa para o consumo.
<http://tinyurl.com/y7gdw9qx> Acesso em: 13.11.2017. Adaptado.
Leia o texto para responder a questão.
Estima-se que cerca de um bilhão de pessoas sofram com a falta de água potável no mundo. Para tentar combater esse tipo de problema, uma empresa desenvolveu um purificador de água distribuído na forma de um sachê que é capaz de transformar dez litros de água contaminada em dez litros de água potável. Os principais componentes do sachê são sulfato de ferro (III) e hipoclorito de cálcio.
ara purificar a água, o conteúdo do sachê deve ser despejado em um recipiente com dez litros de água não potável. Depois é preciso mexer a mistura por cinco minutos, para ocorrer a união dos íons cálcio (Ca2+) e dos íons sulfato (SO4 2- ), produzindo sulfato de cálcio, que vai ao fundo do recipiente juntamente com a sujeira. Em seguida, a água deve ser passada por um filtro, que pode ser até mesmo uma camiseta de algodão limpa. Para finalizar, deve-se esperar por 20 minutos para que ocorra a ação bactericida dos íons hipoclorito, CℓO1–.
Assim, em pouco tempo, uma água barrenta ou contaminada se transforma em água limpa para o consumo.
<http://tinyurl.com/y7gdw9qx> Acesso em: 13.11.2017. Adaptado.
Leia o texto para responder a questão.
Estima-se que cerca de um bilhão de pessoas sofram com a falta de água potável no mundo. Para tentar combater esse tipo de problema, uma empresa desenvolveu um purificador de água distribuído na forma de um sachê que é capaz de transformar dez litros de água contaminada em dez litros de água potável. Os principais componentes do sachê são sulfato de ferro (III) e hipoclorito de cálcio.
ara purificar a água, o conteúdo do sachê deve ser despejado em um recipiente com dez litros de água não potável. Depois é preciso mexer a mistura por cinco minutos, para ocorrer a união dos íons cálcio (Ca2+) e dos íons sulfato (SO4 2- ), produzindo sulfato de cálcio, que vai ao fundo do recipiente juntamente com a sujeira. Em seguida, a água deve ser passada por um filtro, que pode ser até mesmo uma camiseta de algodão limpa. Para finalizar, deve-se esperar por 20 minutos para que ocorra a ação bactericida dos íons hipoclorito, CℓO1–.
Assim, em pouco tempo, uma água barrenta ou contaminada se transforma em água limpa para o consumo.
<http://tinyurl.com/y7gdw9qx> Acesso em: 13.11.2017. Adaptado.
As impressões digitais são desenhos que se formam quando as papilas, presentes nas pontas dos dedos, tocam uma superfície lisa. Nesse contato, ocorre depósito de vestígios papilares visíveis ou ocultos. Os vestígios visíveis podem ser observados se a mão que os contém estiver suja de tinta ou de sangue. Já os ocultos resultam dos vestígios de suor que os dedos deixam em um determinado local.
Há vários reagentes que podem ser usados para tornar visíveis vestígios papilares ocultos. Uma substância bastante utilizada nesse caso é a ninidrina, que reage com um dos componentes do suor formando um produto colorido. <http://tinyurl.com/y99dvkto> Acesso em: 13.11.2017. Adaptado.
A equação química simplificada que representa a reação que ocorre entre a ninidrina e uma das moléculas presentes no suor (apresentada na equação como composto X) é
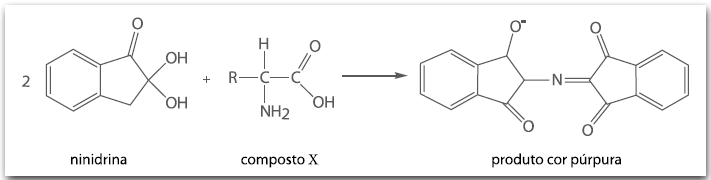
O composto X que reage com a ninidrina apresenta as funções orgânicas
Leia o texto para responder a questão.
Em seu livro Tratado Elementar de Química, publicado em 1789, Antonie Lavoisier estabeleceu uma nova nomenclatura para diversas substâncias químicas. Alguns exemplos, extraídos desse livro, são dados no quadro.
Nome antigo Nome proposto por Lavoisier Nome atual
ar vital oxigênio oxigênio
ar inflamável hidrogênio hidrogênio
ar fixo ácido carbônico dióxido de carbono
ácido vitriólico ácido sulfúrico ácido sulfúrico
vitríolo azul; vitríolo de cobre sulfato de cobre sulfato de cobre (II)
ácido marinho ácido muriático ácido clorídrico
sal marinho muriato de soda cloreto de sódio
soda aerada; soda efervescente carbonato de soda carbonato de sódio
Esse gás é o que, antigamente, era chamado de
Leia o texto para responder a questão.
Em seu livro Tratado Elementar de Química, publicado em 1789, Antonie Lavoisier estabeleceu uma nova nomenclatura para diversas substâncias químicas. Alguns exemplos, extraídos desse livro, são dados no quadro.
Nome antigo Nome proposto por Lavoisier Nome atual
ar vital oxigênio oxigênio
ar inflamável hidrogênio hidrogênio
ar fixo ácido carbônico dióxido de carbono
ácido vitriólico ácido sulfúrico ácido sulfúrico
vitríolo azul; vitríolo de cobre sulfato de cobre sulfato de cobre (II)
ácido marinho ácido muriático ácido clorídrico
sal marinho muriato de soda cloreto de sódio
soda aerada; soda efervescente carbonato de soda carbonato de sódio
Temperatura (°C) Kw pH 0 1,14 × 10–15 7,47 10 2,95 × 10–15 7,27 20 1,00 × 10–14 7,00 30 1,47 × 10–14 6,83 50 5,30 × 10–14 6,27
Analisando-se os dados, pode-se afirmar, corretamente, que a
Assinale a alternativa que apresenta a fórmula molecular e a quantidade mínima, em kg, de gás oxigênio necessária para a combustão completa de 5,6 kg desse combustível.
Massas Molares: H = 1 g/mol O = 16 g/mol C = 12 g/mo
Observe a seguinte reação de polimerização entre o etilenoglicol e o ácido tereftálico:
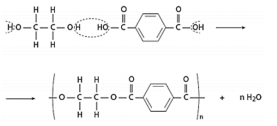
O nome da reação de polimerização acima, o nome do
polímero obtido e a função orgânica presente nele são
respectivamente: