Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume de dióxido de carbono recolhido (Figura 2)
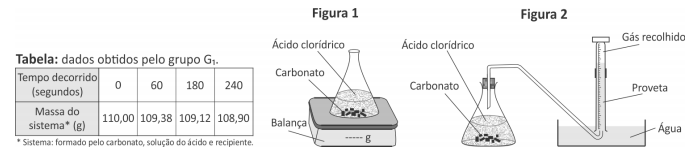
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
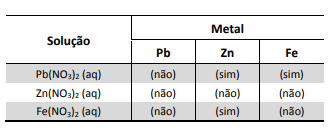
A seguir, montou três diferentes pilhas galvânicas, conforme esquematizado.
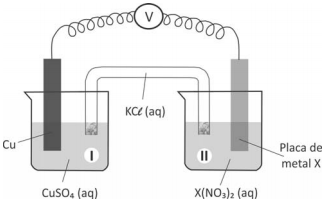
Nessas três montagens, o conteúdo do béquer I era uma solução aquosa de CuSO4 de mesma concentração, e essa solução era renovada na construção de cada pilha. O eletrodo onde ocorria a redução (ganho de elétrons) era o formado pela placa de cobre mergulhada em CuSO4 (aq). Em cada uma das três pilhas, o estudante utilizou, no béquer II, uma placa de um dos metais X (Pb, Zn ou Fe), mergulhada na solução aquosa de seu respectivo nitrato.
O estudante mediu a força eletromotriz das pilhas, obtendo os valores: 0,44 V; 0,75 V e 1,07 V. A atribuição correta desses valores de força eletromotriz a cada uma das pilhas, de acordo com a reatividade dos metais testados, deve se
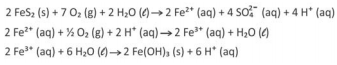
Considerando a equação química que representa a transformação global desse processo, as lacunas da frase “No intemperismo sofrido pela pirita, a razão entre as quantidades de matéria do FeS2 (s) e do O2 (g) é __________, e, durante o processo, o pH do solo __________” podem ser corretamente preenchidas por
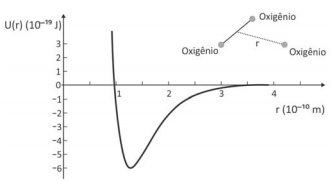
O gráfico representa a energia potencial de ligação entre um dos átomos de oxigênio que constitui a molécula de O3 e os outros dois, como função da distância de separação r.
A frequência dos fótons da luz ultravioleta que corresponde à energia de quebra de uma ligação da molécula de ozônio para formar uma molécula de O2 e um átomo de oxigênio é, aproximadamente .
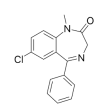
A respeito da molécula do diazepam, é correto afirmar que possui:
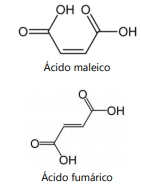
Sabendo que, na composição da nova linha de sorvetes, será utilizado o composto capaz de aumentar a validade do produto, a substância e sua justificativa de escolha são, respectivamente ácido:
Considere as seguintes afirmativas:
I. O but-1,3-dieno apresenta cadeia aberta e insaturada. II. Ambos os monômeros são hidrocarbonetos. III. O but-1,3-dieno pode apresentar isômeros planos de posição, como o but-1,4-dieno. IV. O fenil-eteno apresenta isômeros de posição.
Nesse contexto, é possível afirmar que estão CORRETAS as afirmativas:
AAS (s) + H2O (l) ⇄ AAS‾ (aq) + H3O+ (aq)
Assim, quando se toma um medicamento que contém o AAS com um pouco de água, a maior parte do medicamento encontra-se na forma ionizada (AAS‾ ) e nesta forma ela não atravessa a camada protetora das paredes do estômago. A forma neutra (AAS) pode atravessar as paredes do estômago causando hemorragia em algumas pessoas ou outras complicações médicas.
Sobre o equilíbrio químico do AAS em nosso organismo, é CORRETO afirmar que:
Texto adaptado de http://g1.globo.com/ciencia-e-saude/noticia/erro-decalculo-em-experimento-deixa-2-estudantes-de-ciencia-na-uti-porexcesso-de-cafeina.ghtml Acesso em 15 de abril de 2017.
Sabendo que a massa de cafeína (C8H10O2N4) foi dissolvida em 100 mL de suco de laranja, a concentração de cafeína ingerida por cada estudante foi aproximadamente de
2 H2O + 2 e- → H2 + 2 OH- E° = - 0,828 V ½ O2 + H2O + 2 e- → OH- E° = + 0,401 V
Levando-se em conta essas informações e as assertivas a seguir,
I. A reação global da pilha de combustível é H2 + ½ O2 → H2O II. O hidrogênio sofre oxidação no processo. III. A diferença de potencial da pilha de combustível, em condição padrão, é igual a 1,229 V. IV. O gás oxigênio (O2) é o agente redutor.
Pode-se afirmar que estão CORRETAS apenas:
Química orgânica
Há mulheres altas e mulheres baixas; mulheres bonitas e mulheres feias; mulheres gordas e mulheres magras; mulheres caseiras e mulheres rueiras; mulheres fecundas e mulheres estéreis; (...) Mas, do que pouca gente sabe é que há duas categorias antagônicas de mulheres cujo conhecimento é da maior utilidade, de vez que pode ser determinante na relação desses dois sexos que eu, num dia feliz, chamei de "inimigos inseparáveis". São as mulheres "ácidas" e as mulheres "básicas", qualificação esta tirada à designação coletiva de compostos químicos que, no primeiro caso, são hidrogenados, de sabor azedo; e no segundo, resultam da união dos óxidos com a água e devolvem à tintura do tornassol, previamente avermelhada pelos ácidos, sua primitiva cor azul.
Texto retirado de http://www.viniciusdemoraes.com.br/ptbr/prosa/quimica-organica Acesso em 23 de agosto de 2017.
O texto cita um indicador que muda de coloração de acordo com a característica ácido-básica do meio em que é colocado. A partir das colorações que o indicador pode adquirir, a alternativa que indica um composto que é responsável por deixar azul o papel de tornassol, é:
Texto adaptado de http://sustentabilidade.estadao.com.br/noticias/geral,poluicao-do-arem-sao-paulo-e-duas-vezes-o-limite-da-oms,10000050538 Acesso em 23 de agosto de 2017.
Acerca dos compostos mencionados no fragmento de texto acima, é possível afirmar que:
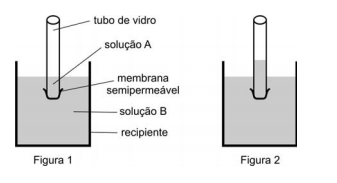
O aumento do nível da solução no interior do tubo de vidro é equivalente
I. A adição de algumas gotas de fenolftaleína a amostras de cada solução fez com que apenas a amostra de B se tornasse rosada.
II. A solução rosada, obtida no ensaio I, tornou-se incolor pela adição de amostra de A.
III. Amostras de A e C produziram precipitados brancos quando misturadas, em separado, com amostras de D.
Com base nessas observações e sabendo que sulfatos de metais alcalino-terrosos são pouco solúveis em água, pode-se concluir que A, B, C e D são, respectivamente, soluções aquosas de
Essas pilhas usam, como eletrólito, o KOH(aq), de modo que todas as reações ocorrem em meio alcalino. A troca de elétrons se dá na superfície de um material poroso. Um esquema dessas pilhas, com o material poroso representado na cor cinza, é apresentado a seguir.
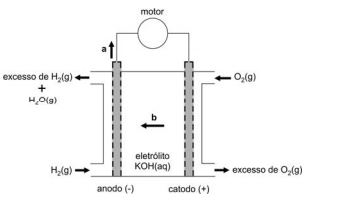
Escrevendo as equações das semirreações que ocorrem nessas pilhas de combustível, verifica-se que, nesse esquema, as setas com as letras a e b indicam, respectivamente, o sentido de movimento dos
Dado: tempo de meia-vida do 14C = 5 700 anos
I. As moléculas dos componentes da gasolina e as do oxigênio estão em equilíbrio químico e, por isso, não reagem.
II. À temperatura ambiente, as moléculas dos componentes da gasolina e as do oxigênio não têm energia suficiente para iniciar a combustão.
III. As moléculas dos componentes da gasolina e as do oxigênio encontram-se tão separadas que não há colisão entre elas.
Dentre as explicações, está correto apenas o que se propõe em