Questões de Vestibular
Sobre sistemas homogêneos: constantes: kc e kp. deslocamento do equilíbrio: fatores. em química
Foram encontradas 234 questões
DESMINERALIZAÇÃO E MINERALIZAÇÃO
Os dentes sofrem contínuos processos de desmineralização seguida por remineralização e restabelecimento da integridade do esmalte dentário devido ao controle do biofilme dentário (placa bacteriana), à presença de saliva, entre outros fatores. Quando a hidroxiapatita se dissolve, em um processo chamado desmineralização, os íons dispersam-se na saliva:
Ca5(PO4)3OH(s) ⇄ 5Ca2+(aq) + 3PO3-4(aq) + OH-(aq)
Sendo os fosfatos de metais alcalino-terrosos pouco solúveis, essa reação não se dá com grande extensão no sentido direto. A reação inversa, chamada mineralização, é a defesa natural do organismo contra a cárie:
5Ca2+(aq) + 3PO3-4(aq) + OH-(aq) ⇄ Ca5(PO4)3OH(s)
Nos adultos, esses dois processos se dão, aproximadamente, à mesma velocidade
Disponível em: https://desmineralizacaod.wordpress.com/2011/06/09/des mineralizacao-e-mineralizacao-2/. Acesso em: 16 de agosto de 2015.
Após uma refeição, as bactérias presentes na boca
decompõem parte dos alimentos, produzindo ácidos
orgânicos como o ácido acético e o ácido lático. Portanto,
é pertinente inferir que
2 NO2(g) ⇄ N2O4(g)
O sistema estará fora do equilíbrio químico, se essa reação ocorrer
3 O2(g) ⇄ 2 O3(g).
À medida que o oxigênio se transforma em ozônio, a pressão interna dos gases dentro do recipiente diminuiu. Isso ocorre devido à diminuição do número de moléculas. Quando o equilíbrio químico é atingido, a pressão fica constante.
Depois de atingido o equilíbrio, se a pressão do sistema for aumentada, o equilíbrio químico se
O uso do ácido acetil salicílico como princípio ativo de medicamentos analgésicos é bastante comum. Ao ser ingerida, essa substância se dissocia no estômago, em uma reação que apresenta equilíbrio químico. A equação abaixo representa a reação de dissociação do ácido acetil salicílico, cuja fórmula é representada de forma simplificada por HAs.
HAs(aq) ⇌ H+ (aq) + As- (aq).
O organismo humano absorve apenas a forma dissociada dessa substância, sendo o íon As- o responsável pelo efeito analgésico.
O procedimento que acelera a absorção do medicamento pelo organismo é
Um refrigerante é uma solução homogênea e líquida enquanto está contido em um frasco fechado. Quando se abre esse frasco, bolhas de gás surgem imediatamente, emergindo do líquido para a superfície. Esse gás é o dióxido de carbono que interage com a água segundo o equilíbrio:
CO2 (g) + H2O (l) ⇆ H2CO3 (aq).A opção que apresenta, corretamente, o deslocamento do equilíbrio da reação representada
é:
Com base na expressão
NH4+(aq) ⇄ H+(aq) + NH3(aq)
que representa a solução aquosa do (NH4)Cℓ , é correto afirmar que:
H2 (g) + Cl 2 (g) ⇄ 2 HCl (g) KC = 1,0 x 1017. H2 (g) + Br2 (g) ⇄ 2 HBr (g) KC = 1,0 x 109 . H2 (g) + I2 (g) ⇄ 2 HI (g) KC = 1,0 x 101.
Depois de atingido o equilíbrio,
A formação da casca dos ovos das aves é, geralmente, proveniente da reação:
Ca2+(aq) + CO32-(aq) ⇄ CaCO3(s)
Os íons CO32- são naturalmente produzidos a partir do metabolismo do CO2 e do Ca2+, que são convertidos em H2CO3 enzimaticamente, originando os seguintes equilíbrios:
CO2(g) + H2O(I) ⇄ H2CO3(aq)
H2CO3(aq) ⇄ H+(aq) + HCO3-(aq)
HCO3-(aq) ⇄ H+(aq) + CO32-(aq)
Como as aves não transpiram, faz-se necessária uma intensa respiração para resfriar seus
corpos, acarretando grande liberação de CO2 e, conseqüentemente, a deficiência de íons
CO32-, comprometendo a formação da casca dos ovos. De acordo com o princípio de Le Chatelier, a melhoria do processo de formação da casca dos ovos das aves se dá com
Em condições reacionais adequadas, hidrogênio, H2(g) e cloro, Cℓ 2(g) reagem entre si formando cloreto de hidrogênio, HCℓ (g). Esse processo é reversível e exotérmico, podendo ser representado por
H2(g) + Cℓ 2(g) 2 HCℓ (g) ΔH = - 92,3 kJ . mol –1 .
Depois de atingido o equilíbrio, o fator que não altera esse estado de equilíbrio é a variação da
O estado de equilíbrio existente em um frasco contendo solução de amoníaco, mantido fechado e a temperatura constante, pode ser representado pelas equações:
I - NH3(g) ⇌ NH3 (aq)
II - NH3 (aq) + H2O ⇌ NH4+(aq) + OH-(aq)
III - 2H2O ⇌ H3O+ + OH-
Se o frasco for aberto e assim permanecer por algumas horas, a concentração de
O gás nitrogênio (N2) reage com o gás oxigênio (O2), conforme a reação a seguir:
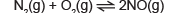
Considere que a constante de equilíbrio da reação é igual a 16 e que as concentrações de equilíbrio de N2 e O2 são, respectivamente, 02mol/L e 02mol/L.
Baseado nos conhecimentos sobre sistemas reversíveis, o valor da concentração molar de NO é igual a
As cavernas são formadas pela dissolução de carbonato de cálcio (CaCO3) em água. Esse sal é muito comum na natureza e pode ser encontrado em grande quantidade na constituição do calcário. Ele não é muito solúvel em água; no entanto, quando está na presença de dióxido de carbono (gás carbônico – CO2) e sendo submetido a altas pressões, o carbonato de cálcio se solubiliza bem na água. As águas subterrâneas se encontram exatamente nessas condições, isto é, com grande quantidade de gás carbônico dissolvido e a elevadas pressões. Assim, quando as águas subterrâneas passam por terrenos contendo calcário, ocorre a dissolução do carbonato de cálcio, conforme pode ser representado pela seguinte equação química:
CaCO3(s) + CO2(g) + H2O(ℓ) → Ca2+(aq) + 2HCO-3(aq) ΔH < 0
Entretanto, essa reação também pode ocorrer no sentido inverso, resultando na formação do calcário. Isso acontece, por exemplo, quando essas águas ficam no teto das cavernas e vão gotejando muito lentamente. Dessa forma, a água vai evaporando e também há a liberação do CO2(g), e o carbonato vai se depositando na forma de estalactites no teto e estalagmites no chão das cavernas.
Ca2+(aq) + 2 HCO-3(aq) → CaCO3(s) + CO2(g) + H2O(ℓ) ΔH > 0
Disponível em:<http://mundoeducacao.bol.uol.com.br/quimica/formacaoconstituicao-estalactites-estalagmites.htm> . Acesso em: 29 de julho de 2016.
2HI(g) ⇌ H2(g) + I2(g) ΔH° = − 53kJ
Uma análise dessas informações permite afirmar:
2H2(g) + O2(g)→ 2H2O(v)
Em um recipiente aberto, a água evapora até o fim, na temperatura e pressão ambiente. Entretanto, quando o recipiente é fechado, as moléculas de água são impedidas de escapar, ocorrendo, então, um equilíbrio de evaporação entre água líquida e vapor, a 25o°C e 1,0atm. Uma análise dessas informações permite corretamente concluir:
As substâncias nitrogenadas desempenham importante papel em nossa sociedade. Dentre as de maior importância estão a amônia e o ácido nítrico, usadas na fabricação do náilon e do poliuretano. A conversão de NH3 em NO com o uso de catalisador é o primeiro passo para a fabricação industrial do ácido nítrico e a rota industrial para a obtenção de substâncias oxigenadas do nitrogênio. A reação de produção de NO a partir de NH3 é:
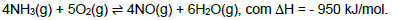
Quando a reação atinge o equilíbrio, uma maneira de aumentar a produção de NO(g) é aumentando a(o)
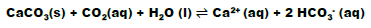
Analise as afirmativas sobre o sistema no equilíbrio e marque a alternativa CORRETA.
A hemoglobina (Hb) é a proteína responsável pelo transporte de oxigênio. Nesse processo, a hemoglobina se transforma em oxihemoglobina (Hb(O2)n). Nos fetos, há um tipo de hemoglobina diferente da do adulto, chamada de hemoglobina fetal. O transporte de oxigênio pode ser representado pelo seguinte equilíbrio:
Hb + nO2 ⇌ Hb(O2)n ,
em que Hb representa tanto a hemoglobina do adulto quanto a hemoglobina fetal. A figura mostra a porcentagem de saturação de Hb por O2 em função da pressão parcial de oxigênio no sangue humano, em determinado pH e em determinada temperatura.
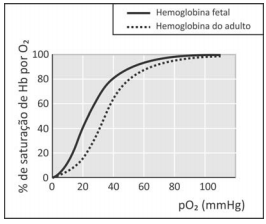
A porcentagem de saturação pode ser entendida como:
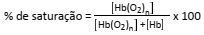
Com base nessas informações, um estudante fez as seguintes afirmações:
I. Para uma pressão parcial de O2 de 30 mmHg, a hemoglobina fetal transporta mais oxigênio do que a hemoglobina do adulto.
II. Considerando o equilíbrio de transporte de oxigênio, no caso de um adulto viajar do litoral para um local de grande altitude, a concentração de Hb em seu sangue deverá aumentar, após certo tempo, para que a concentração de Hb(O2)n seja mantida.
III. Nos adultos, a concentração de hemoglobina associada a oxigênio é menor no pulmão do que nos tecidos.
É correto apenas o que o estudante afirmou em
Note e adote:
pO2 (pulmão) > pO2 (tecidos).
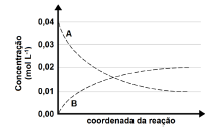
Com base nas informações, analise os itens I a III.
I) A reação balanceada entre as espécies citadas é 3A⇔2B. II) O valor da constante de equilíbrio da reação é 4x102 . III) O equilíbrio estabelecido é deslocado para os produtos ao se diminuir o volume do recipiente.
Está(ão) correto(s):
Uma das reações utilizadas para a demonstração de deslocamento de equilíbrio, devido à mudança de cor, é a representada pela equação a seguir:
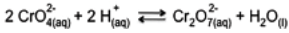
sendo que, o cromato (CrO42- ) possui cor amarela e o dicromato (Cr2O72- ) possui cor alaranjada.
• Sobre esse equilíbrio foram feitas as seguintes afirmações:
I. A adição de HCl provoca o deslocamento do equilíbrio para a direita.
II. A adição de NaOH resulta na cor alaranjada da solução.
III. A adição de HCl provoca o efeito do íon comum.
IV. A adição de dicromato de potássio não desloca o equilíbrio.
• As afirmações corretas são:
