Questões de Vestibular
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 328 questões
A força dos ácidos pode ser considerada como um parâmetro que mede a quantidade de íons H+ liberados para solução quando diluídos em água.
Sobre a força dos ácidos, o grau de ionização e o cálculo do pH, relacione a coluna da esquerda com a da direita.
(I) CH3COOH (Ka = 1,80×10−5 ) (II) HCℓ (Ka = 1,00×107) (III) HF (Ka = 6,70×10−4) (IV) HCN (Ka = 4,90×10−10) (V) HNO2 (Ka = 6,09×10−6)Assinale a alternativa que contém a associação correta.
NH3 (g) + H2O (l) ⇌ NH4+ (aq) + OH– (aq)
Uma solução aquosa de NH3 apresenta concentração inicial de 0,02 mol/L a 25oC. Nessas condições, o valor da concentração de íons OH– , em mol/L, é
Dado: Constante de basicidade da amônia a 25o C: Kb = 1,8 × 10-5
Temperatura (°C) Kw pH 0 1,14 × 10–15 7,47 10 2,95 × 10–15 7,27 20 1,00 × 10–14 7,00 30 1,47 × 10–14 6,83 50 5,30 × 10–14 6,27
Analisando-se os dados, pode-se afirmar, corretamente, que a
Para explorar convenientemente a cultura da soja, é indispensável incorporar calcário aos solos que estão com pH inferior a 5,5. A quantidade de calcário a ser aplicada no terreno é determinada através da análise do solo.
Considerando-se essas informações, é INCORRETO afirmar que
Com base nos dados da tabela, pode-se afirmar que apenas
CH3COOH(aq) + H2O(l) ⇌ CH3COO− (aq) + H+ (aq)
Equilíbrio iônico é o caso particular de equilíbrio químico em que aparecem íons. Os íons estão presentes em várias soluções aquosas encontradas na natureza e nos organismos dos seres vivos. Dos equilíbrios químicos iônicos em solução aquosa, um dos mais importantes é o que ocorre na ionização de ácidos e de bases. A concentração desses íons depende, entre outros fatores, do grau de ionização, α, e do valor da constante de ionização, Ka.
Desse modo, considerando-se uma solução de ácido acético 0,02 mol L−1 , cujo grau de ionização, α, é igual a 3%, em equilíbrio químico representado pela equação química, é correto afirmar:
Experiência – Escrever uma mensagem secreta no laboratório
Materiais e Reagentes Necessários
✓ Folha de papel
✓ Pincel fino
✓ Difusor
✓ Solução de fenolftaleína
✓ Solução de hidróxido de sódio 0,1 mol/L ou solução saturada de hidróxido de cálcio
Procedimento Experimental
Utilizando uma solução incolor de fenolftaleína, escreva com um pincel fino uma mensagem numa folha de papel.
A mensagem permanecerá invisível.
Para revelar essa mensagem, borrife a folha de papel com uma solução de hidróxido de sódio ou de cálcio, com o auxílio de um difusor.
A mensagem aparecerá magicamente com a cor vermelha.
Explicação
fenolftaleína é um indicador que fica vermelho na presença de soluções básicas, nesse caso, uma solução de hidróxido de sódio ou de cálcio.
A fenolftaleína atua como um indicador ácido-base por ser um ácido fraco, que em solução alcóolica, apresenta a cor das moléculas não-dissociadas, HInd, diferente da cor dos respectivos íons, Ind–.
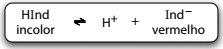
A leitura da mensagem no experimento descrito é possível
porque a presença de íons OH– na solução de fenolftaleína
promove deslocamento do equilíbrio para a
Na indústria têxtil, é uma prática comum aplicar goma aos tecidos no início da produção, para torná-los mais resistentes. Esse produto, entretanto, precisa ser removido posteriormente, no processo de desengomagem. Nesse processo, os produtos têxteis são mergulhados em um banho aquoso com uma enzima do grupo das amilases.
Os gráficos nas figuras 1 e 2 representam a eficiência da atividade dessa enzima em diferentes valores de temperatura e pH.
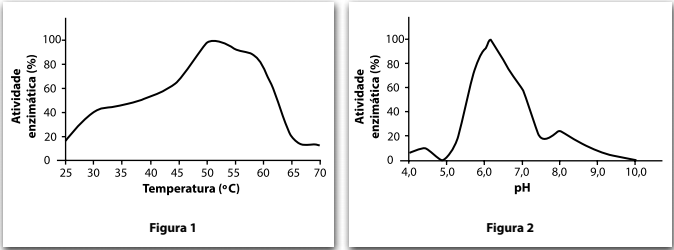
Com base nas informações apresentadas, está correto afirmar que, para se obter a máxima eficiência da ação da enzima no
processo industrial citado no texto, seria necessário manter o banho aquoso de desengomagem a
Com relação às informações, analise as proposições.
I. A solução A contém um ácido forte, com concentração de 0,01000 mol L-1 e a solução B contém um ácido fraco com concentração 1,000x10-4 M. II. As duas soluções contêm a mesma concentração de ácido igual a 0,01000 M, mas os ácidos têm diferentes graus de dissociação. III. Uma vez que o pH das amostras é diferente, a concentração dos ácidos em cada uma é necessariamente diferente. IV. As duas soluções contêm a mesma concentração de ácido, mas o ácido presente na solução A está completamente dissociado, e o ácido na solução B está apenas 1% dissociado. V. A medição apenas do pH não informa sobre a concentração total de ácido, mas apenas sobre a fração de ácido que está dissociada.
Assinale a alternativa correta.
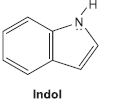 Kb = 2,0x10-12
Kb = 2,0x10-12O indol tem odor semelhante à essência floral, quando bastante diluído em etanol, e odor muito forte, quando em solução etanólica concentrada.
Considerando-se essas informações, é correto afirmar que o indol
Sabe-se pKa = - logKa = 7.20, em que Ka é a constante de dissociação do H2 PO4 - em água a 25 ºC.
O pH da primeira solução e a relação do pH da segunda solução com o pH da primeira são, respectivamente:
O pH plasmático deve ser mantido na faixa de 7,35 - 7,45. Variações do pH afetam a estrutura das proteínas e, consequentemente, os processos bioquímicos. Nosso organismo produz várias substâncias capazes de alterar o pH do plasma como, por exemplo, o ácido láctico e os corpos cetônicos. A manutenção do pH ideal é feita graças à existência: dos sistemas tampão, do centro respiratório e do sistema renal. O principal sistema tampão presente no plasma é constituído por ácido carbônico/hidrogenocarbonato. Esse sistema envolve três equilíbrios, os quais estão representados abaixo.
Observe os equilíbrios e avalie as afirmativas.
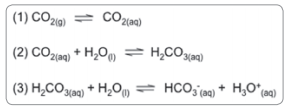
I. O equilíbrio representado na equação 3 mostra o ácido carbônico, que é um ácido fraco, e o HCO3- sua base conjugada.
II. A adição de H3O+, proveniente de uma substância ácida, reage com os íons hidrogenocarbonato deslocando o equilíbrio (equação 3) para a esquerda.
III. A solução tampão impede a variação de pH somente quando substâncias ácidas são adicionadas, não sendo possível a manutenção do pH frente à adição de substâncias básicas.
IV. A solução tampão mantém o pH relativamente constante, independentemente da quantidade de H3O+ adicionada .
É CORRETO afirmar que
Após o preparo de uma solução 5x10-2 mol/L de NaNO2, pode-se afirmar que o pH é aproximadamente igual a: (Dados: Ka=5x10-4 para HNO2); Kw=1,0x10-14 a 25°C).
(1) CO2(g) ⇋ CO2(aq) (2) CO2(aq) + H2O (l) ⇋ H2CO3(aq) (3) H2CO3(aq) + H2O (l) ⇋ HCO3-(aq)+ H3O+ (aq)
I. O equilíbrio representado na equação 3 mostra o ácido carbônico, que é um ácido fraco, e o HCO3- sua base conjugada.
II. A adição de H3O+, proveniente de uma substância ácida, reage com os íons hidrogenocarbonato deslocando o equilíbrio (equação 3) para a esquerda.
III. A solução tampão impede a variação de pH somente quando substâncias ácidas são adicionadas, não sendo possível a manutenção do pH frente à adição de substâncias básicas.
IV. A solução tampão mantém o pH relativamente constante, independentemente da quantidade de H3O+ adicionada .
É CORRETO afirmar que

