Questões de Vestibular
Sobre soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. em química
Foram encontradas 448 questões
Texto adaptado de http://g1.globo.com/ciencia-e-saude/noticia/erro-decalculo-em-experimento-deixa-2-estudantes-de-ciencia-na-uti-porexcesso-de-cafeina.ghtml Acesso em 15 de abril de 2017.
Sabendo que a massa de cafeína (C8H10O2N4) foi dissolvida em 100 mL de suco de laranja, a concentração de cafeína ingerida por cada estudante foi aproximadamente de
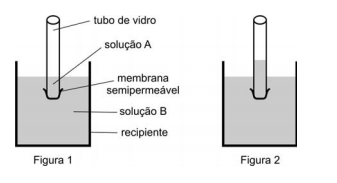
O aumento do nível da solução no interior do tubo de vidro é equivalente
Leia o texto e a tabela para responder à questão.
Barcarena, no nordeste do Pará, é uma cidade da Amazônia marcada por desastres ambientais. Há semanas, depois de fortes chuvas, houve um vazamento de rejeitos em uma das empresas do polo industrial, o que contaminou rios da região. No município de Barcarena já houve outros registros de crimes ambientais de contaminação.
Em 2004, a Universidade Federal do Pará (UFPA) realizou uma pesquisa que concluiu que a água consumida pela população, em 26 localidades, estava contaminada por íons de metais pesados tais como Pb2+, Cd2+ e Hg2+, descartados pelas indústrias. Amostras de água de Vila Nova, Burajuba e do Distrito Industrial apresentaram concentração de chumbo 12 vezes maior que o máximo permitido por uma resolução de 2011 do Ministério da Saúde.

Assinale a alternativa que apresenta a massa total de chumbo ingerida pelo paciente, em miligramas.
O ácido ascórbico, C6H8O6, também conhecido como Vitamina C, é utilizado popularmente por suas propriedades terapêuticas. A vitamina C é comercializada em diversas formas, uma das mais comuns é como comprimidos mastigáveis, que contêm ácido ascórbico na sua composição. Além de ser um ácido, a vitamina C também é um agente redutor. Uma das formas para determinar a quantidade de ácido ascórbico, em uma amostra, é titular com uma solução de bromo, Br2, um agente oxidante, conforme equação química abaixo:
C6H8O6(aq) + Br2(aq) → 2 HBr(aq) + C6H6O6(aq)
Um comprimido, contendo vitamina C em sua composição, possui massa total (vitamina C + excipientes) 1,00 g e requer 20,00 mL de uma solução de bromo, preparada solubilizando 2,25 g de bromo em 100 mL de solução aquosa.
Com base nas informações acima e na equação química, assinale a alternativa que apresenta a concentração da solução de bromo preparada e a massa de vitamina C contida no comprimido.
As curvas de solubilidade têm grande importância no estudo das soluções de sólidos em líquidos, porque a temperatura é o único fator físico perceptível que influi na solubilidade. Há certas substâncias químicas cujas curvas de solubilidade apresentam pontos de inflexão que denotam mudanças de estrutura do soluto, como é possível verificar no gráfico da solubilidade do sulfato de sódio decaidratado, Na2SO4.10H2O.
A análise desse gráfico permite corretamente afirmar:
Experiência – Escrever uma mensagem secreta no laboratório
Materiais e Reagentes Necessários
✓ Folha de papel
✓ Pincel fino
✓ Difusor
✓ Solução de fenolftaleína
✓ Solução de hidróxido de sódio 0,1 mol/L ou solução saturada de hidróxido de cálcio
Procedimento Experimental
Utilizando uma solução incolor de fenolftaleína, escreva com um pincel fino uma mensagem numa folha de papel.
A mensagem permanecerá invisível.
Para revelar essa mensagem, borrife a folha de papel com uma solução de hidróxido de sódio ou de cálcio, com o auxílio de um difusor.
A mensagem aparecerá magicamente com a cor vermelha.
Explicação
fenolftaleína é um indicador que fica vermelho na presença de soluções básicas, nesse caso, uma solução de hidróxido de sódio ou de cálcio.
Um aluno da Fatec foi ao laboratório de Química para realizar esse experimento. Lá ele encontrou apenas uma solução aquosa de NaOH de concentração 0,5 mol/L.
Para realizar a experiência na concentração descrita no texto, a partir da solução que ele encontrou, deverá realizar uma
O uso de flúor é eficaz no combate à cárie dentária. Por isso, foram estabelecidos protocolos de utilização do flúor na área de saúde bucal como a adição de flúor na água de abastecimento público e em pastas dentais. A escovação dental é considerada um dos métodos mais eficazes na prevenção da cárie, ao aliar a remoção da placa à exposição constante ao flúor.
Todavia, a exposição excessiva pode causar alguns malefícios à saúde. Para isso, foram estabelecidos níveis seguros de consumo do flúor, quando este oferece o máximo benefício sem risco à saúde. As pastas de dente apresentam uma concentração de flúor que varia entre 1 100 e 1 500 ppm.
É importante ressaltar que as pastas de dente com flúor devem ser utilizadas durante a escovação e não ingeridas.
(http://tinyurl.com/ovrxl8b Acesso em: 29.08.2014. Adaptado)
A concentração máxima de flúor presente nas pastas de
dente mencionada no texto, em porcentagem em massa,
corresponde a
Observe a sequência de adição de volumes de solução a seguir.
10 mL de H2SO4 1,0 mol/L + 20 mL de NaOH 1,0 mol/L +
10 mL de HNO3 1,0 mol/L + 05 mL de NaOH 2,0 mol/L
Com base nos conhecimentos sobre reações químicas ácido-base, assinale a alternativa que apresenta,
corretamente, o pH final da solução.
(Dados: massa molar do HCℓ 36,46 g/mol)
Dados: Massas Molares (g/mol): NaOH = 40 e HCl = 36,5 Reação: NaOH + HCl → NaCl + H2O
Sobre o resultado da titulação, é correto afirmar que a informação
Com base na informação, assinale a alternativa correta em relação ao resíduo.
Considerando as informações constantes na tabela, assinale a alternativa correta.
Composto Solubilidade a 18ºC (mol/L)
HCl 9,4
AgNO3 8,3
AgCl 10-5
KNO3 2,6
KCl 3,9
Sendo assim, considerando uma piscina de formato retangular que tenha 10 m de comprimento, 5 m de largura e 2 m de profundidade, quando cheia de água,a massa máxima de sulfato de cobre que poderá se dissolver é, em gramas, igual a
Dado: 1m3 = 1 000 L
Ao chegar ao Rio, de Corumbá, Fuentes hospedou-se no Hotel Bragança, na avenida Mem de Sá. Um hotel cheio de turistas argentinos falando portunhol. [...] Na lista telefônica Fuentes escolheu um oftalmologista de nome espanhol, Pablo Hernandez. O dr. Hernandez descendia de uruguaios e, para desapontamento de Fuentes, não falava espanhol. Em seu bem montado consultório, na avenida Graça Aranha, na Esplanada do Castelo, examinou Fuentes cuidadosamente. O cristalino, a íris, a conjuntiva, o nervo ótico, os músculos, artérias e veias do aparelho ocular estavam perfeitos. A córnea, porém, fora atingida. Didaticamente Hernandez explicou ao seu cliente que a córnea era uma camada externa transparente através da qual a luz – e com a luz, a cor, a forma, o movimento das coisas – penetrava no olho.
Córnea – moça, 24ª , vende. Tel. 185-3944. O anúncio no O Dia foi lido por Fuentes. Ele ligou de seu quarto, no Hotel Bragança. Atendeu uma mulher...[...] Ela disse que ele podia pegar um ônibus no largo de São Francisco. “É para você?”, perguntou a mulher quando Fuentes lhe falou que era a pessoa que havia telefonado. [...] “Sim, é para mim.” A mulher não ter percebido a cicatriz no seu olho esquerdo deixou Fuentes satisfeito. [...] “Dez milhas”, disse a mulher impaciente. “E não é caro. O preço de um carro pequeno. Minha filha é muito moça, nunca teve doença, dentes bons, ouvidos ótimos. Olhos maravilhosos.”
(FONSECA, Rubem. A Grande Arte. São Paulo: Companhia das Letras, 2008. p. 137-139.)
Com base em algumas ideias do texto 02, foram elaboradas as proposições abaixo. Marque a única correta:
