Questões de Vestibular
Sobre teoria atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica em química
Foram encontradas 306 questões
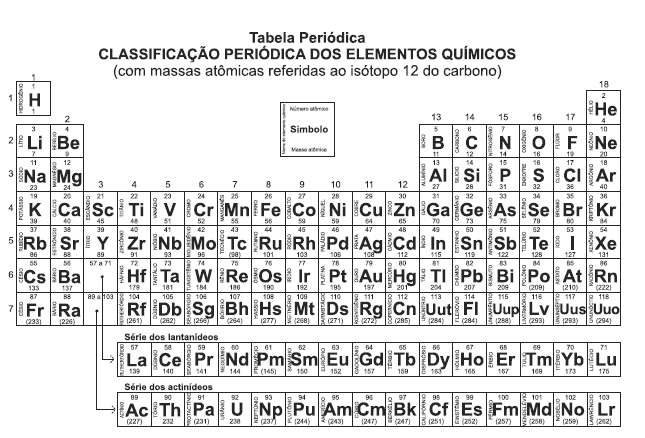
A partir da análise da Tabela Periódica, pode-se afirmar:
I. O raio atômico do sódio é menor que o do estrôncio.
II. A formação do íon Li+ requer mais energia que a do Na+, a partir de seus respectivos átomos neutros.
III. O potássio e o cloro originam íons de cargas idênticas.
IV. A espécie iônica mais estável para o magnésio é o íon Mg3+.
Está(ão) correta(s) apenas a(s) afirmativa(s):
Em abril de 1898, Marie Sklodowska Curie (1867-1934) e Pierre Curie (1859-1906), ao processar a pechblenda obtiveram duas frações radioativas. Uma delas apresentou uma radioatividade 400 vezes maior que a do urânio. O casal Curie associou essa radioatividade a um novo elemento químico, o qual foi denominado polônio, em homenagem à Polônia, terra natal de Marie Curie. O polônio foi o terceiro elemento radioativo identificado, depois do urânio e do tório, o que levou Marie Curie a receber o Prêmio Nobel de Química em 1911.
Na natureza há sete isótopos naturais do polônio, representados por: 210Po, 211Po, 212Po, 214Po, 215Po, 216Po e 218Po. Todos os isótopos desse elemento desintegram-se por emissão de partículas alfa, produzindo isótopos de chumbo. A elevada energia das partículas alfa emitidas pelo polônio permite a identificação de diminutas quantidades desse elemento em uma amostra. O polônio se dissolve em ácidos diluídos produzindo soluções contendo íons Po2+ .
Considere as informações acima e assinale a proposição CORRETA.
O cátion Po2+ apresenta 86 elétrons.
Em abril de 1898, Marie Sklodowska Curie (1867-1934) e Pierre Curie (1859-1906), ao processar a pechblenda obtiveram duas frações radioativas. Uma delas apresentou uma radioatividade 400 vezes maior que a do urânio. O casal Curie associou essa radioatividade a um novo elemento químico, o qual foi denominado polônio, em homenagem à Polônia, terra natal de Marie Curie. O polônio foi o terceiro elemento radioativo identificado, depois do urânio e do tório, o que levou Marie Curie a receber o Prêmio Nobel de Química em 1911.
Na natureza há sete isótopos naturais do polônio, representados por: 210Po, 211Po, 212Po, 214Po, 215Po, 216Po e 218Po. Todos os isótopos desse elemento desintegram-se por emissão de partículas alfa, produzindo isótopos de chumbo. A elevada energia das partículas alfa emitidas pelo polônio permite a identificação de diminutas quantidades desse elemento em uma amostra. O polônio se dissolve em ácidos diluídos produzindo soluções contendo íons Po2+ .
Considere as informações acima e assinale a proposição CORRETA.
Ao receber dois elétrons, o átomo de polônio adquire a configuração eletrônica do gás nobre
radônio.
Em abril de 1898, Marie Sklodowska Curie (1867-1934) e Pierre Curie (1859-1906), ao processar a pechblenda obtiveram duas frações radioativas. Uma delas apresentou uma radioatividade 400 vezes maior que a do urânio. O casal Curie associou essa radioatividade a um novo elemento químico, o qual foi denominado polônio, em homenagem à Polônia, terra natal de Marie Curie. O polônio foi o terceiro elemento radioativo identificado, depois do urânio e do tório, o que levou Marie Curie a receber o Prêmio Nobel de Química em 1911.
Na natureza há sete isótopos naturais do polônio, representados por: 210Po, 211Po, 212Po, 214Po, 215Po, 216Po e 218Po. Todos os isótopos desse elemento desintegram-se por emissão de partículas alfa, produzindo isótopos de chumbo. A elevada energia das partículas alfa emitidas pelo polônio permite a identificação de diminutas quantidades desse elemento em uma amostra. O polônio se dissolve em ácidos diluídos produzindo soluções contendo íons Po2+ .
Considere as informações acima e assinale a proposição CORRETA.
O isótopo 210Po possui número de nêutrons igual a 126.
O seu traje habitual era, como o de todas as mulheres da sua condição e esfera, uma saia de lila preta, que se vestia sobre um vestido qualquer, um lenço branco muito teso e engomado ao pescoço, outro na cabeça (...). Nos dias dúplices, em vez de lenço à cabeça, o cabelo era penteado, e seguro por um enorme pente cravejado de crisólitas.
ALMEIDA, Manuel Antônio de. Memórias de um sargento de milícias. São Paulo:
Ática, 2003. p. 30.
A crisólita é um silicato de ferro e magnésio que tem fórmula geral (Mg, Fe)2SiO4, cujas colorações variam do amarelo ao verde. Possui teor de ferro de 10 a 30%, sendo utilizada na fabricação de refratários e em joalheria.
Dados os valores de energia de ionização (EI) em kJ mol-1 para:
magnésio: EI1 = 738; EI2 = 1450
silício: EI1 = 786; EI2 = 1580
De acordo com as informações acima, assinale a proposição CORRETA.
Átomos de magnésio apresentam configuração eletrônica igual a do íon Si4+

O elemento químico X possui 15 nêutrons, é isótopo do elemento químico Y, que possui 13 prótons, e isóbaro do elemento químico Z, que tem 12 nêutrons.
Com base nessas informações, pode-se afirmar que os elementos químicos X, Y e Z apresentam, respectivamente, números atômicos iguais a:
A nova Tabela Periódica, atualizada em março de 2017 pela
IUPAC, contém os nomes e símbolos dos elementos químicos
niônio113, moscóvio115, tennessínio117 e oganessônio118,
em homenagem aos pesquisadores e descobridores
japoneses, russos e americanos. Os novos elementos são
transactinoides de existência efêmera, de frações de segundos
e foram sintetizados nos aceleradores de partículas. Assim,
completam o sétimo período da Tabela. A equipe de
pesquisadores do niônio113, vai em busca do 119 e de suas
propriedades, o primeiro elemento químico do oitavo período.
As propriedades periódicas dos elementos químicos,
organizados em grupos e períodos, estão relacionadas aos
números atômicos e configurações eletrônicas. As tendências
dessas propriedades são verificadas em um grupo ou de um
grupo para o outro, ou entre elementos de um período.
Os isótopos do cloro, de massas atômicas 35 e 37, estão presentes na natureza, respectivamente, nas porcentagens de:
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
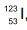 , e iodo-131,
, e iodo-131, 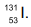 (http://www.cnen.gov.br/radiofarmacos. Adaptado)
(http://www.cnen.gov.br/radiofarmacos. Adaptado)
Os átomos de iodo-123 e iodo-131 possuem
DADOS QUE PODEM SER USADOS NESTA PROVA:

DADOS QUE PODEM SER USADOS NESTA PROVA:

A revista Química Nova na Escola, vol. 37, p.3, traz a seguinte manifestação sobre a produção do tecido das calças jeans: “Além da toxicidade envolvida no cultivo de sua matéria-prima, na produção industrial de jeans a etapa de tingimento consome 90% da água de todo o processo e gera grande volume de efluentes contaminados”. Entre os agentes contaminadores estão corantes sintéticos, metais como cádmio, chumbo, mercúrio, zinco e, ainda, surfactantes, sulfetos e solventes que deixam na água elevados índices de acidez.
Atente às afirmações a seguir e assinale a verdadeira.
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0