Questões de Vestibular
Sobre teoria atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica em química
Foram encontradas 306 questões
Certo isótopo desse elemento possui 86 prótons, 86 elétrons e número de massa 222, logo o número de nêutrons desse isótopo é
Analise o Quadro que apresenta o número de prótons, elétrons e nêutrons de quatro espécies químicas.
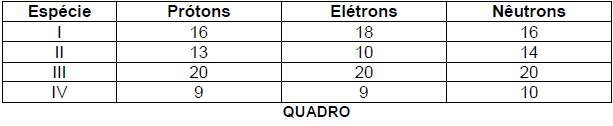
Considerando os dados apresentados no Quadro e de acordo com a Tabela Periódica, assinale
a alternativa incorreta.
Em 2014, na Alemanha, um elemento pesado foi confirmado por experimentos com um colisor de partículas e ocupará sua justa posição como Elemento 117 na Tabela Periódica.
Bombardeando amostras de berquélio radioativo com átomos de cálcio, pesquisadores criaram átomos com 117 prótons, originando um elemento químico, aproximadamente, 42% mais pesado que o chumbo e com meia-vida relativamente longa. Os físicos apelidaram, temporariamente, o novo integrante da Tabela Periódica como “ununséptio” (Uus), alusão direta ao numeral 117, que é a soma dos 20 prótons do cálcio com os 97 do berquélio.
(http://tinyurl.com/m8nlkq2 Acesso em: 13.06.2014. Adaptado)
De acordo com o texto, a massa atômica aproximada do ununséptio é

Analise os pares de elementos químicos a seguir.
(20Ca40 e 19K 40) – (17Cℓ 35 e 17Cℓ 37) – (5B 11 e 6Cℓ 12)
Assinale a alternativa que apresenta, correta e respectivamente, as características desses pares de elementos químicos.
Assinale a alternativa que contém, sequencialmente, o elemento Q e seu número atômico.
I. Os átomos do tálio são maiores que os átomos do bário. II. Os átomos do germânio são mais eletronegativos que os de carbono. III. A configuração eletrônica dos átomos de titânio, em ordem crescente de energia, é 1s22s22p63s23p64s23d2 . IV. Os átomos de bromo são os mais eletronegativos do quarto período da tabela periódica.
Assinale a alternativa correta.
Assinale a alternativa que apresenta o composto químico com o caráter iônico mais acentuado.
X ➔ 1s² 2s² 2p6 3s² 3p4
Sobre as propriedades químicas deste átomo, assinale a alternativa correta:
O urânio 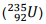 é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
Os valores de Z (N° Atômico), A (N° de Massa), p+ (Prótons), e- (Elétrons) e n° (Nêutrons) do íon Potássio (K) carregado positivamente, na forma catiônica, e com carga elétrica igual a +1, são respectivamente:
Dados: No estado fundamental o Potássio (K) possui N° Atômico = 19 e N° de Massa = 39
Áreas como a medicina, a agricultura e a indústria farmacêutica são beneficiadas com o desenvolvimento dos estudos da radioatividade. A radioterapia – técnica utilizada para destruir células cancerosas – faz uso, principalmente, de radioisótopos do iodo-131 para eliminar lesões identificadas nos radiodiagnósticos da tireoide.
Sobre esse radioisótopo, assinale a alternativa correta.
 têm-se mostrado
promissoras devido ao potencial terapêutico comprovado
em cobaias. Sobre um átomo eletricamente neutro do elemento químico ouro, verifica-se que no núcleo há
têm-se mostrado
promissoras devido ao potencial terapêutico comprovado
em cobaias. Sobre um átomo eletricamente neutro do elemento químico ouro, verifica-se que no núcleo há Assinale a alternativa correta.
A primeira lâmpada comercial, desenvolvida por Thomas Edison, consistia em uma haste de carbono, que era aquecida pela passagem de uma corrente elétrica a ponto de emitir luz visível. Era, portanto, uma lâmpada incandescente, que transforma energia elétrica em energia luminosa e energia térmica. Posteriormente, passou-se a utilizar, no lugar da haste, filamentos de tungstênio, cuja durabilidade é maior. Hoje, esse tipo de lâmpada tem sido substituído pelas lâmpadas fluorescentes e de LED.
As lâmpadas fluorescentes são construídas com tubos de vidro transparente revestidos internamente e contêm dois eletrodos (um em cada ponta) e uma mistura de gases em seu interior — vapor de mercúrio e argônio, por exemplo. Quando a lâmpada fluorescente é ligada, os eletrodos geram corrente elétrica, que, ao passar através da mistura gasosa, excita seus componentes, os quais, então, emitem radiação ultravioleta. O material que reveste o tubo tem a propriedade de converter a radiação ultravioleta em luz visível, que é emitida para o ambiente.
A lâmpada de LED é mais econômica que a incandescente, pois dissipa menos energia em forma de calor. Em geral, essas lâmpadas têm eficiência de 15 lumens por watt. Um lúmen (unidade padrão do Sistema Internacional) é o fluxo luminoso emitido por uma fonte puntiforme com intensidade uniforme de 1 candela e contido em um cone de ângulo sólido de um esferorradiano. A tabela a seguir apresenta características específicas das lâmpadas incandescentes, fluorescentes e de LED.

A partir do texto acima e considerando que 6,63 × 10-34 J-s seja o valor da constante de Planck, que 3 × 108 m/s seja a velocidade da luz e que a temperatura em graus Kelvin seja exatamente igual à temperatura em graus Celsius acrescida de 273, julgue o item.
O tungstênio apresenta, em seu estado fundamental de energia, elétrons que ocupam orbitais ƒ.
A base de uma escultura é formada por uma placa de latão, uma liga metálica de zinco (Zn) e cobre (Cu). Para minimizar os problemas relacionados à corrosão provocada pela chuva ácida, a placa foi recoberta com uma fina camada de prata (Ag). O recobrimento foi realizado a partir da eletrólise de uma solução aquosa de AgCl, fixando-se a placa de latão no anodo da célula eletrolítica. A voltagem foi ajustada de forma a se obter corrente constante de 10,0 A.

Átomos de Cu-63 e de Zn-65 têm a mesma quantidade de nêutrons.
Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes a algumas propriedades dos átomos.
( ) Isótonos têm propriedades físicas iguais.
( ) Isóbaros têm propriedades químicas iguais.
( ) Isótopos têm propriedades químicas iguais.
( ) Isóbaros de elementos diferentes têm necessariamente um número diferente de nêutrons.
A sequência correta de preenchimento dos parênteses, de cima para baixo, é