Questões de Vestibular
Sobre transformações químicas em química
Foram encontradas 1.180 questões
Cl + e- → Cl-
Na - e- → Na+
Como resultado dessas transferências de elétrons, os raios iônicos das espécies Cl - e Na+ , quando comparado com seus respectivos raios atômicos, irão, respectivamente
N2(g) + H2(g)
 NH3(g)
NH3(g)Em uma mistura dos três gases, a 480 °C, a constante de equilíbrio é, aproximadamente, igual a 1,5 x 10-5 . Supondo-se que as pressões parciais de N2 e de H2 sejam iguais a 0,6 e 1,0 atm, respectivamente, a pressão parcial de NH3 nessa mistura em equilíbrio, em atm, é igual a
Combustível produzido com etanol e óleos vegetais está pronto para abastecer ônibus e caminhões
Se tudo correr bem, dentro de dois anos os veículos brasileiros movidos a óleo diesel - caminhões, ônibus,
tratores e locomotivas - estarão rodando com um percentual de biodiesel no tanque. Um dos candidatos a esse novo
combustível foi desenvolvido por meio da reação química de óleos vegetais com etanol, o álcool extraído da cana-de-
açúcar, nos laboratórios da Universidade de São Paulo (USP), em Ribeirão Preto. [...] Com as características de ser
totalmente renovável, produzir menos poluentes que o diesel do petróleo e por já existir uma indústria de produção
de álcool no país, a adoção do biodiesel à base de etanol facilita a incorporação desse tipo de combustível à matriz
energética brasileira. [...]
Apesar da eficiência do processo de conversão [...], o biodiesel brasileiro ainda é mais caro do que o diesel
comum.
Os ensaios ficaram a cargo do engenheiro agrícola Afonso Lopes, professor do Departamento de Engenharia
Rural da Faculdade de Ciências Agrárias e Veterinárias (FCAV). [...] Lopes testou o combustível no trator. [...] Quando
o trator funcionou com 100% de biodiesel, o consumo aumentou, em média, 11%”, conta Lopes.
Eduardo Cesar, Revista Fapesp, Edição 94 – Tecnologia – Dez. 2003. Texto adaptado.
Obrigatório desde 1997, o componente reduz as emissões
provenientes da queima de combustível
Na época de frio, a qualidade do ar tende a piorar e, para não tornar a situação ainda mais crítica, é preciso atenção ao catalisador do veículo. A peça pode transformar mais de 90% dos gases tóxicos em derivados menos poluentes. [...]
O principal indício de problemas no catalisador é a perda de potência. “Combustível adulterado provoca a ineficiência da reação química que faz a catálise, o que afeta o rendimento", explica o diretor Associação de Engenharia Automotiva (AEA), Alfredo Castelli.
A cor da fumaça que sai pelo escapamento não está relacionada a defeitos na peça. Nesse caso, indica que há algo de errado com o motor.
Thais Villaça
O Estado de São Paulo, 28.05.14

Desde a década de 70, não há comercialização do minério bruto ou do concentrado de nióbio (pirocloro) no mercado interno ou externo. O metal é vendido, sobretudo, na forma da liga ferro-nióbio (FeNb STD, com 66% de teor de nióbio e 30% de ferro), obtida a partir de diversas etapas de processamento. Segundo o governo, as exportações de ferro-liga de nióbio atingiram em 2012 aproximadamente 71 mil toneladas, no valor de US$ 1,8 bilhão.
(http://g1.globo.com. Adaptado.)

Desde a década de 70, não há comercialização do minério bruto ou do concentrado de nióbio (pirocloro) no mercado interno ou externo. O metal é vendido, sobretudo, na forma da liga ferro-nióbio (FeNb STD, com 66% de teor de nióbio e 30% de ferro), obtida a partir de diversas etapas de processamento. Segundo o governo, as exportações de ferro-liga de nióbio atingiram em 2012 aproximadamente 71 mil toneladas, no valor de US$ 1,8 bilhão.
(http://g1.globo.com. Adaptado.)
A água de coco é considerada uma bebida muito saudável e indicada para reposição de íons após atividades físicas intensas. Em especial, é uma rica fonte de potássio, que contribui para evitar cãibras. Além disso, a água de coco contém açúcares, que fornecem energia para o organismo. Essa bebida não contém quantidades significativas de proteínas e gorduras. Em uma amostra de água de coco de 200 g (aproximadamente um copo), foram encontradas as seguintes quantidades:
Açúcares 8,0 g
Cálcio 40 mg
Sódio 40 mg
Potássio 156 mg
Magnésio 12 mg
Com base nessas informações, é correto afirmar que a água de coco
A Classificação Periódica dos Elementos é importante ferramenta dos químicos. Sobre esse assunto, são feitas as seguintes afirmativas:
I. Os elementos prata e chumbo apresentam, respectivamente, massa atômica aproximada de 108 e 207.
II. Com exceção do hidrogênio, os elementos da extremidade esquerda da tabela periódica são metais de transição.
III. Na tabela periódica atual, os elementos são organizados em função do seu número atômico.
IV. Em geral, elementos representativos de mesmo grupo da tabela periódica apresentam massas atômicas similares.
São corretas somente as afirmativas
Sobre os compostos de cálcio, assinale a afirmativa INCORRETA.
C8H18 (L) + 25/2 O2(g) ➡ 8CO2(g) + 9H2O(L) Δ H0 = -5471KJ
Nestas condições, é CORRETO afirmar que a razão entre as energias gastas em um ano, nessa jornada, pelo automóvel e o estudante na bicicleta, é aproximadamente
Sobre os números quânticos propostos no modelo de Bohr e no modelo da mecânica quântica, é CORRETO afirmar que

O(s) produto(s) da reação de decomposição térmica do carbonato de cálcio é(são).
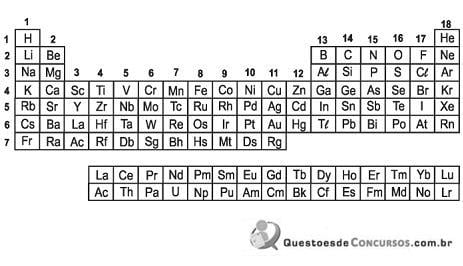
Assinale a alternativa na qual os conjuntos de três elementos ou substâncias elementares estão corretamente associados às propriedades indicadas no quadro abaixo.
I. Gases são facilmente compressíveis, preenchem o espaço disponível e suas moléculas possuem movimento caótico incessante.
II. A energia cinética média das moléculas de um gás é diretamente proporcional à temperatura absoluta.
III. A pressão de um gás é o resultado das colisões das moléculas com as paredes do recipiente.
IV. As moléculas se movimentam sem colidirem com as paredes do recipiente que as contém.
Assinale a alternativa que apresenta informações corretas.
Na0 + H2O
 NaOH + 1/2 H2
NaOH + 1/2 H2Assinale a alternativa que apresenta a classe de reação na qual se enquadra essa transformação.