Questões de Vestibular
Sobre velocidade de reação, energia de ativação, concentração, pressão, temperatura e catalisador em química
Foram encontradas 271 questões

Após uma série de quatro experimentos, o estudante representou os dados obtidos em uma tabela:
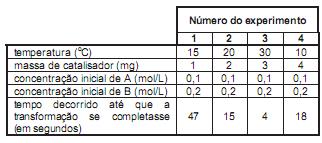
Que modificação deveria ser feita no procedimento para obter resultados experimentais mais adequados ao objetivo proposto?
MgCO3 (s) + 2HCl(aq) → MgCl 2 (aq) + H2 O(L) + CO (g)
Sabendo que a reação ocorre em um sistema aberto, o parâmetro do meio reacional que deverá ser considerado para a determinação da velocidade dessa reação é
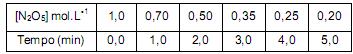
Qual a concentração de [NO2(g) ] em mol.L-1 entre 0 e 2min?
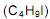 com a água a 25 o C pode ser estudada do ponto de vista da cinética química. A equação da reação é mostrada a seguir:
com a água a 25 o C pode ser estudada do ponto de vista da cinética química. A equação da reação é mostrada a seguir: 
Nessas condições, o HI , que é um dos produtos da reação, comporta-se como um eletrólito forte e solúvel. Dessa forma, pode-se fazer um estudo da cinética dessa reação, medindo-se
A partir dessa informação, é correto afrmar:
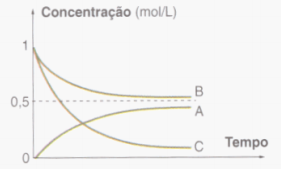
Para este experimento, qual dos gráficos abaixo melhor representa o comportamento dos íons na solução durante o processo. Considere t = tempo em minuto e concentração [ ] = mol/L
2NO(g) + O2(g) → 2NO2(g)
A tabela a seguir apresenta dados obtidos experimentalmente para determinação da cinética de reação do dióxido de nitrogênio à temperatura de 400o C.
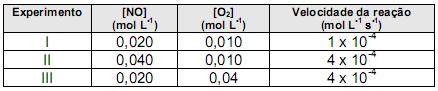
A ordem global da reação é:

A molécula de sacarose, em contato com a água, sofre uma
reação na qual se degrada em moléculas de glicose e frutose,
conforme o esquema acima. Essa reação, conhecida como reação de
inversão da sacarose, é catalisada em meio ácido. A sacarose desvia
o plano da luz polarizada para a direita, e uma mistura equimolar de
glicose e frutose é desviada para a esquerda, podendo o andamento
da reação ser acompanhado por intermédio de um polarímetro, que
mede o desvio da luz polarizada. A figura a seguir apresenta, de
forma esquemática, as curvas de energia potencial para as reações
catalisada e não catalisada de inversão da sacarose.

A partir dessas informações, julgue os próximos itens.

A molécula de sacarose, em contato com a água, sofre uma
reação na qual se degrada em moléculas de glicose e frutose,
conforme o esquema acima. Essa reação, conhecida como reação de
inversão da sacarose, é catalisada em meio ácido. A sacarose desvia
o plano da luz polarizada para a direita, e uma mistura equimolar de
glicose e frutose é desviada para a esquerda, podendo o andamento
da reação ser acompanhado por intermédio de um polarímetro, que
mede o desvio da luz polarizada. A figura a seguir apresenta, de
forma esquemática, as curvas de energia potencial para as reações
catalisada e não catalisada de inversão da sacarose.

A partir dessas informações, julgue os próximos itens.

A molécula de sacarose, em contato com a água, sofre uma
reação na qual se degrada em moléculas de glicose e frutose,
conforme o esquema acima. Essa reação, conhecida como reação de
inversão da sacarose, é catalisada em meio ácido. A sacarose desvia
o plano da luz polarizada para a direita, e uma mistura equimolar de
glicose e frutose é desviada para a esquerda, podendo o andamento
da reação ser acompanhado por intermédio de um polarímetro, que
mede o desvio da luz polarizada. A figura a seguir apresenta, de
forma esquemática, as curvas de energia potencial para as reações
catalisada e não catalisada de inversão da sacarose.

A partir dessas informações, julgue os próximos itens.
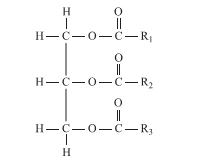
onde
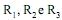 são cadeias abertas de carbono e hidrogênio formadas, em geral, por 13 a 17 átomos de carbono, que po- dem ser iguais ou diferentes, saturadas ou insaturadas, com predominância das insaturadas com até três insaturações. A partir desses óleos, podem ser obtidos diversos produtos de interesse industrial e tecnológico. Como exemplos, considere os seguintes processos:
são cadeias abertas de carbono e hidrogênio formadas, em geral, por 13 a 17 átomos de carbono, que po- dem ser iguais ou diferentes, saturadas ou insaturadas, com predominância das insaturadas com até três insaturações. A partir desses óleos, podem ser obtidos diversos produtos de interesse industrial e tecnológico. Como exemplos, considere os seguintes processos:I. Hidrogenação parcial, catalisada por Ni metálico, formando o produto X.
II. Reação com NaOH, formando glicerol e o produto Y.
III. Reação com
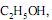 catalisada por KOH, formando glicerol e o produto Z.
catalisada por KOH, formando glicerol e o produto Z.É correto afirmar que os produtos X, Y e Z correspondem, respectivamente, a
NaCl + MnO2 + H2SO4 → Na2SO4 + Cl2 + H2O
Sabendo que a mesma teve um rendimento de 80% e foi realizada a uma temperatura de 27 °C e a uma pressão de 1 atm e que utilizou 600 g de NaCl, o volume de Cl2 obtido, em litros, foi, aproximadamente,
Na tabela a seguir, são apresentadas informações contidas na bula de comprimidos sólidos de ibuprofeno.
cada comprimido contém
ibuprofeno____|___ 300 mg
excipientes ___|___ ácido cítrico, benzoato de sódio,dióxido de titânio e amido
Assinale a opção que apresenta o gráfico que melhor representa a variação da temperatura em função do tempo para um comprimido que tenha a composição mostrada na tabela e tenha sido macerado e aquecido.
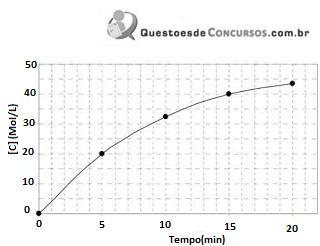
Considerando-se que a curva a seguir represente a variação da concentração de C em função do tempo para a reação química A + 3B ? 2C, é correto afirmar que, no intervalo de 0 a 5 min, a velocidade média da reação é 2,0 mol/L min.
( ) O processo que ocorre no cano de descarga dos veículos automotivos é uma catálise homogênea.
( ) Óxidos de nitrogênio, oriundos das descargas dos veículos, são responsáveis pela névoa fotoquímica.
( ) O conversor catalítico oxida o CO e hidrocarbonetos não queimados, transformando-os em dióxido de carbono e água.
( ) O conversor catalítico reduz os óxidos de nitrogênio a nitrogênio gasoso.
( ) Os conversores catalíticos eliminam totalmente a poluição atmosférica causada pelos gases liberados na descarga dos veículos automotivos.
A sequência correta, de cima para baixo, é


