Questões Militares
Sobre teoria atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica em química
Foram encontradas 170 questões
Observe as configurações eletrônicas dos elementos químicos I, II e III em suas camadas de valência.
I - 3s2 3p1
II - 4s2 4p3
III- 4s2 4p5
Com base nas configurações eletrônicas desses três elementos químicos, assinale a opção correta.
Uma análise dessas equações permite afirmar que:
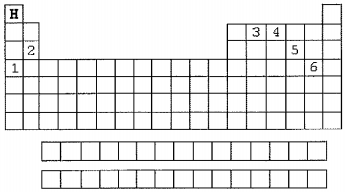
Analise as afirmativas abaixo referentes a esse esboço.
I - O elemento representado por 5 apresenta variantes alotrópicas quando forma moléculas de substâncias compostas.
II - A quantidade de elétrons que o elemento representado por 1 ganha é a mesma que aquele representado por 6 perde quando ambos sofrem ionização.
III- O elemento representado por 3 forma ligações covalentes quando se liga ao hidrogênio.
IV - O elemento indicado por 4 forma a substância simples mais abundante na atmosfera terrestre, e o elemento indicado por 2 faz parte da composição dos ossos humanos.
Assinale a opção correta.
Para uma molécula diatômica, a energia potencial em função da distância internuclear é representada pela figura ao lado. As linhas horizontais representam os níveis de energia vibracional quanticamente permitidos para uma molécula diatômica. Uma amostra contendo um mol de moléculas diatômicas idênticas, na forma de um sólido cristalino, pode ser modelada como um conjunto de osciladores para os quais a energia potencial também pode ser representada qualitativamente pela figura. Em relação a este sólido cristalino, são feitas as seguintes proposições:
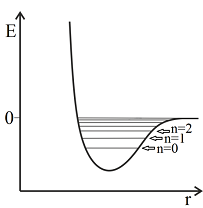
I. À temperatura de 0 K, a maioria dos osciladores estará estado vibracional fundamental, cujo número quântico vibracional, n, é igual a zero.
II. À temperatura de 0 K, todos os osciladores estarão no estado vibracional fundamental, cujo número quântico vibracional, n, é igual a zero.
III. O movimento vibracional cessa a 0 K.
IV. O movimento vibracional não cessa a 0 K.
V. O princípio de incerteza de Heisenberg será violado se o movimento vibracional cessar.
Das proposições acima estão CORRETAS
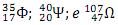
marque a alternativa correta, considerando-se as condições de 1 atm e 25 ?.
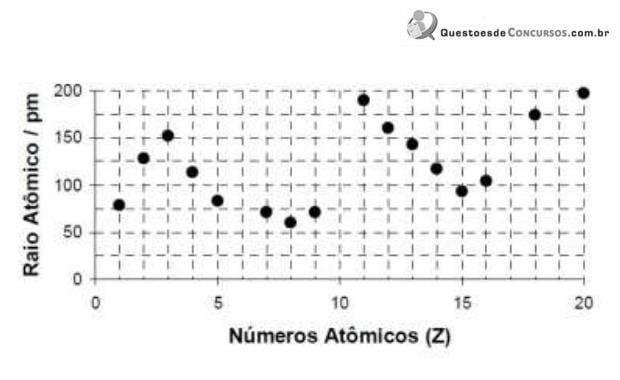
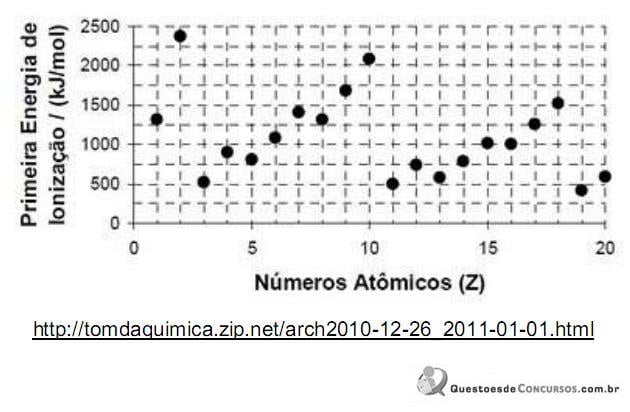
A explicação para o fato de a primeira energia de ionização do elemento sódio ser menor do que a do elemento fósforo é:
Com base nas informações acima e na tabela periódica, incluída no final deste caderno de provas, julgue os itens a seguir.
Para combater a classe de incêndios gerados por esses materiais, deve-se empregar um extintor de pó químico elaborado à base de cloreto de sódio (NaCl).
Considerando o texto acima e os múltiplos aspectos que ele suscita, julgue os itens a seguir, utilizando, caso necessário, a tabela periódica inserida no final deste caderno de provas.
Entre os metais citados no texto, aquele que apresenta maior energia de ionização é o alumínio.
K( s) + H2O( l) → KOH( aq) + H2(g)
Ba(s) + O2(g) → BaO(s)
Para combater a classe de incêndios gerados por esses materiais, deve-se empregar um extintor de pó químico elaborado à base de cloreto de sódio (NaCl).
Considerando o texto acima e os múltiplos aspectos que ele suscita, julgue os itens a seguir, utilizando, caso necessário, a tabela periódica inserida no final deste caderno de provas.
No material base que compõe o pó químico dos extintores utilizados contra incêndios classe D, a espécie química cloro apresenta a configuração eletrônica 1s 2 2s 2 2p6 3s 2 3p5 , conforme o diagrama de Linus Pauling.
Um experimento clássico indica que o oxigênio molecular (O2) exibe propriedades magnéticas no seu estado fundamental. O experimento consiste em fazer passar oxigênio líquido pelos polos de um ímã. Observa-se que o oxigênio fica retido, como mostra a figura a seguir:
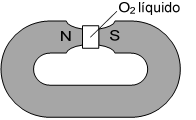
Nas alternativas abaixo, são apresentados os orbitais 2p de dois átomos de oxigênio e o spin dos elétrons que ocupam seus orbitais atômicos. Também são apresentadas possíveis interações químicas que podem resultar em ligações químicas estabelecidas entre esses dois átomos.
Considerando a observação experimental e os requisitos eletrônicos e energéticos para o
estabelecimento de ligações químicas, indique qual das alternativas abaixo representa melhor o O2 no
estado fundamental.
Em 19,9 g de um sal de cálcio encontra-se 0,15 mol desse elemento. Qual a massa molar do ânion trivalente que forma esse sal?
Dado: Ca = 40 g/mol.