Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.139 questões
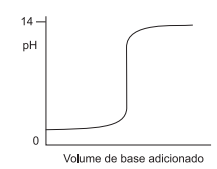
Considere a curva de titulação produzida quando uma base forte é adicionada a um ácido forte.
O pH da solução, quando 50 mL da base forte de concentração de 0,1 mol/L são adicionados a 51 mL do ácido forte de concentração de 0,1 mol/L, é de
Um químico dispõe de duas soluções estoque de NaC, uma de 1,7 mol/L (solução I) e outra de título 25% e densidade 2 g/mL (solução II), para preparar 500 mL da solução de cloreto de sódio 10% p/v.
Os volumes das soluções I e II para o preparo da solução desejada, quando usados separadamente são, respectivamente,
Dado:1 mol de NaCl corresponde a 58, 5 g de Nacl
I. Precisão e exatidão têm o mesmo significado.
II. Limite de detecção é a menor concentração do analito que pode ser quantificada.
III. A linearidade correlaciona a resposta do método de quantificação com concentração conhecida da substância a ser analisada.
IV. A seletividade avalia o grau de interferência de outros ingredientes na amostra.
Assinale:
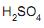 em peso; densidade 1,727 g/mL.
em peso; densidade 1,727 g/mL. A partir dessa identificação, conclui-se que a molaridade dessa solução é, aproximadamente, igual a
I – Sais são compostos formados por ânions provenientes de bases e por cátions provenientes de ácidos.
II – A maioria dos óxidos dos elementos fortemente eletronegativos tem caráter básico.
III – Os óxidos dos elementos fracamente eletronegativos apresentam ligação tipicamente iônica.
Está correto o que se afirma em

Sobre uma bancada de laboratório, há dois frascos com soluções aquosas de hidróxido de sódio com concentrações diferentes: um com uma concentração igual a 0,4 g/L, e outro com concentração de 0,2 g/L, como ilustrado na figura acima.
A transferência de 100 mL do frasco 1 e 200 mL do frasco 2 para um cilindro graduado, seguida da adição de água destilada até completar o volume de 1,0 L e da homogeneização completa, dá origem a uma solução cuja concentração de Na+, em mol/L, é igual a
Na2CO30,120mol/L.
A massa aproximada, em g, de Na2CO3 contida em 200 mL dessa solução é igual a Dado: M(Na2CO3) = 106 g/mol
(Dados: Massas molares, em g/mol: H – 1; Cl – 35,5)
I – O CrO é um óxido básico.
II – O Cr2O3 é um óxido ácido.
III – O CrO3 é um óxido anfótero.
IV– A ordem crescente de acidez é dada por CrO < Cr2O3 < CrO3.
Estão corretas APENAS as afirmativas
(Dados: Massas molares em g/mol: H2SO4 = 98; NaOH = 40; Mg = 24; Ca = 40; Fe = 56; Zn = 65; Pb = 207)



