Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.219 questões
2KNO3(s) + S(s) + 3C(s)-> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
O nitrato reage com a água conforme a reação NO3 – + H2O -> 6 HNO3 + OH– , aumentando significativamente o pH da solução formada, haja vista que o caráter básico do OH– é mais forte que o caráter ácido do NO3 – .
Os principais diagramas de classificação química das águas subterrâneas (Piper, Stiff e Schoeller) apresentam a concentração dos principais elementos em mg/L.
Levando em conta o produto formado na reação com a água, o CO2 é classificado como óxido
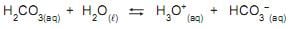
Se, a 200 mL dessa solução são adicionados aproximadamente 2 mL de solução aquosa de NaOH, 0,1 mol/L, ocorre a(o)
Abaixo está representada a reação de combustão do metanol:
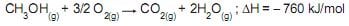
Na combustão completa de 1,0 L de metanol, no estado gasoso, a quantidade de energia liberada, em kJ, é, aproximadamente, igual a
Sendo o NaCl um eletrólito forte (dissolvido se dissocia por completo), a concentração de Na+, em mol/L, no soro é, aproximadamente, igual a
Dado
M(NaCl) = 58,5 g/mol
Dado
M(H2 SO4 ) = 98 g/mol
NaCl ↔ Na+ + Cl-
MgSO4 ↔ Mg2+ + SO42-
CaCl2 ↔ Ca2+ + 2Cl-
Analise as seguintes afirmativas e assinale a alternativa correta.
I. Os íons transportam cargas positivas ou negativas.
II. Visto que uma solução é eletricamente neutra, o número total de cargas positivas na solução deve ser igual ao número total de cargas negativas.
III. As moléculas desses eletrólitos, quando dissolvidas em água, se dissociam em átomos ou agrupamentos de átomos carregados.
IV. As moléculas conduzem a corrente elétrica por deslocamento em solução em direção ao cátodo e ânodo.
Estão corretas apenas as afirmativas:
Quanto maior for o valor da constante de ionização básica, maior será o valor do pH.
A ionização do ácido sulfídrico (H2S), constituído de dois hidrogênios ionizáveis, ocorre em duas etapas e apresenta duas constantes de ionização que têm o mesmo valor.
A fração em massa de sacarose no soro caseiro equivale a 40,0%.
A concentração de sacarose no soro caseiro é inferior a 0,10 mol/L.
(Adaptado de: Revista Pesquisa FAPESP n. 198. Disponível em: http://agencia. fapesp.br/16030. Acesso em janeiro de 2013.)
O óxido citado no texto pode ser classificado como:
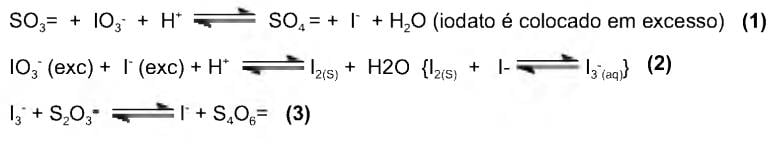
2 S2O32-
 S4O62- + 2e-
S4O62- + 2e-Para proceder a essa análise, é necessária a utilização dos reagentes a seguir, EXCETO.
Mn04- + Fe 2+ + H+ —> Mn 2+ + Fe3+ + H20
Quantos mililitros de uma solução 0,0240 mol L-1 são necessários para titular 20,00mL de uma solução 0,112 mol L-1 em Fe2+ .