Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.239 questões
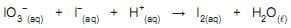
Nessa reação, o
É uma propriedade da função química inorgânica:
I. A densidade também pode ser considerada como sendo 9,00.102 g/L.
II. Se um rótulo informa que tem 50,0Kg de etilenodiamina, então, o volume da embalagem tem que ser maior do que 100L.
III. É possível considerar que o teor de etilenodiamina é 90,0%(m/v).
IV. A concentração da solução de etilenodiamina pode ser considerada como sendo 15,0mol/L.
É correto o que se afirma em
Equação 1:
NH4 + (aq) + OH- (aq)
 NH3(aq) +H2O(l)
NH3(aq) +H2O(l) Equação 2:
HSO4 - (aq) + HCO3-(aq)
 SO4 2- (aq) + H2CO3(aq)
SO4 2- (aq) + H2CO3(aq) São pares de base e base conjugada de Bronsted-Lowry, respectivamente, em cada equação:
Na2S2O3(aq)+ I2(aq) → Na2S4O6(aq)+ NaI(aq)
Diante do exposto, assinale a alternativa que apresenta a concentração de iodo presente na solução estoque.
Os íons de maior e de menor prioridade de descarga são, respectivamente,
NaHCO3(s) + HC2 H3 O2(aq) → NaC2 H3O2(aq) + H2 O(l) + CO2(g)
Nessa reação, o
Dado Massa molar do NaOH = 40 g/mol
Nessas condições, a concentração de NaOH, em g/L, na solução comercial é
• seu cátion corresponde ao elemento químico de maior raio atômico do bloco s da tabela de classificação periódica dos elementos;
• seu ânion corresponde ao elemento químico de maior energia de ionização do grupo VIIA da tabela de classificação periódica dos elementos.
A fórmula mínima desse sal é
A fórmula química do ânion desse sal é
A concentração, em mol/L, da solução diluída é igual a
Dado
massa molar do H2 SO4 = 98 g/mol
Supondo que essa contaminação da água seja por um monoácido, a concentração desse monoácido, em mol/L, encontrada na água dessa caixa é igual a
A concentração dos íons acetato e o pH da solução ácida serão, respectivamente,
Cl2 + 2NaOH ? NaCl + H2O + NaClO
O outro método de produção é a eletrólise de uma solução concentrada de cloreto de sódio, com o que se obtêm o mesmo produto.
Sobre esse segundo método de produção do hipoclorito de sódio, assinale a alternativa CORRETA.
( 1 ) NaOH 0,1 mol/L
( 2 ) NaOH 3%
( 3 ) NaOH 50 mM
( 4 ) NaOH 5 g/L
( ) Diluir 25 µL de uma solução a 3 mol/L e diluir até 100 µL.
( ) Diluir 50 mL de uma solução a 16 g/L até 200 mL.
( ) Diluir 10 mL de uma solução a 1,25 mol/L até 100 mL.
( ) Diluir 2 mL de solução a 25 % até 250 mL.
A ordem CORRETA de associação, de cima para baixo, é: