Questões de Concurso
Sobre substâncias inorgânicas: dissociação iônica e ionização, conceitos de ácido-base. em química
Foram encontradas 373 questões
A respeito de ácidos e bases, julgue o item a seguir.
O BF3 é uma base de Lewis porque o elemento boro (B)
pode receber um par de elétrons.
A respeito de ácidos e bases, julgue o item a seguir.
Um ácido de Brønsted é um receptor de próton.
reação 1: HCO2H (l) + H2O (l) ⇌ H3O+ (aq) + HCO2 – (aq) reação 2: CH3NH2 (l) + H2O (l) ⇌ CH3NH3 + (aq) + OH– (aq)
A partir dessas informações, assinale a opção que apresenta os pares conjugados ácido/base para as reações 1 e 2, respectivamente, considerando a reação direta, ou seja, o reagente ácido e sua respectiva base conjugada.
Os diversos componentes presentes na água, que alteram seu grau de pureza, podem ser retratados em termos de suas características físicas, químicas e biológicas. Essas características podem ser traduzidas na forma de parâmetros de qualidade da água. Acerca desse assunto, julgue o item seguinte.
Alcalinidade é a concentração de cátions multimetálicos em
solução, como os divalentes Ca2+ e Mg2+.
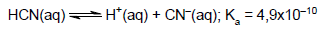
Considerando a equação que representa o equilíbrio desse ácido e sua constante de equilíbrio, conclui-se que esse ácido apresenta solução aquosa
Hcl↔H+ + Cl- (K = 1,0.10 +7)
H2SO4 ↔H+ + HSO4 - (Ka = 1,0.10 +3)
H2CO3 ↔H+ + HCO3 - (Ka = 4,3.10 -7)
I - O ácido clorídrico é o que apresenta maior ionização. II - O ácido carbônico é um ácido mais forte que o ácido sulfúrico. III- A ordem de acidez para essas substâncias é HCl > H2SO4 > H2CO3 IV - O ácido sulfúrico possui uma maior tendência em liberar íons H+ que o ácido clorídrico.
Estão corretas:
Coluna - 1 (pares de substâncias) (I) Cloreto de sódio e glicose (II) Naftaleno e sacarose (III) Nitrato de sódio e bicarbonato de sódio
Coluna - 2 (testes) (X) pH de suas soluções aquosas (Y) Dissolução em água (Z) Condutividade de suas soluções aquosas
Quais os testes (Coluna - 2) devem ser usados para distinguir os pares de substâncias em I, II e III, (Coluna - 1), respectivamente.
Acerca de eletroquímica e de processos de oxidação e redução, julgue o item
ma substância cujas soluções aquosas contêm íons é
chamada de eletrólito. Uma substância que não forma
íons em solução é chamada não eletrólito. Por exemplo,
as diferenças entre soluções contendo cloreto de sódio
e sacarose devem‐se, em grande parte, ao fato de o NaCl
ser iônico, enquanto o C12H22O11 é molecular.
Julgue o item, relativos a ácidos e bases.
Um exemplo simples de uma reação ácido‐base é a
reação de um próton com o íon hidróxido. Nessa reação,
o íon hidróxido é um ácido de Lewis porque recebe o par
de elétrons que se torna compartilhado com o
hidrogênio.
Julgue o item, relativos a ácidos e bases.
Pela definição de Brønsted‐Lowry, um ácido é uma
substância doadora de prótons em água e uma base é
uma substância receptora de prótons em água. Pela
definição de Lewis, um ácido é uma substância que pode
doar um par de elétrons para formar uma ligação. Uma
base de Lewis é definida como uma substância que pode
aceitar um par de elétrons para a formação de uma
ligação covalente.
Acerca das propriedades e reações características de hidretos, ácidos, hidróxidos, óxidos e sal, julgue o item
Em uma reação de neutralização, ou reação ácido‐base,
íons hidrogênio de um reagente ácido reagem com íons
hidróxido de uma base, formando água.
I Ácido é uma espécie química capaz de receber um par eletrônico e base é uma espécie química capaz de doar um par eletrônico. II Ácido é uma substância que, em água, produz, como cátion, apenas íons H+, e base é uma substância que, em água, produz, como ânion, apenas íons OH!. III Ácido é uma espécie que reage com bases para formar sais, doando cátions ou aceitando ânions ou elétrons, e base é uma espécie que reage com ácidos para formar sais, doando ânions ou elétrons ou combinando-se com cátions. IV Ácido é um doador de prótons e base é um receptor de prótons.
Assinale a opção que apresenta a seqüência correspondente aos conceitos de ácido e base de Arrhenius, de Lowry e Brönsted e de Lewis, respectivamente.
PORQUE
HBr e HI transferem de forma praticamente completa os seus prótons para a água, formando H₃O+.
A esse respeito conclui-se que
O Ca(OH)2 é ____________, ou seja, em solução aquosa está ____________.