Questões de Concurso
Sobre substâncias inorgânicas: dissociação iônica e ionização, conceitos de ácido-base. em química
Foram encontradas 373 questões
A respeito das funções inorgânicas, julgue o item.
Em solução aquosa, o ácido iodídrico é mais forte que o ácido clorídrico.
A respeito das funções inorgânicas, julgue o item.
Um ácido fraco ioniza‑se completamente em solução aquosa.
A respeito das funções inorgânicas, julgue o item.
Na definição de Bronsted‑Lowry, ácido é um aceitador de prótons.
Dado: log 9 = 0.96
Dado: Densidade da solução = 1,0 g/mL
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
Admitindo-se que há completa dissociação dos solutos, a concentração de íons K+ , em mol L-1 , na solução formada é igual a
[Ni(NH3)6]SO4; [CoCl2(NH3)4]Cl; K4[Fe(CN)6]; [Mn(CN)6]4-; [Fe(Cl)4]2-; [Co(Cl)3(NH3)3]
(i) um ácido forte for adicionado?
(ii) uma base forte for adicionada?
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
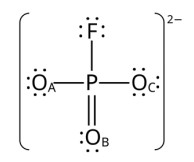
Ao se calcular as cargas formais de cada átomo na estrutura apresentada, conclui-se que são nulas, com exceção dos átomos:
Coluna 1 Substâncias Inorgânicas
1. Al2(SO4)3 2. HNO3 3. NaClO 4. H2CO3 5. BaSO4
Coluna 2 Aplicações
( ) Em água mineral gaseificada ( ) Como desinfetante e alvejante ( ) No tratamento de águas ( ) Contraste em radiografias ( ) Na fabricação de fertilizantes e explosivos
Assinale a alternativa que indica a sequência correta, de cima para baixo.
( ) Deve-se adicionar lentamente a água no ácido e nunca ao contrário, a fim de evitar uma reação violenta.
( ) A adição de ácido sobre a água faz a temperatura aumentar rapidamente, podendo haver uma pequena explosão, espirrando ácido na pessoa e/ou podendo até mesmo quebrar o recipiente que contém a solução.
( ) Devem-se utilizar luvas, óculos de proteção ou proteção facial e jaleco, sendo dispensado o uso de capela se tiver próximo a um lava-olhos e a um chuveiro de segurança.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Qual a concentração da solução de hidróxido de potássio para neutralizar completamente o ácido?
Considere a massa molar do HNO3 igual a 63 g/mol e a massa molar do KOH igual a 56 g/mol.
CH3COOH(aq) ⇄ CH3COO- (aq) + H+ (aq)
Dado: pH = -log [H+]
Suponha que foi preparada, em laboratório, uma solução aquosa de ácido acético 0,2 mol L-1. O pH dessa solução possui valor aproximado de
1 - pH = - log [ H+ ] 2 - pH = pOH = 7
3 - pOH = - log [OH- ]
4 - pH menor 7 e pOH maior 7
5 - pH maior 7 e pOH menor 7
( ) Soluções básicas. ( ) Soluções ácidas.
( ) Potencial hidroxiliônico da solução.
( ) Potencial hidrogeniônico da solução.
( ) Água pura (ou soluções neutras).
( ) O indicador alaranjado de metila no meio ácido a cor fica laranja e no meio básico a cor fica amarela com seu pH variando de 3,1 a 4,4.
( ) O indicador azul de bromotimol no meio ácido a cor fica amarela e no meio básico a cor fica azul com seu pH variando de 6,0 a 7,6.
( ) O indicador vermelho de metila no meio ácido a cor fica incolor e no meio básico a cor fica rosa com seu pH variando de 8,3 a 10,0.
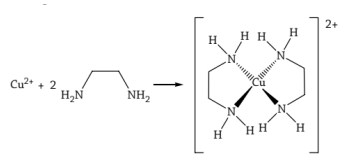
Fonte: https://www2.ufjf.br/quimicaead/wp - content/uploads/sites/224/2013/09/QI_Aula4