Questões de Concurso
Sobre substâncias inorgânicas: dissociação iônica e ionização, conceitos de ácido-base. em química
Foram encontradas 389 questões
Com relação à classificação dos materiais em misturas ou substâncias, assinale a alternativa CORRETA.
Considere as equações I, II e III apresentadas abaixo:
I) CHO2 - (aq) + H2O(l) ⇄ HCOH2(aq) + OH- (aq)
II) HSO4 - (aq) + HCO3 - (aq) ⇄ SO4 2- (aq) + H2CO3(aq)
III) HSO3 - (aq) + H3O + (aq) ⇄ H2SO3(aq) + H2O(l)
De acordo com o conceito de ácido/base de Bronsted e Lowry, é CORRETO afirmar que na equação:
As substâncias químicas citadas a seguir possuem características próprias e podem sofrer modificações, à medida que interagem entre si e com outras substâncias.
H2O |
CO |
HF |
H2SO4 |
NH3 |
Com relação a essas substâncias é CORRETO afirmar:
Considere as afirmativas com relação às propriedades físicas e químicas dos elementos do grupo I da Tabela Periódica.
I) Apresentam baixo potencial de ionização.
II) Todos reagem com água formando hidróxidos, liberando o gás hidrogênio.
III) O ponto de fusão e ebulição cresce de baixo para cima.
IV) À temperatura ambiente (25oC), todos são sólidos.
É CORRETO afirmar que:
Com relação aos conceitos de misturas e soluções marque a alternativa ERRADA.
O óxido nitroso está sendo usado como sedativo em tratamento odontológico. Esse se constitui em uma experiência que provoca medo, ansiedade e estresse em muitas pessoas. Analise as afirmativas seguintes, relacionadas aos óxidos e marque a alternativa CORRETA.
I. O peróxido de hidrogênio em solução aquosa é vendido no comércio com o nome de água oxigenada.
II. Os óxidos ácidos não apresentam caráter covalente.
III. Os óxidos neutros não apresentam reatividade diante da água, de ácidos ou bases.
IV. Os óxidos anfóteros são aqueles que têm um comportamento que pode variar de acordo com a substância a que forem adicionados.
As misturas homogêneas são denominadas soluções. Do ponto de vista prático, consideramos que as soluções são formadas de um solvente e um ou mais solutos. Analise as afirmativas seguintes, relacionadas às soluções e marque a alternativa CORRETA.
I. Material homogêneo é aquele que possui uma única fase, ou seja, é monofásico.
II. Material ou sistema heterogêneo é aquele que possui duas ou mais fases.
III. As dispersões coloidais sofrem sedimentações somente pela ação de uma ultracentrífuga.
Relacione a Coluna 1 à Coluna 2, associando o tipo de reação química com a respectiva equação.
Coluna 1
1. Reação de neutralização.
2. Reação de precipitação.
3. Reação de oxirredução
Coluna 2
( ) Cu(s) + 4HNO3(aq) -> Cu(NO3)2(aq) + 2H2O(l)+2NO2(g)
( ) Mg(NO3)2(aq) + 2NaOH(aq) -> Mg(OH)2(s) + 2NaNO3(aq)
( ) 2HNO3(aq) + Ca(OH)2(s) -> 2H2O(l) + Ca(NO3)2(aq)
( ) Mg(s) + 2HCl(aq) -> MgCl2(aq) + H2(g)
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
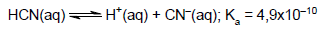
Considerando a equação que representa o equilíbrio desse ácido e sua constante de equilíbrio, conclui-se que esse ácido apresenta solução aquosa
O quadro abaixo representa os equilíbrios ácido-base entre o ácido sulfuroso e amônia em solução aquosa.
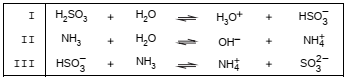
De acordo com a teoria de Brönsted-Lowry,
Ao reagir com água, o óxido nitroso apresenta o comportamento de
Em 1923, o químico dinamarquês Johannes Brønsted (1879- 1947) e o químico inglês Thomas Lowry (1874-1936) propuseram uma definição de ácidos e bases mais geral do que a proposta anteriormente por Arrhenius (1859-1927).
O conceito de Brønsted- Lowry está baseado no fato de que a reação ácido-base envolve transferência de íons H+ de uma substância para outra.
Analise o equilíbrio a seguir:
HSO3 – (aq)+ H2O(ℓ) ⇄ H2SO3(aq) +OH– (aq)
Baseado nesse conceito, os pares conjugados são:
Acerca das teorias ácido-base e tampão são feitas as seguintes afirmações:
I. Segundo a teoria de Arrhenius ácidos e bases são classificados segundo sua capacidade de doar e receber prótons.
II. Quanto maior o valor da constante de ionização de uma base, maior será o valor do pH da solução.
III. Para uma solução de amônia que apresenta concentração dos íons OH- igual a 10-3 mol L-1, o pH é igual a 3.
IV. Um sistema tampão pode ser formado por um ácido forte e sua base conjugada.
V. Dobrando a concentração de ácido e sua base conjugada, que formam a solução tampão, o pH permanece constante, porém o poder tamponante aumenta.
É CORRETO o que se afirma em:
Analise as afirmativas abaixo sobre a classificação e propriedades dos óxidos, julgue se são VERDADEIRAS (V) ou FALSAS (F) e marque a alternativa que contém a sequência CORRETA.
( ) Os óxidos ácidos formam ácido quando reagem com água, e quando reagem com base formam sal e água.
( ) Óxidos neutros não reagem nem com água, ácido ou base. Podemos citar como exemplos de óxidos neutros o CO e o CO2.
( ) O óxido de cálcio, CaO, também chamado de cal viva, é um exemplo de óxido básico. Quando o CaO reage com a água, é formado o hidróxido de cálcio, Ca(OH)2, também chamado de cal hidratada ou cal extinta.
( ) O dióxido de enxofre é um óxido ácido e é um dos óxidos contribuintes para a chamada chuva ácida.
X, Y e Z representam genericamente três ácidos que, quando dissolvidos em um mesmo volume d’água, à temperatura constante, comportam-se de acordo com a tabela:

Considere as afirmações em relação aos três ácidos:
I- X representa o maior grau de ionização.
II- Y representa o ácido mais forte.
III- Z representa o ácido mais fraco.
Está(ão) correta(s) a(s) afirmativa(s)
A iodometria é um método analítico indireto de titulação de iodo. Dentre os reagentes envolvidos, temos o triiodeto, que se forma segundo a reação em equilíbrio representada a seguir:
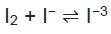
Ao analisar a equação dada e as propriedades químicas das espécies participantes, é correto afirmar
que