Questões de Concurso
Sobre termodinâmica: energia interna, trabalho, energia livre de gibbs e entropia em química
Foram encontradas 111 questões
Caso o petróleo extraído de um poço esteja armazenado em um tanque metálico por um tempo longo e suficiente para que esse petróleo esteja em equilíbrio térmico com as paredes do tanque e o meio externo, então, nessa situação, não haverá trocas de energia térmica entre o petróleo e o meio externo.
Uma estratégia que permite retirar as tampas metálicas de conservas de vidro é o resfriamento da tampa, se o coeficiente de dilatação linear da tampa metálica for superior ao do vidro.

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
O termo “deslocamento hipsocrômico” é usado para
descrever a mudança da banda de absorção para
regiões do espectro onde o comprimento de onda
é maior

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
O termo “deslocamento batocrômico” é utilizado
para descrever a mudança da banda de absorção para
regiões do espectro onde a energia é menor.

Internet:<www.tabelaperiodica.org>
Em relação à termodinâmica química, julgue o item.
Em uma reação química realizada à pressão constante,
quando o sistema libera 60 kJ.mol‑1 de energia na
forma de calor (Q) e realiza 10 kJ.mol‑1 de trabalho
de expansão (W), a variação da energia interna é
de ‑70 kJ.mol‑1.

Internet:<www.tabelaperiodica.org>
Em relação à termodinâmica química, julgue o item.
A primeira lei da termodinâmica afirma que a energia
total em um sistema isolado é constante, podendo
apenas ser transformada de uma forma para outra.

Internet:<www.tabelaperiodica.org>
Em relação à termodinâmica química, julgue o item.
Toda transformação isocórica ocorre com pressão
constante.
“A energia livre de Gibbs é uma grandeza termodinâmica notável”. A entropia é considerada uma função de estado assim como a entalpia. Considerando a síntese da amônia a partir de N2(g) e H2(g) a 298 K conforme equação a seguir:
(BROWN; LEMAY; BURSTEN, Química: a ciência central, São Paulo: Pearson Prentice Hall, 2005, p. 702)
N2(g) + 3 H2(g) → 2 NH3(g)
E conhecendo as informações do quadro abaixo:
Substância |
ΔHºf(kJ.mol-1) |
Sº (J.mol-1.k-1) |
N2(g) |
0 |
191,5 |
H2(g) |
0 |
130,6 |
NH3(g) |
–80,3 |
111,3 |
Podemos afirmar, com base nos dados apresentados, que o valor da variação da energia livre de Gibbs para a síntese da amônia, em kJ.mol-1, é aproximadamente:
https://www.ecycle.com.br/bom-ou-ruim-usado-como-conservante-em-vinhos-dioxido-de-enxofrepode-causar-reacoes-alergicas/ (adaptado) acessado:2109/2023.
Ao se atacar 1,04 kg de sulfito de magnésio, com ácido clorídrico, qual o volume de anidrido sulfuroso obtido a 27°C e 1869 mmHg?
Em um laboratório, foram realizadas quatro réplicas de uma análise de cromo em uma liga metálica, obtendo-se os seguintes valores: 14 mg g-1 , 10 mg g-1 , 16 mg g-1 e 12 mg g-1 .
Para esse conjunto de dados, o desvio-padrão, em mg g-1 , encontra-se na faixa entre
Baseado no tamanho e no grau de espalhamento de luz incidente, calculou-se em 1 × 10-5 mol L-1 a concentração de AgNP na dispersão. A partir do tamanho médio, determinou-se que haveria 500 átomos de Ag por nanopartícula.
Considerando-se esses dados, verifica-se que a massa de prata, em mg, presente em 1 mL de dispersão é
Dado 1 mol = 6 x 1023 unidades M (Ag) = 108 g mol-1
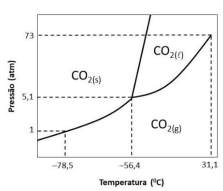
(*diagrama não desenhado em escala)
A partir das informações apresentadas avalie se as afirmativas a seguir são verdadeiras (V) ou falsas (F).
( ) Sob a condição de 5,1 atm e –56,40C prevalece o equilíbrio entre as fases sólida e gasosa.
( ) Sob a condição de 1,0 atm e –78,50C ocorre o ponto crítico para dióxido de carbono.
( ) Sob a condição de 73,0 atm e 31,1 atm ocorre o ponto de sublimação do dióxido de carbono.
As afirmativas são, respectivamente,
Considere as três reações abaixo:
(1) Ca(s) + ½O2 (g) ⇋ CaO(s)
(2) C12H22O11(s) + 12O2 (g) → 12CO2 (g) + 11H2 O(l)
(3) N2
(g) + 3H2
(g) → 2NH3
(g)
Sobre os valores esperados da variação da
entropia padrão das reações (∆r
S°), podemos dizer que:
Note que a absorvância não é uma quantidade medida diretamente, mas é obtida por meio de cálculo matemático a partir dos valores de transmitância.
Assinale a opção que apresenta a relação matemática que define corretamente a absorvância.
Quanto maior o número de partículas na amostra, maior será ______ da radiação incidente e, portanto, menor será a quantidade de radiação incidida no detector.
Assinale a opção que preenche corretamente a lacuna do fragmento acima.
A variação de energia livre relacionada à reação de combustão do etanol, apresentada pela equação a seguir, é mais próxima do comportamento descrito pela seguinte letra (correspondente no gráfico):
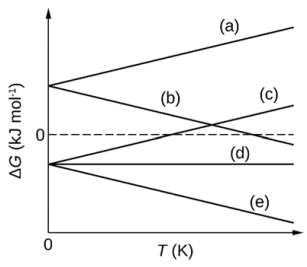
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(g)
Se a ANM se comportar como um vaso perfeitamente adiabático, não ocorrerá trocas de calor entre ela e o meio externo.
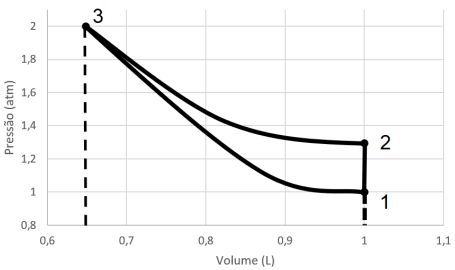
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale
Pedro mora em Campos do Jordão, cidade situada a cerca de 1600m de altitude. Ao visitar sua tia que mora em Praia Grande, no litoral, aqueceu água para preparar café.
Pedro observou que a temperatura de ebulição da água na Praia Grande é _____________ ele observa na ebulição da água em Campos do Jordão, pois em maior altitude, a pressão atmosférica _____________.
As lacunas são preenchidas, correta e respectivamente, por:
No fenômeno de transferência de massa para uma mistura gasosa binária formada pelos gases A+B, o fluxo molar do componente A na direção z (NA, mol.s-1.m-2) pode ser calculado pela expressão:
NA=NA+NBNA. zDAB . c. ln [(NA+NBNA)−(ccA1)(NA+NBNA)−(ccA2)]
Essa equação é aplicada para difusão na direção de z com NA e NB constantes e em estado estacionário. Nesse contexto, assinale a opção CORRETA.