Questões de Química - Transformações Químicas e Energia para Concurso
Foram encontradas 1.421 questões
A corrosão é definida como a deterioração de um material, geralmente metálico, em virtude da ação do meio ambiente que o modifica por meio de um processo espontâneo. Isso pode acarretar a inutilização de estruturas de uso corrente no dia-adia.
É corrente vermos estruturas metálicas espalhadas por toda parte, seja nos meios de transporte como automóveis, caminhões, navios ou aviões, ou em gasodutos, adutoras, entre outros. Todos esses objetos ou aplicações metálicas sofrem a ação do meio, tornando-se, com o passar do tempo e com a corrosão, inadequados ao seu uso, com grandes prejuízos.
(Fonte: http://www.searadaciencia.ufc.br/sugestoes/quimica/quimica003.htm.)
A corrosão do ferro pode ser descrita pela reação:
A medicina nuclear envolve dois usos distintos de radioisótopos: terapia e diagnóstico. No uso terapêutico, a radiação é empregada na tentativa de curar doenças. Algumas formas de câncer, por exemplo, podem ser tratadas por radioterapia (...) Os radioisótopos também podem ser empregados com o propósito de diagnóstico, fornecendo informações sobre o tipo ou extensão da doença. O isótopo iodo-131 é usado para determinar o tamanho, forma e atividade da glândula tireóide. (Fonte: Química Nuclear na Medicina. http://www.qmc.ufsc.br)
A representação do iodo-131 faz referência
Avalie as duas reações de combustão a seguir e escolhaa alternativa correta, considerando que a entalpia decombustão do carbono é 9 kWh/kg e a do metano 14kWh/kg:
C + O₂➩CO₂
CH₄ + 20₂ ➩ CO₂ + 2H₂O
Dados: CH₄ + 20₂ → C0₂ + 2H₂0
Variação de entalpia: ΔH = 2800 kj/mol
Massas atômicas relativas: C = 12 H = 1
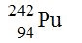
O ΔE0 da reação mostrada a seguir é igual a:
No caso de um acidente nuclear, é aconselhável tomar comprimidos de iodeto de potássio, pois ajudam a proteger a glândula tireoide.
Assinale a opção que justifica esta afirmativa.
A nitroglicerina é um líquido oleoso de cor amarelo-pálido, muito sensível ao impacto. É um dos explosivos mais fortes que existem. Sua decomposição ocorre conforme mostra a equação a seguir:

Sobre os possíveis motivos que justificam seu alto poder explosivo, foram feitas as seguintes
afirmações:
I. A energia de ligação entre os átomos de Nitrogênio, assim como entre C e O e entre H e O, são muito fortes.
II. Os produtos gasosos aumentam a pressão, consequentemente, seu poder destrutivo.
III. O aumento do grau de desordem do sistema torna a equação altamente favorável, em acordo com a segunda lei da termodinâmica.
IV. Processos endotérmicos liberam grande quantidade de energia.
Considere a figura a seguir.
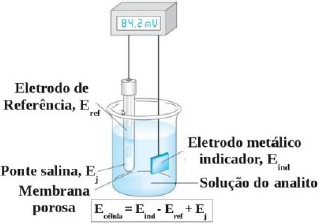
Disponível em: <http://www.c2o.pro.br/hackaguas/figuras/medida_potencial.png>. Acesso em: 2 out.2016.
Dos componentes potenciométricos do sistema representado pela figura, o potencial
“O cromo pode ser liberado para o ambiente por meio de resíduos originados de um amplo número de processamentos industriais, incluindo a indústria curtumeira, têxtil e de metalurgia do ferro, aço e outros metais. Dentre as formas normalmente encontradas na natureza, o cromo hexavalente apresenta-se como cromatos e dicromatos (CrO42- e Cr2O72- ), os quais são tóxicos e mutagênicos, solúveis em uma ampla faixa de pH e geralmente móveis no sistema solo/água. O cromo trivalente apresenta-se na forma do cátion Cr3+ e do ânion CrO2- , sendo consideravelmente menos tóxico e de baixa mobilidade, em razão de sua precipitação como óxidos e hidróxidos em pH superior a 5,0.”
Um dos processos de transformação do cromo hexavalente tóxico em cromo trivalente menos tóxico, é a reação destes compostos com ferro puro ou cátion Fe2+ como mostram as reações abaixo (a 25 ºC e 1 atm).
Fe(s) + CrO42−(aq) + 4H2O(l)  Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
6Fe2+(aq) + Cr2O72−(aq) + 14H+  6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
Dados: potenciais de redução em volts (V) a 25 ºC e 1 atm
Fe2+(aq)  Fe3+(aq) + e− E0 = −0,77
Fe3+(aq) + e− E0 = −0,77
Fe0(s)  Fe3+(aq) + 3e− E0 = 0,04
Fe3+(aq) + 3e− E0 = 0,04
CrO42−(aq) + 4H2O(l) + 3e−  Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr2O72−(aq) + 14H+ (aq) + 6e−  2Cr3+(aq) + 7H2O(l) E0 = 1,33
2Cr3+(aq) + 7H2O(l) E0 = 1,33
Considere a seguinte reação nuclear:

O isótopo Ra-223, em relação ao isótopo Rn-219, possui
Atenção: A questão refere-se ao conteúdo de Noções de Gás Natural.
Em comparação ao Gás Liquefeito de Petróleo − GLP, o gás natural tem uma maior capacidade de se dissipar na atmosfera. Isso se deve, basicamente
Com base no césio-137, é CORRETO afirmar que:
De acordo com a tabela a seguir

Numa eventual pilha entre os metais mostrados acima, aquele que será sempre o agente redutor é o: