Questões de Concurso
Sobre transformações químicas e energia em química
Foram encontradas 1.458 questões
Avalie as duas reações de combustão a seguir e escolhaa alternativa correta, considerando que a entalpia decombustão do carbono é 9 kWh/kg e a do metano 14kWh/kg:
C + O₂➩CO₂
CH₄ + 20₂ ➩ CO₂ + 2H₂O
Dados: CH₄ + 20₂ → C0₂ + 2H₂0
Variação de entalpia: ΔH = 2800 kj/mol
Massas atômicas relativas: C = 12 H = 1
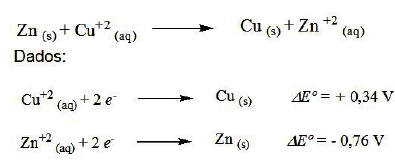
O ΔE0 da reação mostrada a seguir é igual a:
No caso de um acidente nuclear, é aconselhável tomar comprimidos de iodeto de potássio, pois ajudam a proteger a glândula tireoide.
Assinale a opção que justifica esta afirmativa.
A nitroglicerina é um líquido oleoso de cor amarelo-pálido, muito sensível ao impacto. É um dos explosivos mais fortes que existem. Sua decomposição ocorre conforme mostra a equação a seguir:

Sobre os possíveis motivos que justificam seu alto poder explosivo, foram feitas as seguintes
afirmações:
I. A energia de ligação entre os átomos de Nitrogênio, assim como entre C e O e entre H e O, são muito fortes.
II. Os produtos gasosos aumentam a pressão, consequentemente, seu poder destrutivo.
III. O aumento do grau de desordem do sistema torna a equação altamente favorável, em acordo com a segunda lei da termodinâmica.
IV. Processos endotérmicos liberam grande quantidade de energia.
Considere a figura a seguir.
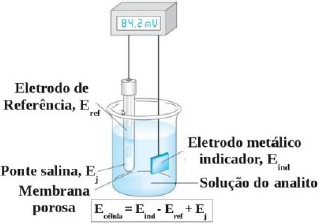
Disponível em: <http://www.c2o.pro.br/hackaguas/figuras/medida_potencial.png>. Acesso em: 2 out.2016.
Dos componentes potenciométricos do sistema representado pela figura, o potencial
“O cromo pode ser liberado para o ambiente por meio de resíduos originados de um amplo número de processamentos industriais, incluindo a indústria curtumeira, têxtil e de metalurgia do ferro, aço e outros metais. Dentre as formas normalmente encontradas na natureza, o cromo hexavalente apresenta-se como cromatos e dicromatos (CrO42- e Cr2O72- ), os quais são tóxicos e mutagênicos, solúveis em uma ampla faixa de pH e geralmente móveis no sistema solo/água. O cromo trivalente apresenta-se na forma do cátion Cr3+ e do ânion CrO2- , sendo consideravelmente menos tóxico e de baixa mobilidade, em razão de sua precipitação como óxidos e hidróxidos em pH superior a 5,0.”
Um dos processos de transformação do cromo hexavalente tóxico em cromo trivalente menos tóxico, é a reação destes compostos com ferro puro ou cátion Fe2+ como mostram as reações abaixo (a 25 ºC e 1 atm).
Fe(s) + CrO42−(aq) + 4H2O(l)  Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
6Fe2+(aq) + Cr2O72−(aq) + 14H+  6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
Dados: potenciais de redução em volts (V) a 25 ºC e 1 atm
Fe2+(aq)  Fe3+(aq) + e− E0 = −0,77
Fe3+(aq) + e− E0 = −0,77
Fe0(s)  Fe3+(aq) + 3e− E0 = 0,04
Fe3+(aq) + 3e− E0 = 0,04
CrO42−(aq) + 4H2O(l) + 3e−  Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr2O72−(aq) + 14H+ (aq) + 6e−  2Cr3+(aq) + 7H2O(l) E0 = 1,33
2Cr3+(aq) + 7H2O(l) E0 = 1,33
Considere a seguinte reação nuclear:

O isótopo Ra-223, em relação ao isótopo Rn-219, possui
Atenção: A questão refere-se ao conteúdo de Noções de Gás Natural.
Em comparação ao Gás Liquefeito de Petróleo − GLP, o gás natural tem uma maior capacidade de se dissipar na atmosfera. Isso se deve, basicamente
Com base no césio-137, é CORRETO afirmar que:
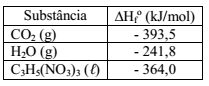
De acordo com a tabela a seguir

Numa eventual pilha entre os metais mostrados acima, aquele que será sempre o agente redutor é o:
A nitroglicerina é um explosivo poderoso que ao detonar forma quatro gases diferentes, conforme apresentado na reação não balanceada:
C3H5(NO3)3 (ℓ) → N2 (g) + O2 (g) + CO2 (g) + H2O (g)
Determine a energia liberada (kJ/mol) na detonação de 100 g de nitroglicerina, a partir da tabela abaixo e considerando que H = 1u; C = 12u; N = 14u; O = 16u:
Em reatores nucleares, a energia é gerada pela reação de fissão do isótopo 235 do urânio (U-235). Esse elemento, quando absorve um nêutron (n), transforma-se no isótopo U-236, que espontaneamente gera dois elementos mais leves, nêutrons e energia, como indicado nas equações a seguir:
235U92 + n → 236U92
236U92 → 86Kr36 + 144Ba56 + x.n + energia
Sabendo-se que o número de prótons e nêutrons deve ser igual antes e depois da fissão do U-236, quantos nêutrons (x)
são liberados nesse processo?